Содержание
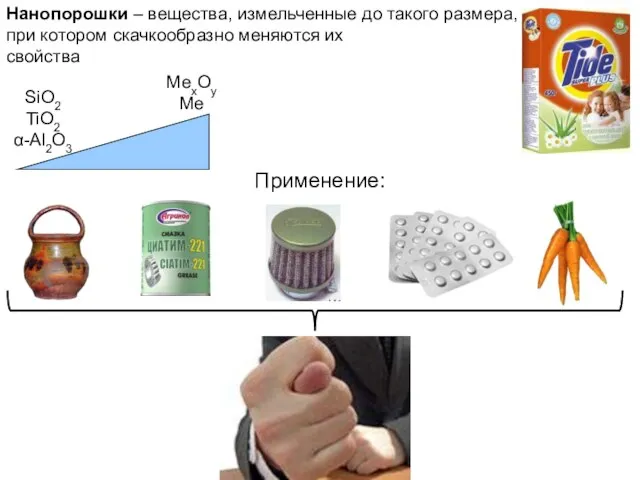
- 2. Нанопорошки – вещества, измельченные до такого размера, при котором скачкообразно меняются их свойства SiO2 TiO2 α-Al2O3
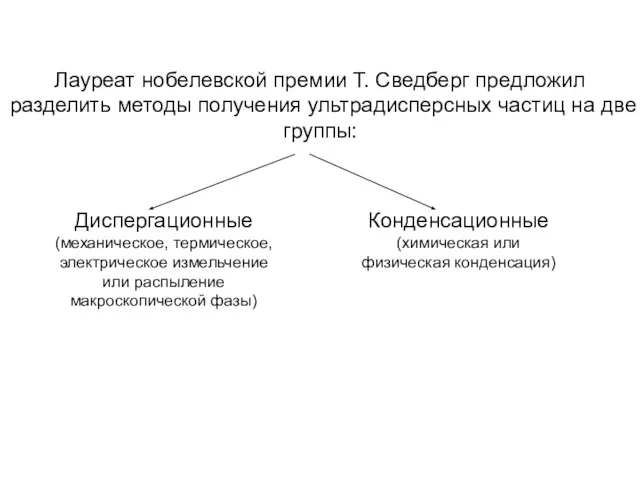
- 3. Лауреат нобелевской премии Т. Сведберг предложил разделить методы получения ультрадисперсных частиц на две группы: Диспергационные (механическое,
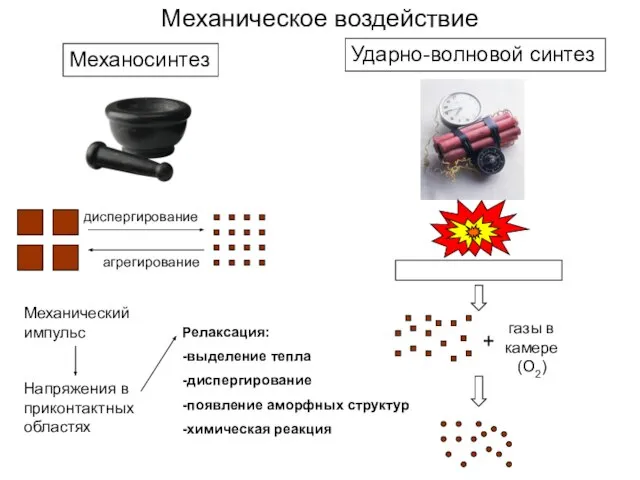
- 4. Механическое воздействие Механосинтез Ударно-волновой синтез + газы в камере (O2) диспергирование агрегирование Механический импульс Напряжения в
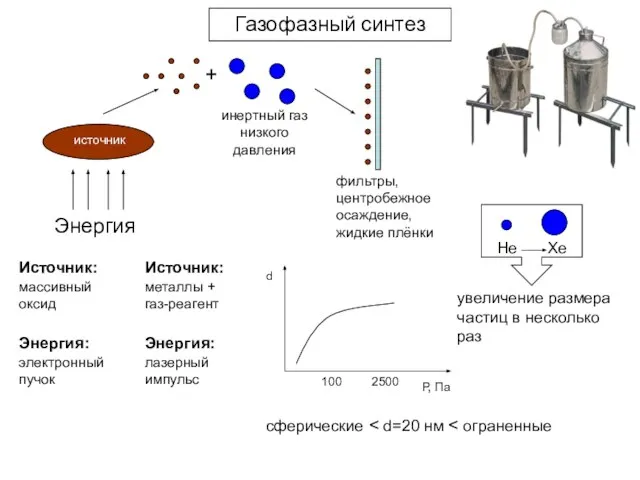
- 5. Газофазный синтез Энергия + инертный газ низкого давления фильтры, центробежное осаждение, жидкие плёнки Источник: Источник: массивный
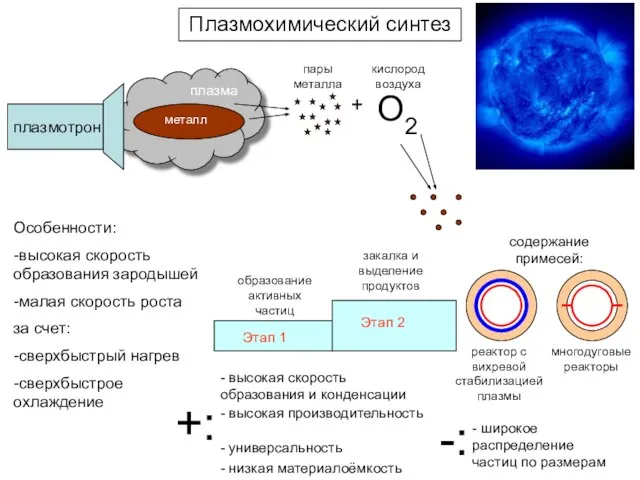
- 6. Плазмохимический синтез плазма плазмотрон пары металла + O2 кислород воздуха Особенности: -высокая скорость образования зародышей -малая
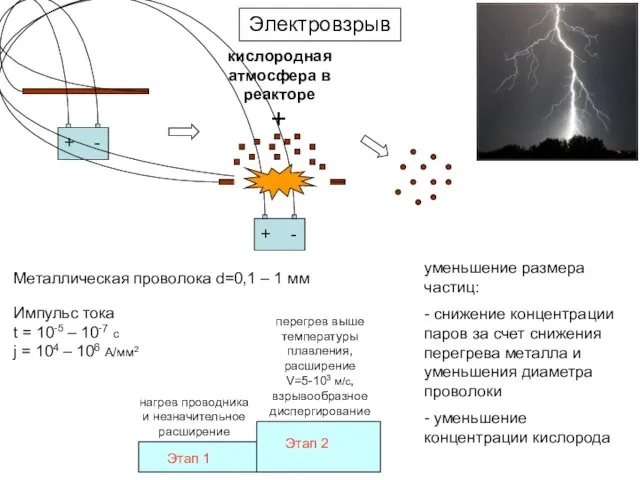
- 7. Электровзрыв + кислородная атмосфера в реакторе Металлическая проволока d=0,1 – 1 мм Импульс тока t =
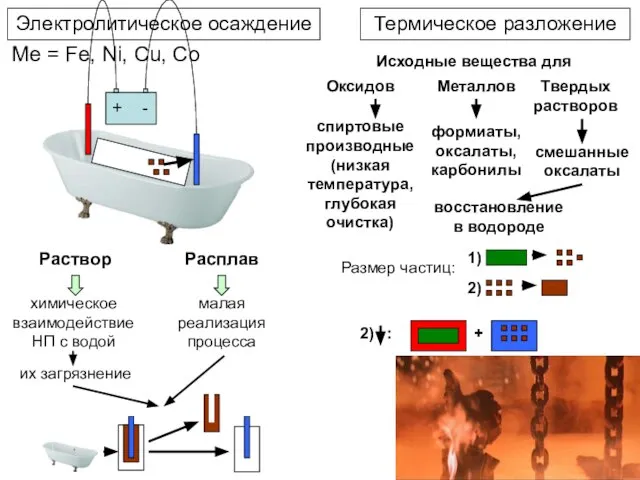
- 8. Электролитическое осаждение Me = Fe, Ni, Cu, Co Термическое разложение Раствор Расплав химическое взаимодействие НП с
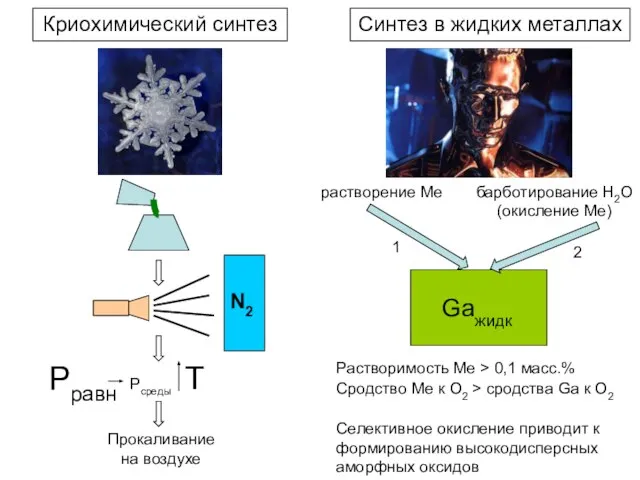
- 9. Синтез в жидких металлах Криохимический синтез Gaжидк 1 2 растворение Me барботирование H2O (окисление Мe) Растворимость
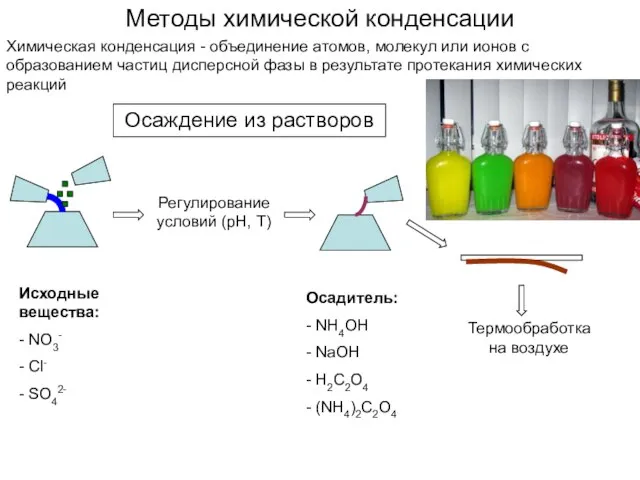
- 10. Методы химической конденсации Химическая конденсация - объединение атомов, молекул или ионов с образованием частиц дисперсной фазы
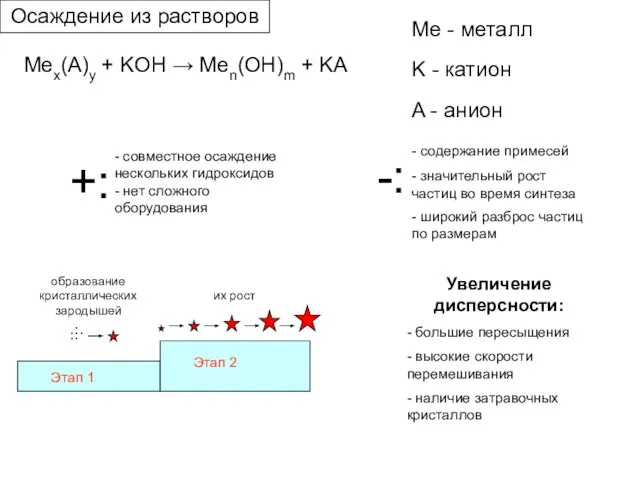
- 11. Mex(A)y + KOH → Men(OH)m + KA Me - металл K - катион A - анион
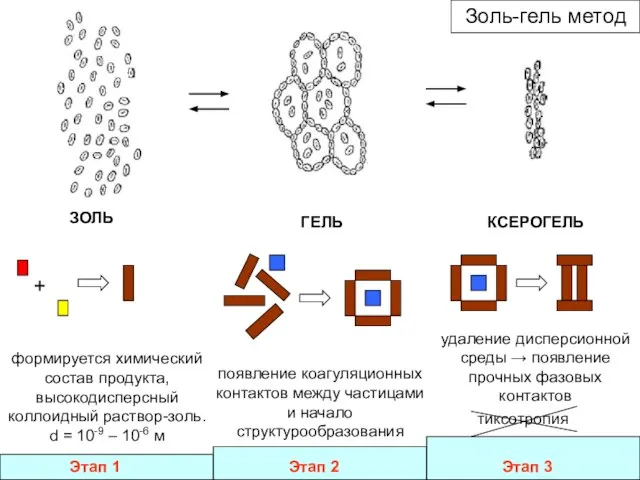
- 12. Золь-гель метод Золь – дисперсная система с жидкой дисперсионной средой и твердой дисперсной фазой Гель –
- 13. формируется химический состав продукта, высокодисперсный коллоидный раствор-золь. d = 10-9 – 10-6 м ЗОЛЬ ГЕЛЬ КСЕРОГЕЛЬ
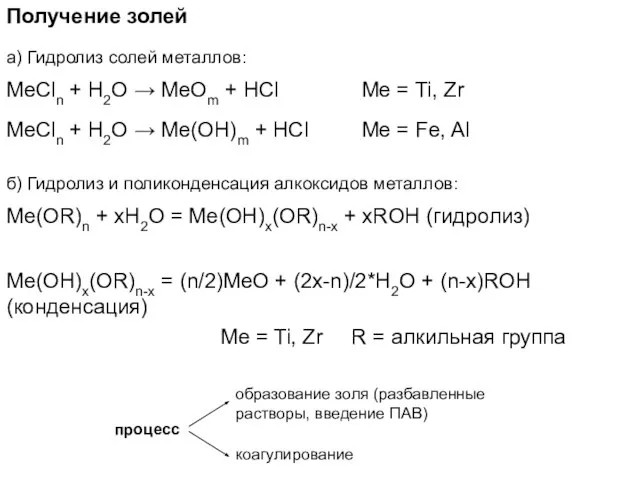
- 14. Получение золей а) Гидролиз солей металлов: MeCln + H2O → MeOm + HCl MeCln + H2O
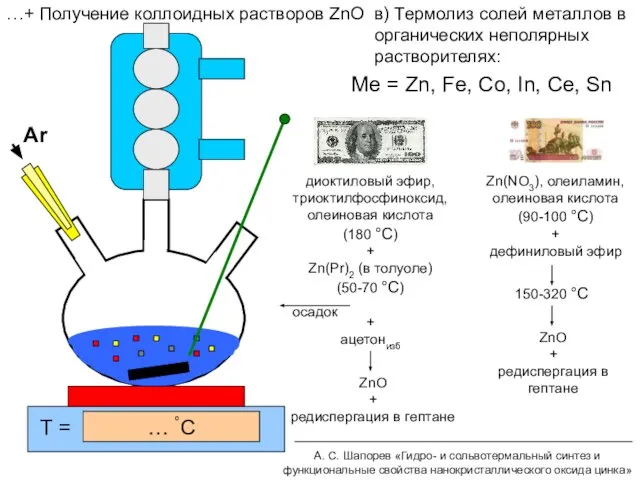
- 15. в) Термолиз солей металлов в органических неполярных растворителях: Me = Zn, Fe, Co, In, Ce, Sn
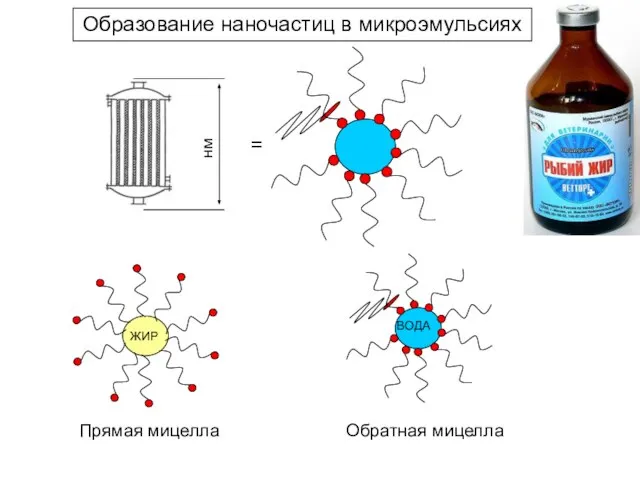
- 16. Образование наночастиц в микроэмульсиях = Прямая мицелла Обратная мицелла
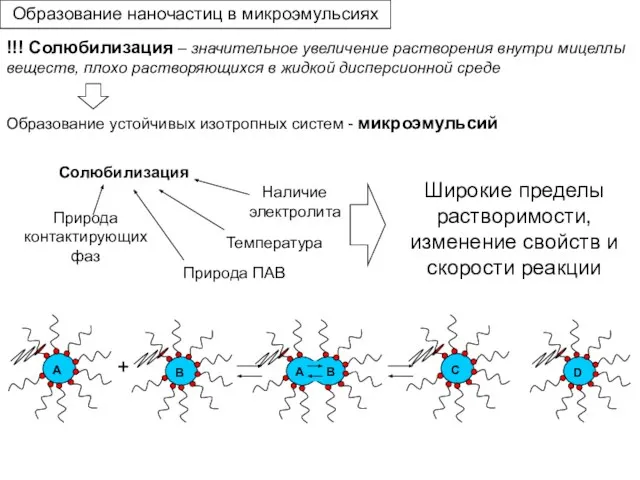
- 17. !!! Солюбилизация – значительное увеличение растворения внутри мицеллы веществ, плохо растворяющихся в жидкой дисперсионной среде Солюбилизация
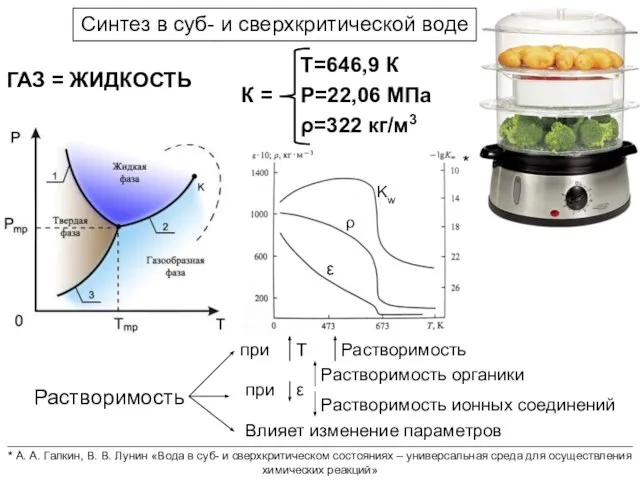
- 18. Синтез в суб- и сверхкритической воде ГАЗ = ЖИДКОСТЬ Растворимость при Т Растворимость при ε Растворимость
- 19. ВОДА среда, передающая давление Синтез фаз, не стабильных при высоких температурах Механизм образования оксидов: MLx +
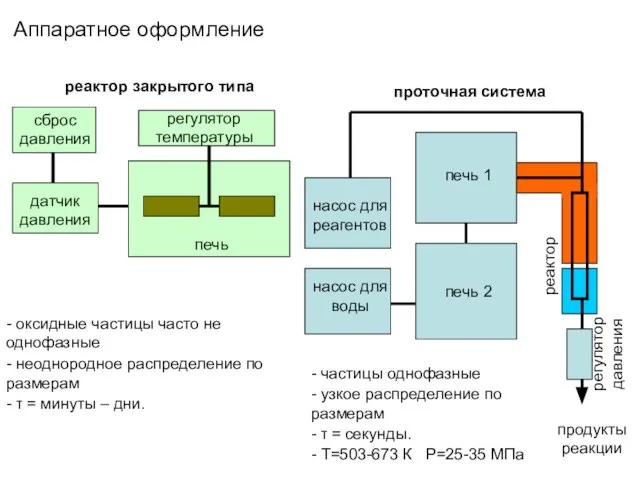
- 20. Аппаратное оформление реактор закрытого типа проточная система сброс давления датчик давления регулятор температуры печь насос для
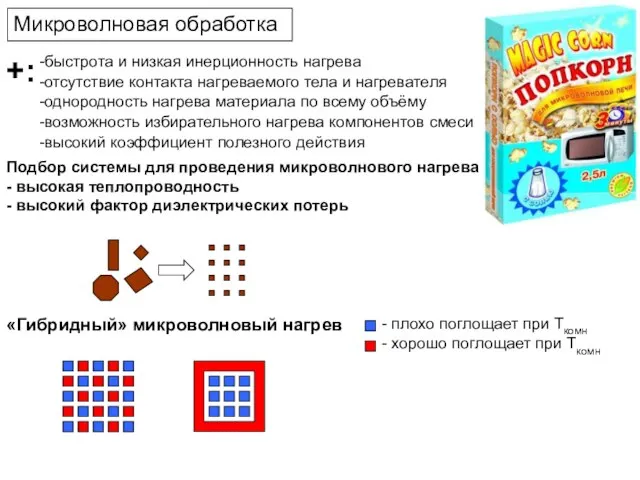
- 21. Микроволновая обработка «Гибридный» микроволновый нагрев - хорошо поглощает при Ткомн - плохо поглощает при Ткомн
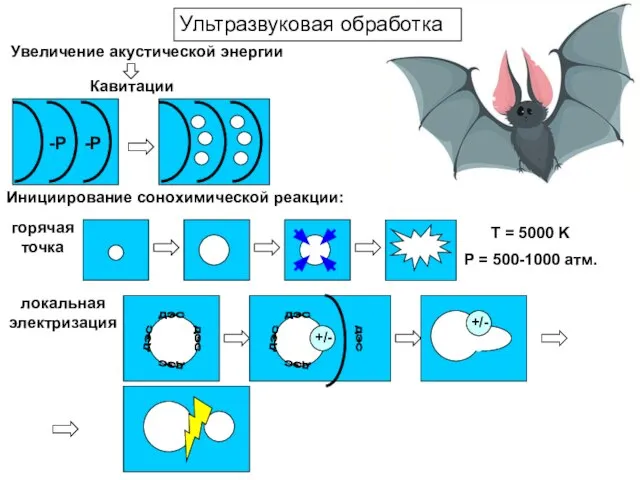
- 22. Увеличение акустической энергии Кавитации горячая точка Инициирование сонохимической реакции: T = 5000 K P = 500-1000
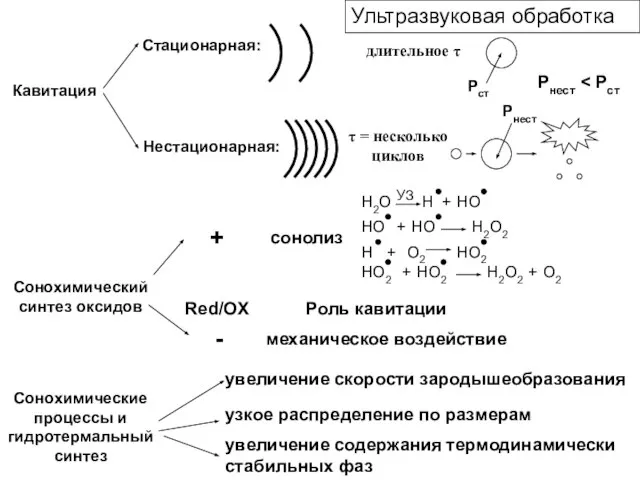
- 23. Кавитация Стационарная: Нестационарная: τ = несколько циклов длительное τ Рст Рнест Рнест Сонохимический синтез оксидов Red/OX
- 25. Скачать презентацию


 Становление герба Самарской губернии
Становление герба Самарской губернии Франкл: логотерапия. Логотерапия, как терапия смыслом
Франкл: логотерапия. Логотерапия, как терапия смыслом Alla stazione. In carrozza, si parte
Alla stazione. In carrozza, si parte Small talk
Small talk  Русская матрёшка
Русская матрёшка о математике и математиках
о математике и математиках Система менеджмента качестваЧТТПиК 2009-2010
Система менеджмента качестваЧТТПиК 2009-2010 Система менеджмента качества в образовании
Система менеджмента качества в образовании Муниципальное общеобразовательное учреждение средняя общеобразовательная школа №11 г.Вичуга Ивановской области Электронное пр
Муниципальное общеобразовательное учреждение средняя общеобразовательная школа №11 г.Вичуга Ивановской области Электронное пр 1_Лекція Будова атома
1_Лекція Будова атома Гжель. Элементы росписи
Гжель. Элементы росписи БЕТМАН ПРОТИВ ДЖОКЕРА
БЕТМАН ПРОТИВ ДЖОКЕРА Урок как педагогический феномен
Урок как педагогический феномен Театральные маски. Рисуем маску сказочного героя
Театральные маски. Рисуем маску сказочного героя Портфолио Касьяновой Н.А.
Портфолио Касьяновой Н.А. Удивительное начало великой поэмы
Удивительное начало великой поэмы Власова И.В. – старший преподаватель КНО, методист отдела научной работы ГОУ ДПО ЧИПКРО, Почетный работник общего образования Твор
Власова И.В. – старший преподаватель КНО, методист отдела научной работы ГОУ ДПО ЧИПКРО, Почетный работник общего образования Твор Деятельностный подход в образовании
Деятельностный подход в образовании Атом құрылысы туралы жалпы түсінік. Квант сандары
Атом құрылысы туралы жалпы түсінік. Квант сандары Презентация на тему Русские народные танцы
Презентация на тему Русские народные танцы  Тестирование Пользовательского Интерфейсакак это делает Интел
Тестирование Пользовательского Интерфейсакак это делает Интел Институты государственной власти (тема 7)
Институты государственной власти (тема 7) Физика и техника – тебе, фронт!
Физика и техника – тебе, фронт! Известные творческие коллективы Омска
Известные творческие коллективы Омска Christmas Day
Christmas Day Thema: “Wie orientiert man sich in einer fremden Grossstadt?”
Thema: “Wie orientiert man sich in einer fremden Grossstadt?” Применение ИКТ для подготовки к ЕГЭ по математике
Применение ИКТ для подготовки к ЕГЭ по математике Николай Михайлович Карамзин
Николай Михайлович Карамзин