Содержание
- 2. Давайте вспомним, что мы знаем о важнейших классах углеводородов, сравним их строение, физические и химические свойства.
- 3. Сравнительная характеристика углеводородов
- 4. Сравнительная характеристика углеводородов
- 5. Сравнительная характеристика углеводородов (продолжение)
- 6. Сравнительная характеристика углеводородов (продолжение)
- 7. Представитель от каждой группы должен подойти к столу и взять конверт с набором карточек и принести
- 8. Алкены Алканы Алкадиены Алкины Арены Циклоалканы А теперь расскажем свои увлекательные истории
- 9. Представитель от каждой группы вновь подойдет к столу и возьмет конверт с набором карточек и принесет
- 10. Время представить свое решение…. Кто первый?
- 11. № 1. С3Н8 С3Н7Сl C3H6 C3H6Br2 C3H4 C3H6O C3H8 + Cl2 (свет) С3Н7Сl + HCl С3Н7Сl
- 12. № 2. С2Н5Br С2Н4 C2H4Cl2 C2H2 C6H6 C6H5Cl C2H5Br + NaOH (спирт) СН2 = СН2 +
- 13. № 3. С2Н6 С2Н5Сl C4H10 C4H9Cl C4H8 C4H9OH C2H6 + Cl2 (свет) С2Н5Сl + HCl 2С2Н5Сl
- 14. № 4. С2Н2 С6Н6 C6H12 C6H14 C6H13Cl C6H12 3C2H2 (C акт) С6Н6 С6Н6 + 3Н2 С6Н12
- 15. № 5. С2Н5 OH С2Н4 C2H5Cl C2H4Cl2 C2H2 C6H6 C2H5OH (H2SO4) СН2 = СН2 СН2 =
- 16. Ну и что в ней особенного? Обычные слова, как и во всех теориях Михаил Алексей Какая
- 17. 1-я группа: Все атомы, образующие молекулы органических веществ, связаны в определенной последовательности согласно их валентностям 2-я
- 18. Пришло время следующего испытания – решения задачи – загадки Вы получите карточку с номером и условием
- 19. Задача «Газ, выделяющийся из трещин в земле». Ещё римляне были знакомы с горючими свойствами газов, выделяющихся
- 20. Задача № 2. Ваше решение? Задача «Греческий огонь» Подлинным открытием древности было изобретение “греческого огня”. Учёными
- 21. Задача № 3. Ваше решение? Задача «Маслородный газ» В 1680 году Беккер упоминает о получении “горючего
- 22. Задача № 4. Ваше решение? Задача: «Газ, используемый для освещения». Этот газ был получен в 1836
- 23. Задача № 5. Ваше решение? Задача «Сильнейшее наркотическое средство». Это вещество было получено Либихом в 1831
- 24. Подведем итоги вашей работы в группах? Возьмите конверт, напишите на нем свое имя, вложите в него
- 26. Скачать презентацию
Слайд 2Давайте вспомним, что мы знаем о важнейших классах углеводородов,
сравним их строение,
Давайте вспомним, что мы знаем о важнейших классах углеводородов,
сравним их строение,

Возможно нам удастся:
увидеть закономерности,
проследить взаимосвязи
доказать положения теории А.М. Бутлерова
Мы будем работать по одному, в парах и группах.
Мы будем доказывать свою точку зрения
Но мы не будем забывать, что могут быть и другие точки зрения
Мы будем помнить, что «терпение – это ключ, открывающий все двери»
Не допустимо:
Слайд 3Сравнительная характеристика углеводородов
Сравнительная характеристика углеводородов
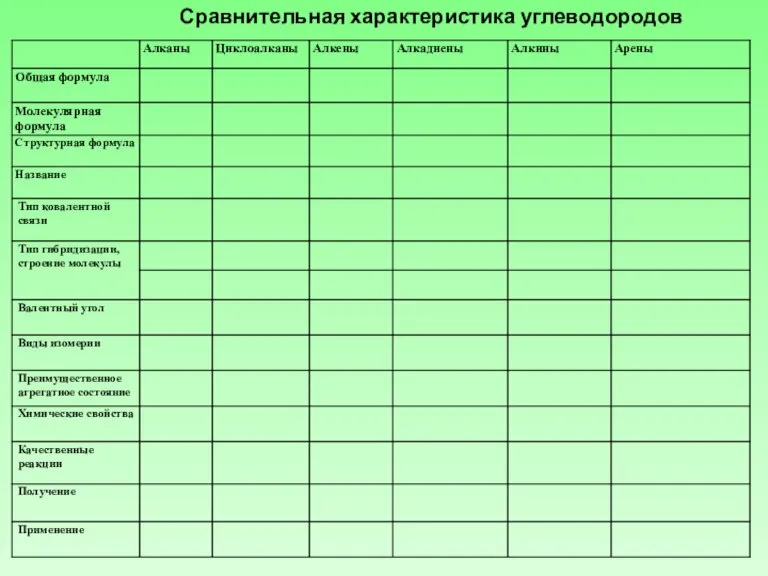
Слайд 4Сравнительная характеристика углеводородов
Сравнительная характеристика углеводородов
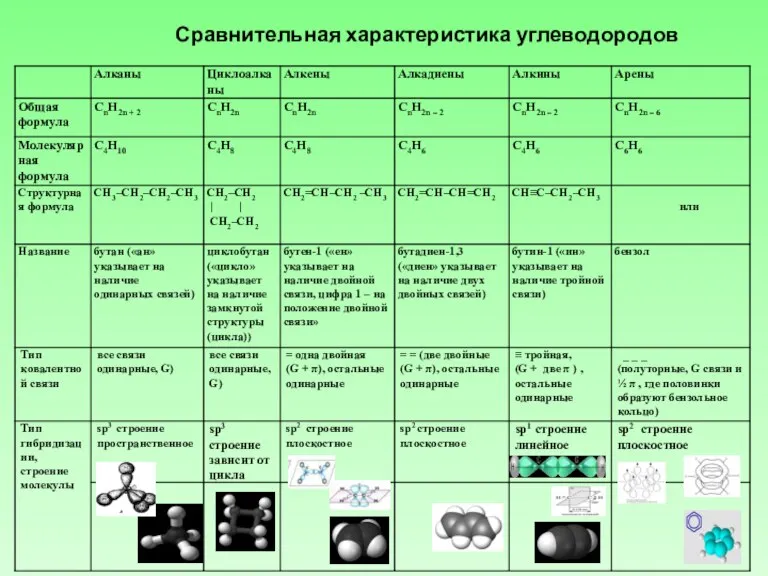
Слайд 5Сравнительная характеристика углеводородов (продолжение)
Сравнительная характеристика углеводородов (продолжение)
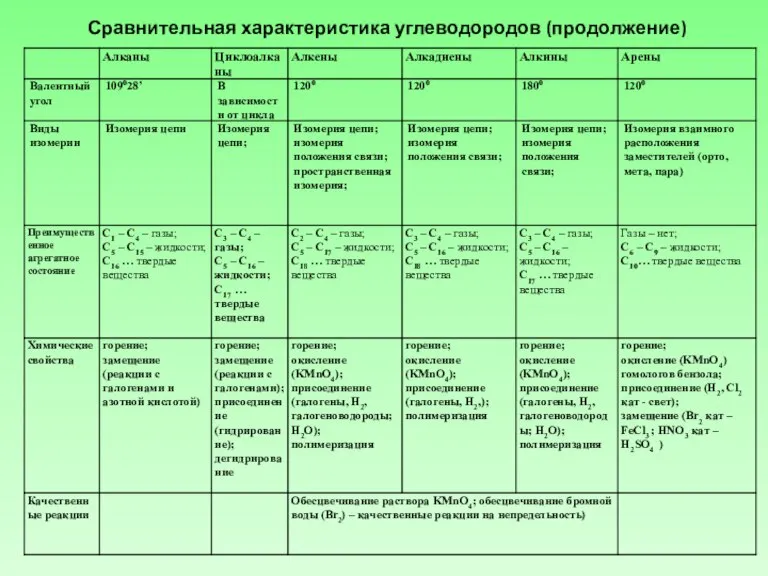
Слайд 6Сравнительная характеристика углеводородов (продолжение)
Сравнительная характеристика углеводородов (продолжение)
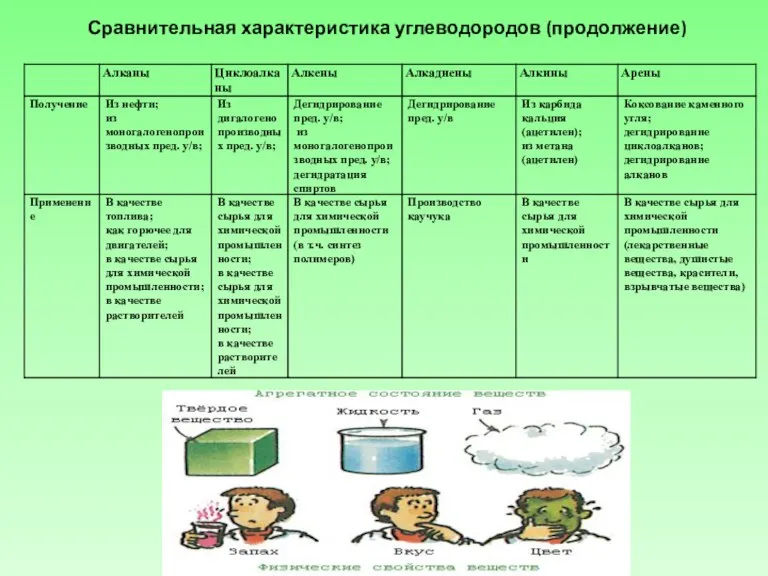
Слайд 7Представитель от каждой группы должен подойти к столу и взять конверт с
Представитель от каждой группы должен подойти к столу и взять конверт с

У вас будет 15 минут на то, чтобы составить рассказ о своем классе углеводородов. Рассказ следует составить от имени класса углеводородов, например, «Мы, алканы…» Нужно рассказать о себе (строении), своей жизни (свойствах, применении, получении и т.п.), о том какие проблемы вас (класс углеводородов) волнуют, какие трудности вы встречаете, как вы относитесь к другим веществам, и как бы вы хотели, чтобы относились к вам.
Представить «свой» класс углеводородов (рассказать остальным) вы можете по разному - это может быть один человек из группы, несколько или вся группа.
Составляя рассказ старайтесь придерживаться истины, но можете и немножко пофантазировать…
Давайте составим рассказ
Давайте составим рассказ
Слайд 8Алкены
Алканы
Алкадиены
Алкины
Арены
Циклоалканы
А теперь расскажем свои увлекательные истории
Алкены
Алканы
Алкадиены
Алкины
Арены
Циклоалканы
А теперь расскажем свои увлекательные истории
Слайд 9Представитель от каждой группы вновь подойдет к столу и возьмет конверт с
Представитель от каждой группы вновь подойдет к столу и возьмет конверт с

На этот раз на карточках написаны вещества, из которых нужно сначала составить цепочку превращений, а затем решить ее, то есть составить уравнения реакций.
На выполнение задания у группы будет 10 минут, затем группа должна будет представить свою цепочку и свое решение.
Также как и в предыдущем задании вы можете по разному представлять реш - это может быть один человек из группы, несколько или вся группа.
Выполняя это задание старайтесь придерживаться истины, фантазировать не желательно…
Давайте подумаем о превращениях углеводородов
и о том, как они связаны между собой
Давайте подумаем о превращениях углеводородов
и о том, как они связаны между собой
Слайд 10Время представить свое решение…. Кто первый?
Время представить свое решение…. Кто первый?
Слайд 11№ 1.
С3Н8 С3Н7Сl C3H6 C3H6Br2 C3H4 C3H6O
C3H8 + Cl2 (свет)
№ 1.
С3Н8 С3Н7Сl C3H6 C3H6Br2 C3H4 C3H6O
C3H8 + Cl2 (свет)
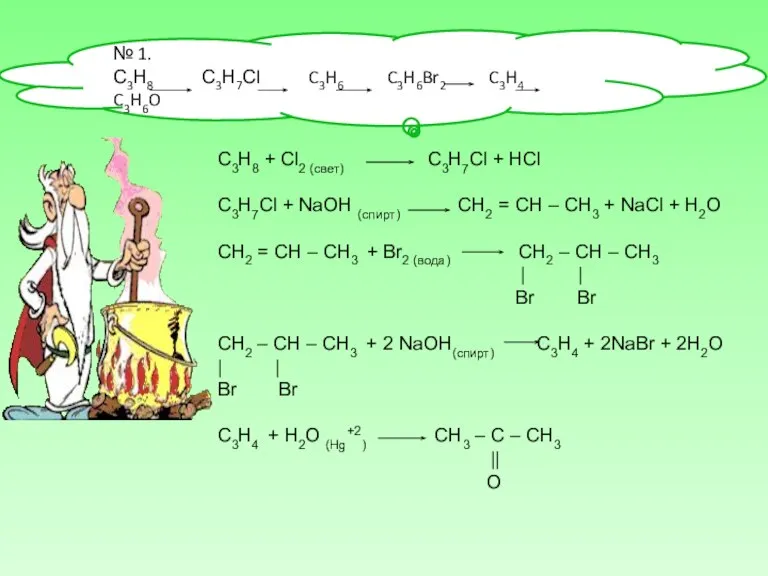
С3Н7Сl + NaOH (спирт) СН2 = СН – СН3 + NaCl + H2O
СН2 = СН – СН3 + Br2 (вода) CH2 – CH – CH3
| |
Br Br
CH2 – CH – CH3 + 2 NaOH(спирт) C3H4 + 2NaBr + 2H2O
| |
Br Br
C3H4 + H2O (Hg+2) CH3 – C – CH3
||
O
Слайд 12№ 2.
С2Н5Br С2Н4 C2H4Cl2 C2H2 C6H6 C6H5Cl
C2H5Br + NaOH (спирт)
№ 2.
С2Н5Br С2Н4 C2H4Cl2 C2H2 C6H6 C6H5Cl
C2H5Br + NaOH (спирт)
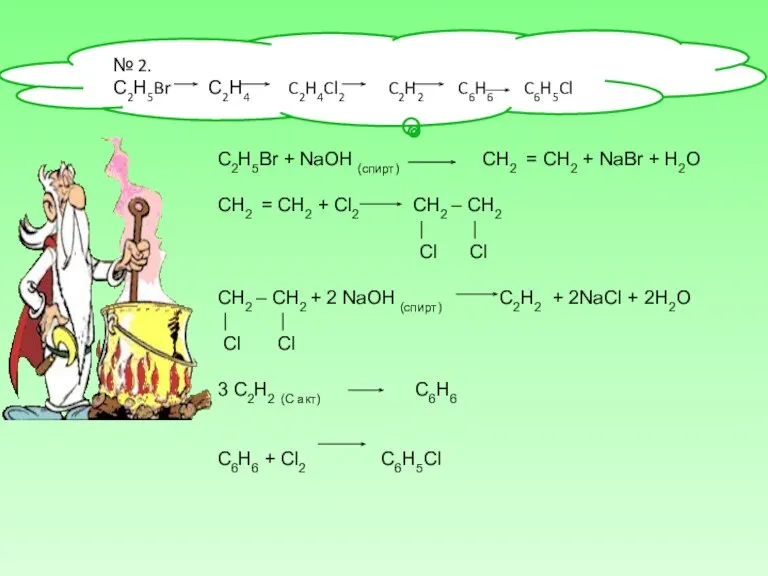
СН2 = СН2 + Cl2 СН2 – СН2
| |
Cl Cl
СН2 – СН2 + 2 NaOH (спирт) C2H2 + 2NaCl + 2H2O
| |
Cl Cl
3 C2H2 (C акт) С6Н6
C6H6 + Сl2 С6Н5Cl
Слайд 13№ 3.
С2Н6 С2Н5Сl C4H10 C4H9Cl C4H8 C4H9OH
C2H6 + Cl2 (свет)
№ 3.
С2Н6 С2Н5Сl C4H10 C4H9Cl C4H8 C4H9OH
C2H6 + Cl2 (свет)
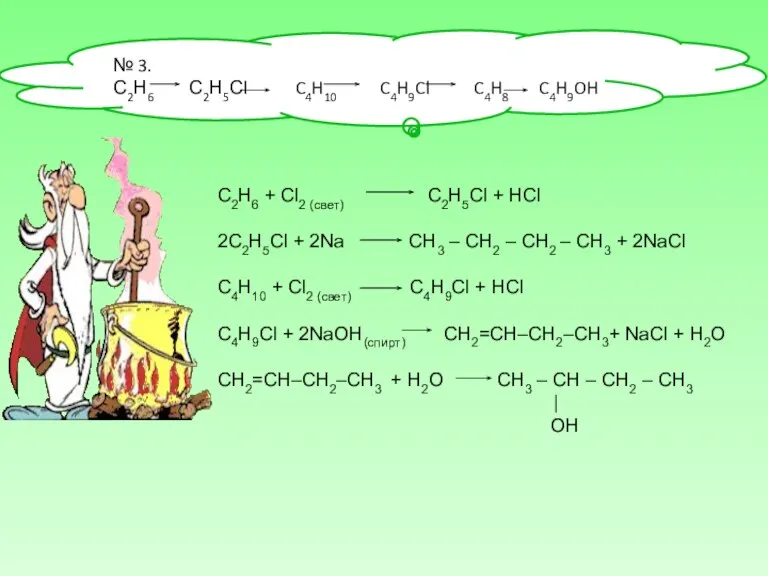
2С2Н5Сl + 2Na СН3 – СН2 – СН2 – CH3 + 2NaCl
C4H10 + Cl2 (свет) C4H9Сl + HCl
C4H9Сl + 2NaOH(спирт) CH2=CH–CH2–CH3+ NaCl + H2O
CH2=CH–CH2–CH3 + H2O CH3 – CH – CH2 – CH3
|
OH
Слайд 14№ 4.
С2Н2 С6Н6 C6H12 C6H14 C6H13Cl C6H12
3C2H2 (C акт) С6Н6
С6Н6
№ 4.
С2Н2 С6Н6 C6H12 C6H14 C6H13Cl C6H12
3C2H2 (C акт) С6Н6
С6Н6
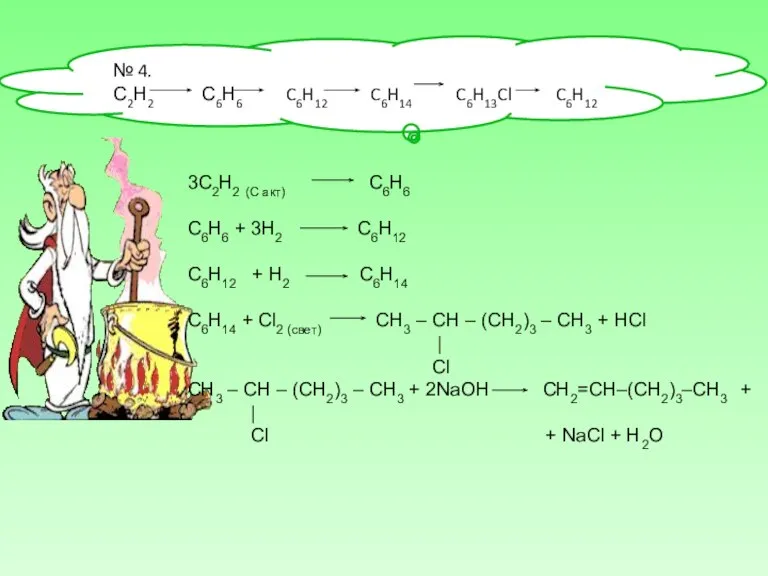
С6Н12 + Н2 С6Н14
С6Н14 + Сl2 (свет) СН3 – СН – (СН2)3 – СН3 + HCl
|
Cl
СН3 – СН – (СН2)3 – СН3 + 2NaOH CH2=CH–(CH2)3–CH3 +
|
Cl + NaCl + H2O
Слайд 15№ 5.
С2Н5 OH С2Н4 C2H5Cl C2H4Cl2 C2H2 C6H6
C2H5OH (H2SO4) СН2
№ 5.
С2Н5 OH С2Н4 C2H5Cl C2H4Cl2 C2H2 C6H6
C2H5OH (H2SO4) СН2
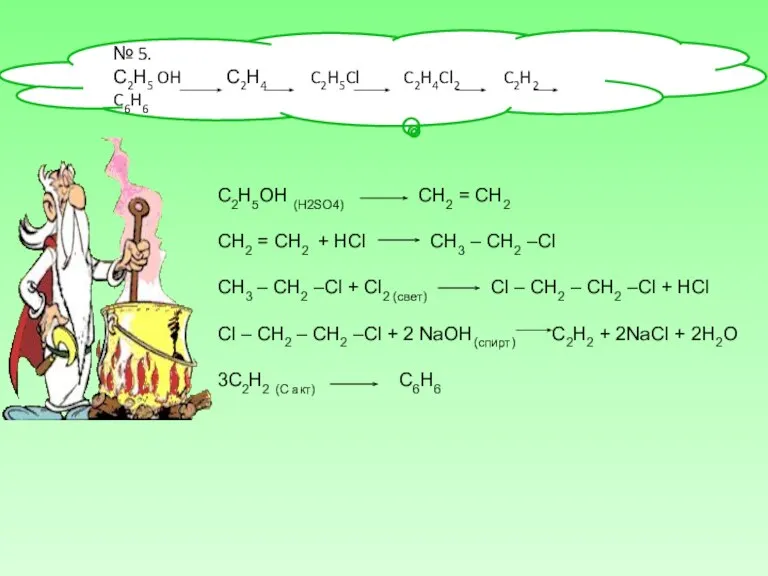
СН2 = СН2 + HCl СН3 – СН2 –Cl
СН3 – СН2 –Cl + Cl2 (свет) Сl – СН2 – СН2 –Cl + HCl
Сl – СН2 – СН2 –Cl + 2 NaOH(спирт) C2H2 + 2NaCl + 2H2O
3C2H2 (C акт) С6Н6
Слайд 16Ну и что в ней особенного?
Обычные слова, как и во всех
Ну и что в ней особенного?
Обычные слова, как и во всех

Михаил
Алексей
Какая особенная теория органических соединений у Александра Михайловича Бутлерова и как верно и четко все сформулировано! Каждое положение о многом говорит!
Посмотрите на спор юношей о теории строения органических соединений
Слайд 171-я группа: Все атомы, образующие молекулы органических веществ, связаны в определенной
последовательности
1-я группа: Все атомы, образующие молекулы органических веществ, связаны в определенной
последовательности

2-я группа: Свойства веществ зависят не только от того, сколько и каких атомов входит в состав
молекул, но и от того, как они соединены
3-я группа: По свойствам данного вещества можно определить его строение, а по строению
предвидеть свойства
4-я группа: Атомы и группы атомов в молекулах органических веществ взаимно влияют друг на друга
а 5-ой группе - предлагается «играть» на стороне Алексея, приготовить вопросы для остальных групп
И попробуйте помочь Михаилу «перетащить» Алексея на свою сторону
Номера групп определите по номеру предыдущего задания – цепочки превращений
Группам 1, 2, 3, 4 предлагается попытаться доказать отдельные положения теории
Слайд 18Пришло время следующего испытания – решения задачи – загадки
Вы получите карточку
Пришло время следующего испытания – решения задачи – загадки
Вы получите карточку

У вас будет 7 минут на то, чтобы решить задачу.
Представить свое решение вы можете по разному – это может быть один человек из группы, несколько или вся группа. При представлении задачи целесообразно начать с ее условия, а затем поделиться вашими размышлениями
Слайд 19Задача «Газ, выделяющийся из трещин в земле».
Ещё римляне были знакомы с горючими
Задача «Газ, выделяющийся из трещин в земле».
Ещё римляне были знакомы с горючими

В XV веке были отмечены случаи взрывов рудничного газа.
Болотный газ был известен ещё раньше.
Однако, после того, как Кавендиш в 1766 году описал водород (“горючий воздух”), некоторое время все горючие газы отождествляли с водородом.
Бертолле в 1785 году исследовал болотный газ и установил, что при его горении выделяется углекислота.
Что представляют собой газ, выделяющийся из трещин, рудничный газ, болотный газ?
Откуда произошли эти названия?
Дайте объяснение открытию Бертолле.
Итак, задача № 1. Ваше решение?
Слайд 20Задача № 2. Ваше решение?
Задача «Греческий огонь»
Подлинным открытием древности было изобретение “греческого
Задача № 2. Ваше решение?
Задача «Греческий огонь»
Подлинным открытием древности было изобретение “греческого

Что составляло основу “греческого огня”?
С чем связана длительность описанного пожара?
Слайд 21Задача № 3. Ваше решение?
Задача «Маслородный газ»
В 1680 году Беккер упоминает о
Задача № 3. Ваше решение?
Задача «Маслородный газ»
В 1680 году Беккер упоминает о

При реакции с хлороводородом этот газ образует жидкость, которая используется как наружное местноанестезирующее средство при проведении несложных операций (оно как бы “замораживает кожу”).
О каком газе идёт речь?
Какие жидкости образуются при реакциях с хлором и с хлороводородом?
Как Беккер получил этот газ?
Слайд 22Задача № 4. Ваше решение?
Задача: «Газ, используемый для освещения».
Этот газ был получен
Задача № 4. Ваше решение?
Задача: «Газ, используемый для освещения».
Этот газ был получен

В прежние времена, когда в большой моде были велосипеды, а электрические фонари с батарейками ещё не получили широкого распространения, сосуды с вышеуказанной солью нередко использовали для велофонарей. В такой сосуд по каплям стекала вода, а образующийся газ поступал в горелку, освещавшую путь велосипедисту. Использовался этот газ и в фарах первых автомобилей…
Ле Шателье в 1895 году открыл, что равная смесь этого газа и кислорода даёт самое горячее пламя (ок.40000с) из всех известных тогда и, следовательно, может применяться для сварки.
Назовите этот газ.
Укажите способ его получения, описанный в рассказе.
С чем связано его использование “для освещения” в прежние времена?
Слайд 23Задача № 5. Ваше решение?
Задача «Сильнейшее наркотическое средство».
Это вещество было получено Либихом
Задача № 5. Ваше решение?
Задача «Сильнейшее наркотическое средство».
Это вещество было получено Либихом

Оно используется уже 150 лет. Ещё в1847 году его впервые испытал на больных английский врач Джеймс Симпсон. Позже он применил его, что-бы облегчить королеве Виктории рождение ребёнка. Ему было не так легко добиться согласия на это: многие считали, что способность испы-тывать боль дана человеку богом и что вмешиваться в его замыслы – кощунство. Однако д-р Симпсон возражал, что, согласно Библии, бог, создавая Еву из ребра Адама, сам не обошёлся без анестезии: “И навёл Господь Бог на человека крепкий сон; и, когда он уснул, взял одно из рёбр его, и закрыл то место плотию”. Этот довод решил спор, а тот факт, что наркозом воспользовалась королева Виктория, сильно способствовал его распространению…
Это вещество является галогенопроизводным метана; его преимущество перед другими анестезирующими средствами – негорючесть, а его недостаток – сильная токсичность.
О каком веществе идёт речь?
Как его можно получить из метана?
С чем связана его негорючесть?
Слайд 24Подведем итоги вашей работы в группах?
Возьмите конверт, напишите на нем свое имя,
Подведем итоги вашей работы в группах?
Возьмите конверт, напишите на нем свое имя,

Достаньте бумагу из конверта, который Вам передали, и напишите что-нибудь положительное, что Вы заметили во время совместной работы в группе о человеке, имя которого указано на конверте. Сложите бумагу и положите обратно в конверт.
Передайте конверт соседу справа, получите следующий конверт от соседа слева и повторите все сначала.
Когда Ваш конверт вернется к Вам, прочитайте комментарии. Если у Вас появилось желание поделиться этими комментариями с членами команды, Вы можете это сделать.
Обдумайте комментарии, чтобы использовать их для групповой работы в будущем.
Внимание! Приемлемо: «у тебя всегда есть в запасе хорошие идеи», «ты всегда излагаешь свои идеи в приятной манере», «ты всегда следишь за тем, чтобы у каждого члена команды была возможность высказаться»
Неприемлемо: «ты много шумишь и этим раздражаешь всю команду», «у тебя красивая блузка»
 Новый год
Новый год Актуальные задачи реализации ФГОС НОО и пути их решения средствами УМК ИЗДАТЕЛЬСТВА «ПРОСВЕЩЕНИЕ» для начальной школы «ШКОЛА РО
Актуальные задачи реализации ФГОС НОО и пути их решения средствами УМК ИЗДАТЕЛЬСТВА «ПРОСВЕЩЕНИЕ» для начальной школы «ШКОЛА РО Презентация на тему Архиваторы
Презентация на тему Архиваторы  Презентация на тему Древняя Индия
Презентация на тему Древняя Индия Presentation Title Your company information
Presentation Title Your company information  Цунами и их характеристика (7 класс)
Цунами и их характеристика (7 класс) Физиология высшей нервной деятельности Ассоциативное обучение у человека
Физиология высшей нервной деятельности Ассоциативное обучение у человека Индивидуальное обслуживание пользователей в библиотеке
Индивидуальное обслуживание пользователей в библиотеке Военнослужащий – патриот, с честью и достоинством несущий звание защитника Отечества.
Военнослужащий – патриот, с честью и достоинством несущий звание защитника Отечества. Включение проектной и исследовательской деятельности в Образовательную программу ОУ в соответствии с ФГОС
Включение проектной и исследовательской деятельности в Образовательную программу ОУ в соответствии с ФГОС Система мотивации заместителя директора салона
Система мотивации заместителя директора салона Художник Алексей Адамов
Художник Алексей Адамов Coming and going
Coming and going  Технология составления алгоритмов и программы для решения линейных задач на языке Паскаль
Технология составления алгоритмов и программы для решения линейных задач на языке Паскаль Создание официального сайта Российской Федерации в сети «Интернет» для размещения информации о размещении заказов на поставки то
Создание официального сайта Российской Федерации в сети «Интернет» для размещения информации о размещении заказов на поставки то Проектная деятельность как одно из условий повышения мотивации обучения учащихся начальных классов.
Проектная деятельность как одно из условий повышения мотивации обучения учащихся начальных классов. «Турнир знатоков»7-еклассы
«Турнир знатоков»7-еклассы Презентация на тему "ГБУ НСО "Ценрт "Виктория"" - скачать презентации по Педагогике
Презентация на тему "ГБУ НСО "Ценрт "Виктория"" - скачать презентации по Педагогике Classification of English speech sounds
Classification of English speech sounds Письмо-обращение к родителям
Письмо-обращение к родителям Муниципальное общеобразовательное учреждение средняя общеобразовательная школа №16
Муниципальное общеобразовательное учреждение средняя общеобразовательная школа №16  Sacred and Profane Love
Sacred and Profane Love Повышение заработной платы. ГНЦ АО ЛИИ им. М.М. Громова
Повышение заработной платы. ГНЦ АО ЛИИ им. М.М. Громова Финансовые риски
Финансовые риски Современный компьютер
Современный компьютер пвш лекція 3
пвш лекція 3 Фонетические средства выразительности
Фонетические средства выразительности Mit Lufthansa nach Deutschland
Mit Lufthansa nach Deutschland