Слайд 2Цели и задачи
1. Познакомить учащихся с взглядами на строение атома, существовавших до

начала XIX века.
2. Рассказать о ядерной модели атома Резерфорда
3.Показать, чем отличаются друг от друга атомы различных химических элементов.
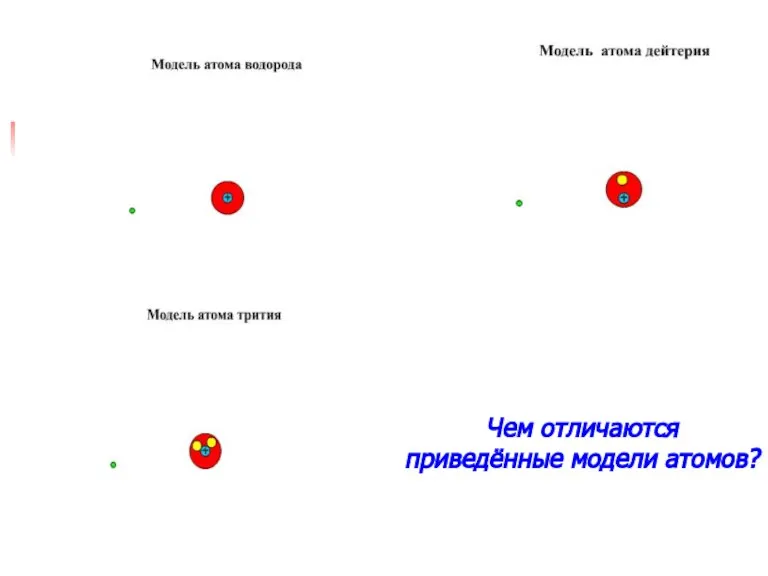
4. Показать строение атомов водорода, дейтерия, трития.
Слайд 3Взгляды учёных на строение атома
В начале XIX века в физике бытовали самые

разные и часто фантастические представления о строении атома.
Например, ректор Мюнхенского университета Фердинанд Линдеман в 1905 году утверждал, что « атом кислорода имеет форму кольца, а атом серы – форму лепёшки».
Слайд 4Модель атома по Дж. Томсону.
Дж. Томсон в 1898 году предложил

модель атома в виде положительно заряженного шара радиусом 10-10 м, в котором « плавают» отрицательные электроны, размеры которых 10-13 м. Сам Томсон относился к своим моделям без энтузиазма.
Слайд 5Русские физики
Вопрос о строении атома изучали и русские физики:
Пётр Николаевич Лебедев
И

известный учёный – народник Николай Морозов
Слайд 6Атом, атомная физика, атомный век…
Мы чуть не с пелёнок слышим со

всех сторон: атом, атомная физика, атомная энергия, атомная электростанция, атомная подводная лодка, атомный век…
Известно, что атомы – это крошечные частички, из которых состоит всё на свете: воздух, вода, земля, еда, Солнце, звёзды…
Слайд 7Опыты Резерфорда.
В 1911 году Резерфорд со своими сотрудниками провёл ряд опытов

по исследованию состава и строения атомов.
Слайд 8Строим модель атома. Как выглядит атом? Что у него внутри?
Если изобразить «детали»

из которых состоит атом, пластилиновыми шариками:
Красный – протон,
зелёный – нейтрон,
синий - электрон
Слайд 9Модель самого простого атома.
Возьмём красный шарик - протон и синий – электрон

и соединим их ниткой.
Протон – частица неповоротливая, он в две тысячи раз тяжелее электрона. Неудивительно, что протон «сидит»в центре атома, а легкий и непоседливый электрон крутится вокруг него, словно спутник вокруг Земли.
Слайд 10Модель атома самого лёгкого газа.
Самый лёгкий газ – водород. Он в 15

раз легче воздуха, поэтому наполненный водородом дирижабль всплывает в воздушном океане, словно поплавок
Слайд 11« Воздушные шарики»
Шары, которые подняли в воздух одного из героев сказки Юрия

Олеши «Три толстяка», были наполнены водородом…
Слайд 12Дейтерий
Лёгкий водород можно сделать потяжелее, если присоединить к протону нейтрон. Вот теперь

в атоме все три детали: протон, нейтрон и электрон. Это тяжёлый водород - дейтерий.
Слайд 13Тритий
Но можно сделать водород ещё тяжелее, присоединив к протону не один,

а два нейтрона – получаем сверхтяжёлый водород – тритий.
Слайд 14«Водо –род»
Водород «родит воду» он хорошо горит, а при этом атомы водорода
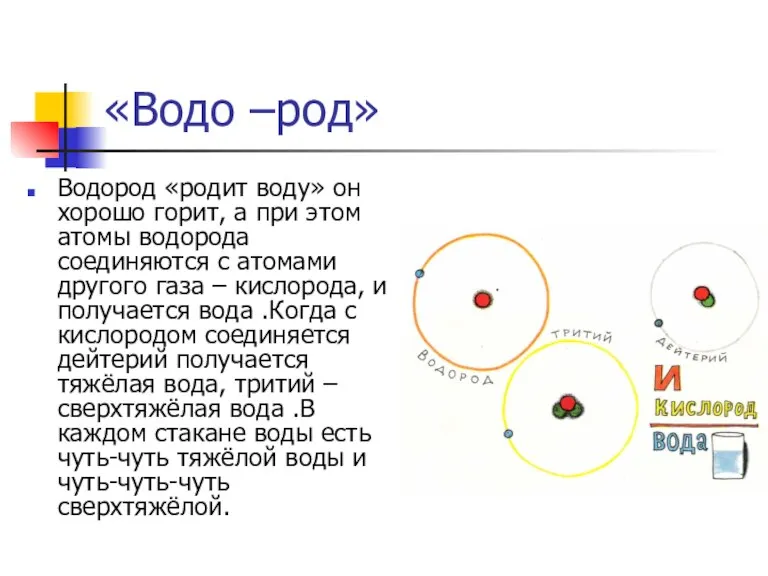
соединяются с атомами другого газа – кислорода, и получается вода .Когда с кислородом соединяется дейтерий получается тяжёлая вода, тритий – сверхтяжёлая вода .В каждом стакане воды есть чуть-чуть тяжёлой воды и чуть-чуть-чуть сверхтяжёлой.
Слайд 15Модель атома гелия
Если теперь в ядре атома будет два протона, два нейтрона,

а вокруг них будут вращаться два электрона, то получим модель атома совсем другого газа – гелия.
Слайд 17Чем отличаются приведённые модели атомов?
















 АКЦИОНЕРНОЕ ОБЩЕСТВО «АГРАРНАЯ КРЕДИТНАЯ КОРПОРАЦИЯ»
АКЦИОНЕРНОЕ ОБЩЕСТВО «АГРАРНАЯ КРЕДИТНАЯ КОРПОРАЦИЯ» Конституция
Конституция новое в 1C по ЭСФ
новое в 1C по ЭСФ Понятие материалоемкости
Понятие материалоемкости Основные типы алгоритмов. Линейные алгоритмы
Основные типы алгоритмов. Линейные алгоритмы Немытое в рот Ни за что не возьмет. И ты будь таким, Как чистюля… - презентация
Немытое в рот Ни за что не возьмет. И ты будь таким, Как чистюля… - презентация Теории мотивации
Теории мотивации Презентация на тему ТЭК России (9 класс)
Презентация на тему ТЭК России (9 класс)  آموزش سواد رسانه ای – درس سوم
آموزش سواد رسانه ای – درس سوم Представление о Power Point
Представление о Power Point Сотовый поликарбонат – актуальное предложение сезона!
Сотовый поликарбонат – актуальное предложение сезона! Схема взаимосвязей образовательных понятий
Схема взаимосвязей образовательных понятий Защита социального проектаО курении
Защита социального проектаО курении Основные направления аудита: финансовый, государственный и управленческий
Основные направления аудита: финансовый, государственный и управленческий Кризисные периоды в развитии семьи
Кризисные периоды в развитии семьи Методичні рекомендації щодо вивчення хімії у 2012-2013 році
Методичні рекомендації щодо вивчення хімії у 2012-2013 році Изучаем правила дорожного движения Активно участвуем в жизни школы ЯРМАРКА.
Изучаем правила дорожного движения Активно участвуем в жизни школы ЯРМАРКА. Интегрированный урок чтения.
Интегрированный урок чтения. Занимательная атмосфера
Занимательная атмосфера Река Воря
Река Воря Maynor_prezentatsia_1-2_chasti
Maynor_prezentatsia_1-2_chasti Famous British people
Famous British people Роберт Саути "Father William"
Роберт Саути "Father William" КАЗНЕТ СЕГОДНЯ. - презентация
КАЗНЕТ СЕГОДНЯ. - презентация Центральные
Центральные Тонкий лед
Тонкий лед Сжатие данных
Сжатие данных Словарный диктант № 13
Словарный диктант № 13