Содержание
- 2. ОФИЦИАЛЬНАЯ ПС ЭЛЕМЕНТОВ ИЮПАК (2012 г.)
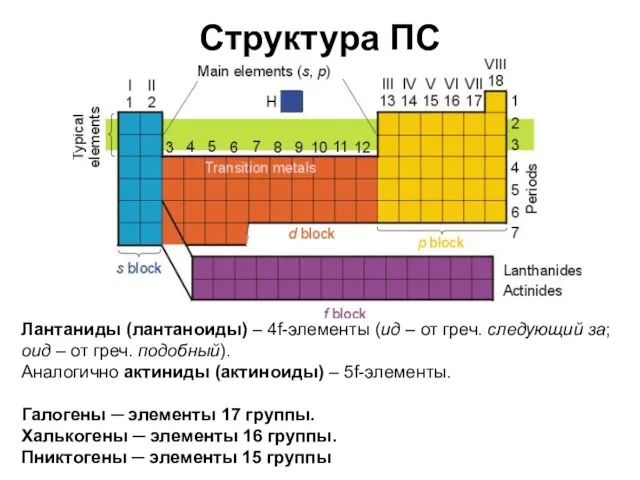
- 3. Структура ПС Лантаниды (лантаноиды) – 4f-элементы (ид – от греч. следующий за; оид – от греч.
- 4. Закономерности изменения свойств атомов и ионов Одна из основных характеристик атомов и ионов – их размеры.
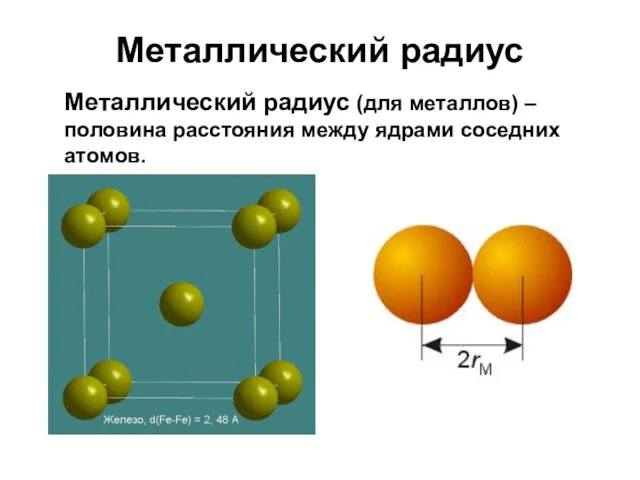
- 5. Металлический радиус Металлический радиус (для металлов) – половина расстояния между ядрами соседних атомов.
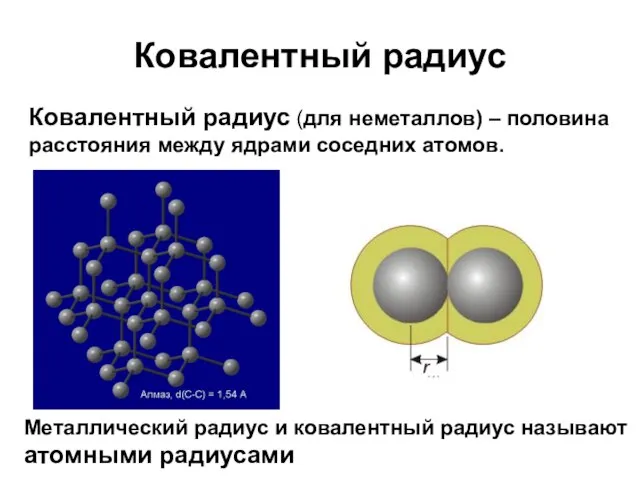
- 6. Ковалентный радиус Ковалентный радиус (для неметаллов) – половина расстояния между ядрами соседних атомов. Металлический радиус и
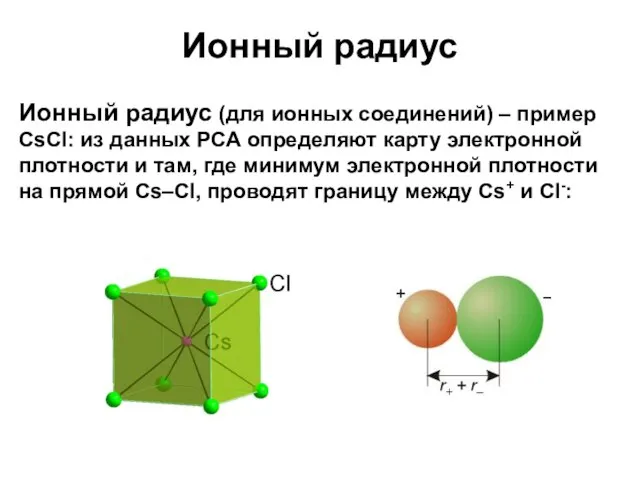
- 7. Ионный радиус Ионный радиус (для ионных соединений) – пример CsCl: из данных РСА определяют карту электронной
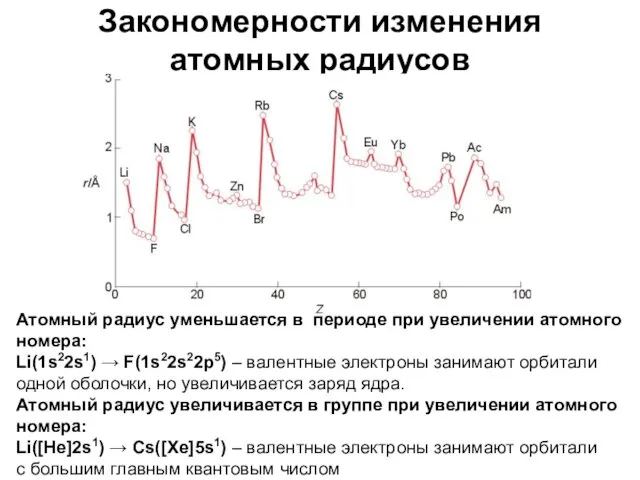
- 8. Закономерности изменения атомных радиусов Атомный радиус уменьшается в периоде при увеличении атомного номера: Li(1s22s1) → F(1s22s22p5)
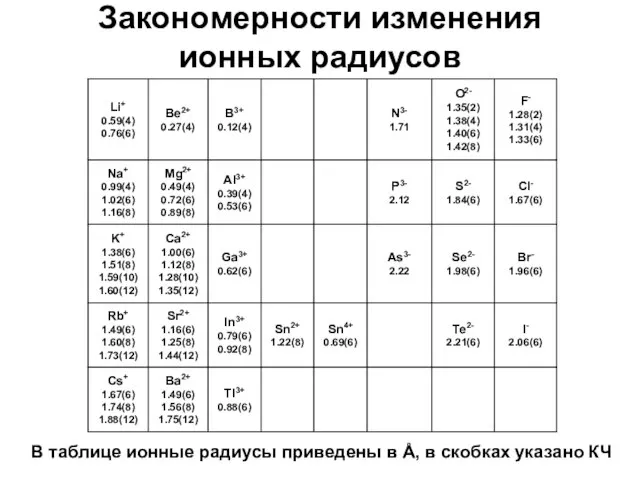
- 9. Закономерности изменения ионных радиусов В таблице ионные радиусы приведены в Å, в скобках указано КЧ
- 10. Закономерности изменения ионных радиусов Ионный радиус зависит от координационного окружения (КЧ) – чем больше КЧ, тем
- 11. Закономерности изменения ионных радиусов для переходных металлов В периоде Ti2+ (1,00 Å) → Ni2+ (0,83 Å)
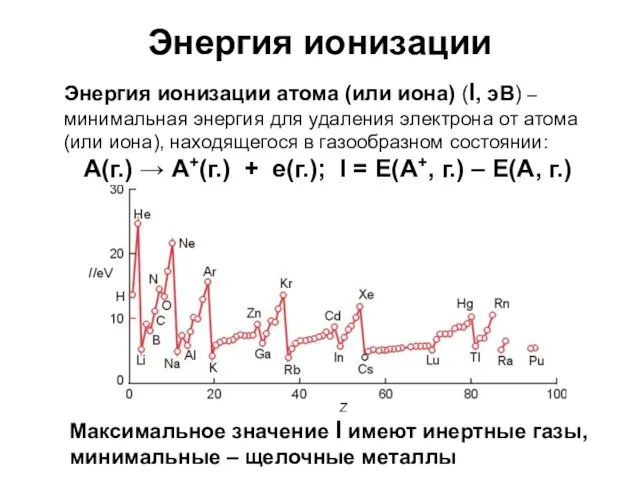
- 12. Энергия ионизации Энергия ионизации атома (или иона) (I, эВ) – минимальная энергия для удаления электрона от
- 13. Энергия ионизации Горизонтальная периодичность – в пределах одного периода значения I увеличиваются, так как увеличивается заряд
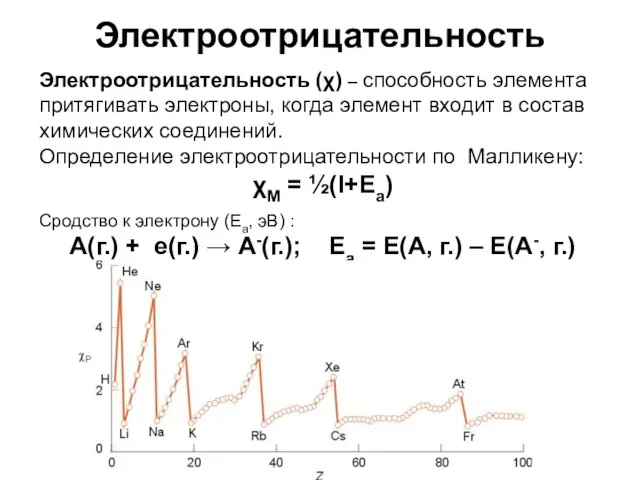
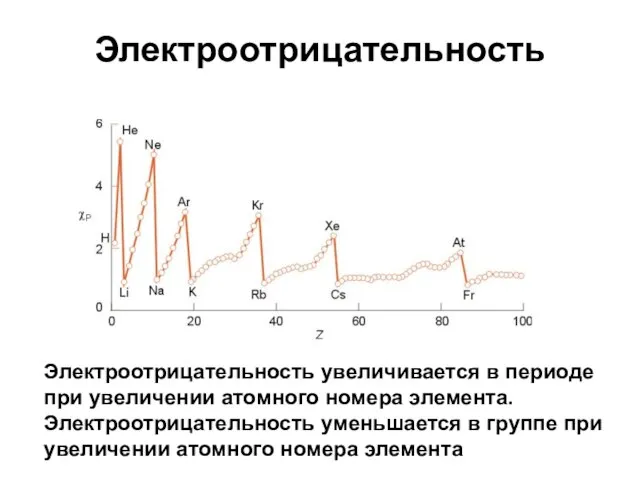
- 14. Электроотрицательность Электроотрицательность (χ) – способность элемента притягивать электроны, когда элемент входит в состав химических соединений. Определение
- 15. Электроотрицательность Электроотрицательность увеличивается в периоде при увеличении атомного номера элемента. Электроотрицательность уменьшается в группе при увеличении
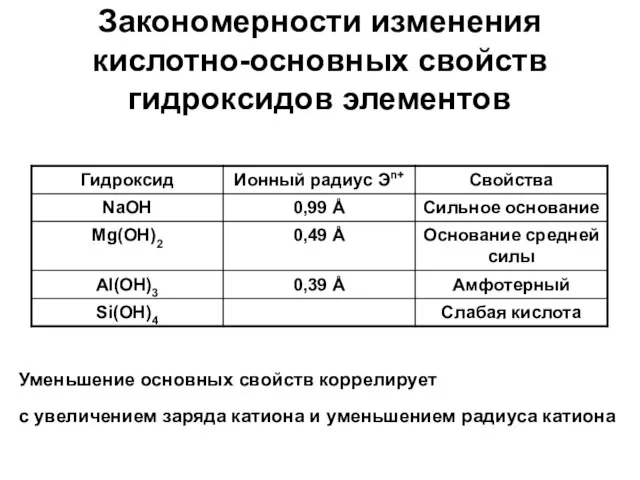
- 16. Закономерности изменения кислотно-основных свойств гидроксидов элементов Основные свойства: ЭОН → Э+ + ОН- Кислотные свойства: ЭОН
- 17. Закономерности изменения кислотно-основных свойств гидроксидов элементов Уменьшение основных свойств коррелирует с увеличением заряда катиона и уменьшением
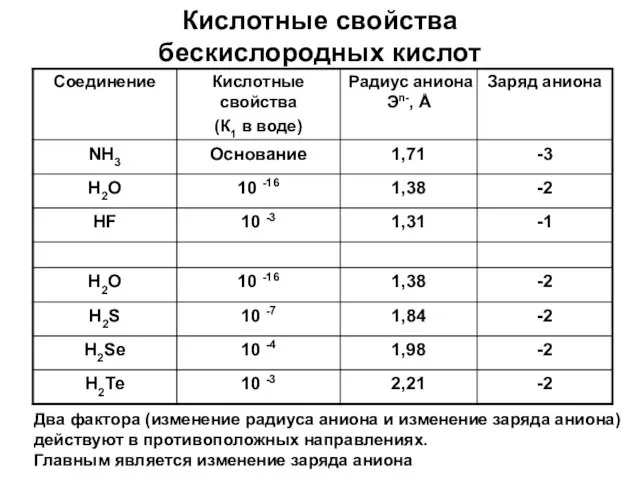
- 18. Кислотные свойства бескислородных кислот Два фактора (изменение радиуса аниона и изменение заряда аниона) действуют в противоположных
- 19. Некоторые закономерности изменения окислительно-восстановительных свойств Э + 2е + 2Н+ → Н2Э (Э – халькоген) Окислительные
- 20. Окислительно-восстановительные свойства соединений элементов в высших степенях окисления Главные элементы – s и p: 14 группа:
- 22. Скачать презентацию








 Азы перспективы
Азы перспективы Задачи на 2014-2015 учебный год (4 класс) ФГОС
Задачи на 2014-2015 учебный год (4 класс) ФГОС Диагностическая линия NTS 5xx
Диагностическая линия NTS 5xx Пассажирские перевозки и их планирование
Пассажирские перевозки и их планирование Фото-отчёт. Классный час День Конституции 9-11 классы
Фото-отчёт. Классный час День Конституции 9-11 классы Русские народные куклы ( тест )
Русские народные куклы ( тест )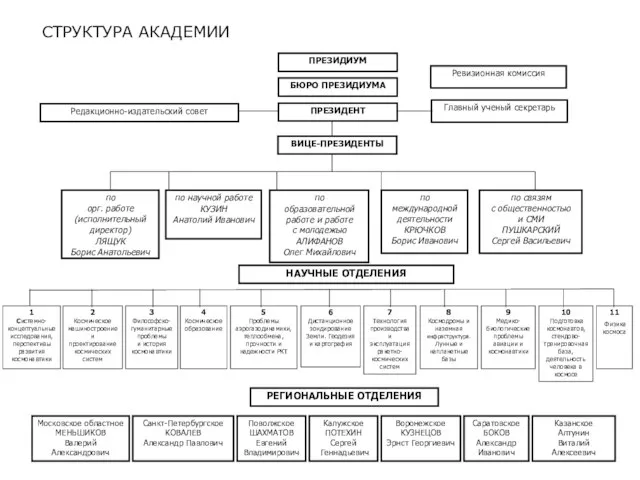 СТРУКТУРА АКАДЕМИИ
СТРУКТУРА АКАДЕМИИ Профессия моих родителей: моя мама -врач Ученица 3Б класса МАОУ «Лицей № 4» г.Перми Савельева Валерия Руководитель: Лунегова Ири
Профессия моих родителей: моя мама -врач Ученица 3Б класса МАОУ «Лицей № 4» г.Перми Савельева Валерия Руководитель: Лунегова Ири Выступление классного руководителя 10 а класса Бессмертных Елены Анатольевны по итогам адаптационного период.
Выступление классного руководителя 10 а класса Бессмертных Елены Анатольевны по итогам адаптационного период. Praktiki_gruppy_TL_44
Praktiki_gruppy_TL_44 Димакс
Димакс Золотое сечение (11 класс)
Золотое сечение (11 класс) Реформы Российской Империи
Реформы Российской Империи Презентация на тему Кайсын Кулиев
Презентация на тему Кайсын Кулиев Игра в футбол. Таблица сложения чисел с переходом через десяток. Интерактивный тренажёр.1 класс
Игра в футбол. Таблица сложения чисел с переходом через десяток. Интерактивный тренажёр.1 класс Метапредметные и личностные результаты в основной школе
Метапредметные и личностные результаты в основной школе С Е М Ь Ч У Д Е С С В Е Т А
С Е М Ь Ч У Д Е С С В Е Т А Деструктивные организации
Деструктивные организации Soonest пункт выдачи заказов
Soonest пункт выдачи заказов В мире профессий (8 класс)
В мире профессий (8 класс) Получение белка в биотехнологическом производстве
Получение белка в биотехнологическом производстве  Знакомство с Латинской Америкой
Знакомство с Латинской Америкой Welcome in the city of the Astrakhan
Welcome in the city of the Astrakhan Свои среди чужих
Свои среди чужих Своя игра русский язык
Своя игра русский язык Нахождение наибольшего и наименьшего значения функции
Нахождение наибольшего и наименьшего значения функции Куница
Куница Презентация на тему основные понятия и определения управления в таможенных органах
Презентация на тему основные понятия и определения управления в таможенных органах