Содержание
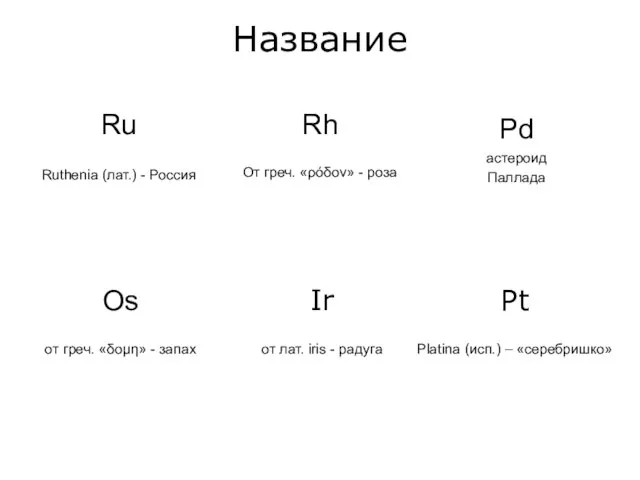
- 3. Название Ru Ruthenia (лат.) - Россия Rh От греч. «ρóδoν» - роза Os от греч. «δoμη»
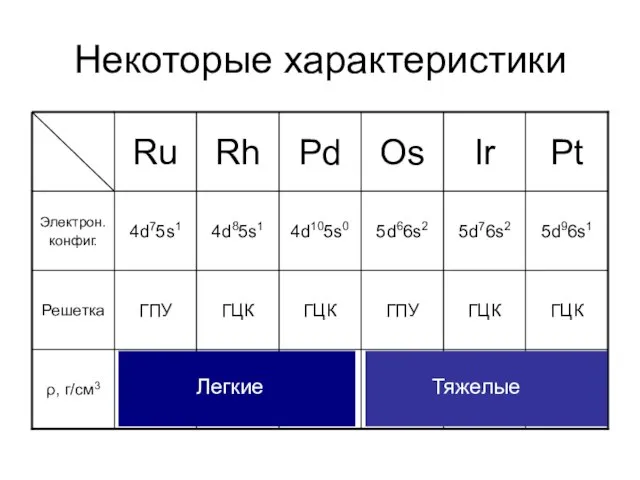
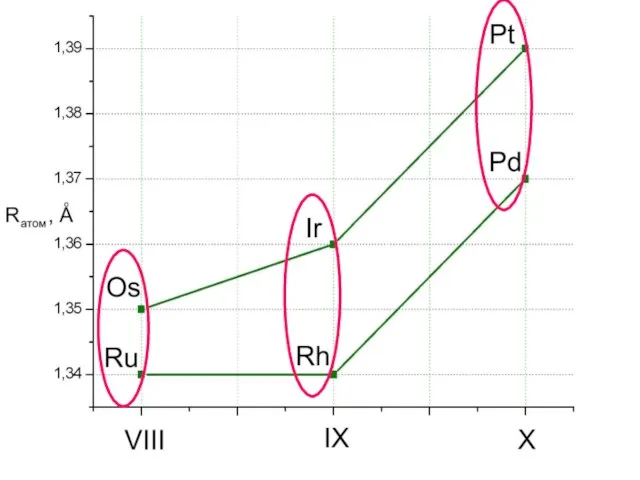
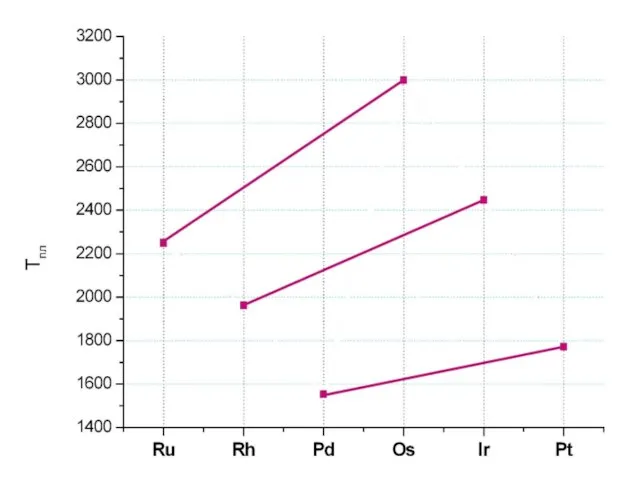
- 4. Некоторые характеристики Легкие Тяжелые
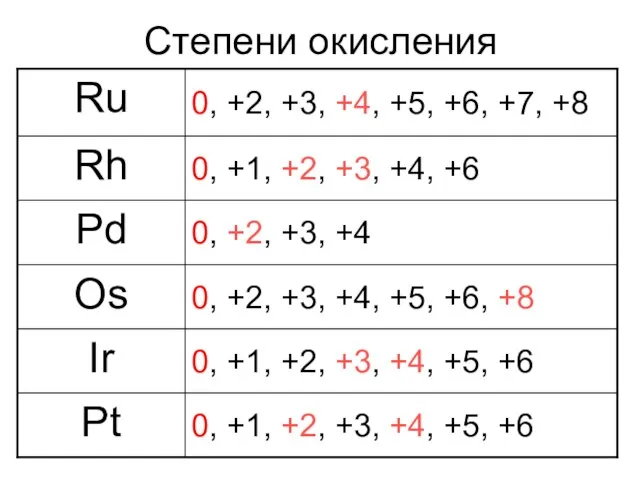
- 5. Степени окисления
- 8. Распространенность в земной коре, в %
- 9. Основные минералы Поликсен (Pt, Fe): Pt 80 — 88% Ферроплатина: Pt 84 — 81% Палладистая платина:
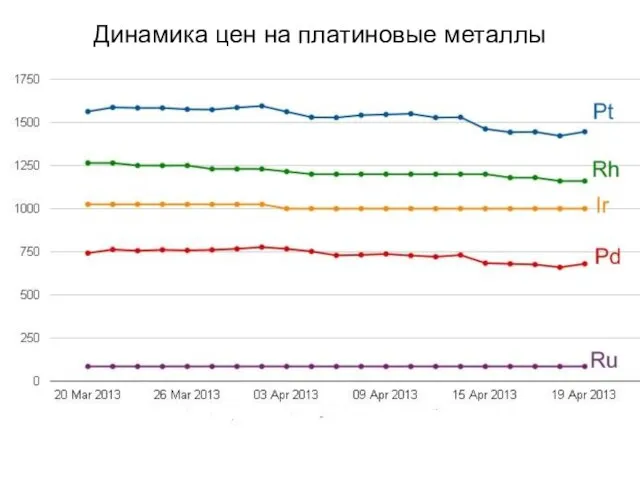
- 10. Динамика цен на платиновые металлы
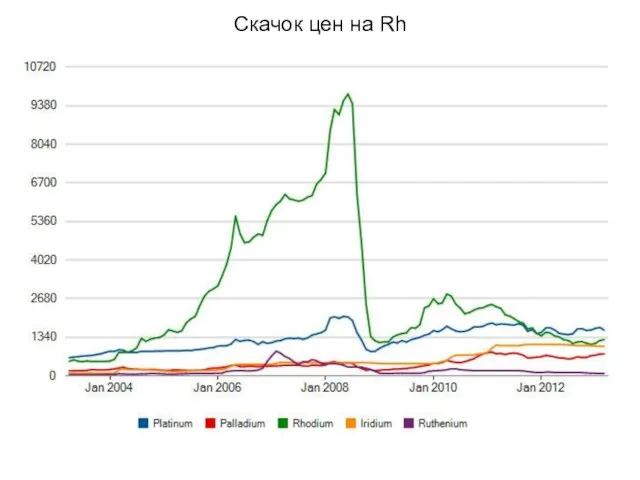
- 11. Скачок цен на Rh
- 12. Получение аффинаж Смесь + «царская водка» = H2[ЭСl6], Os,Ir не растворяются 3Pt + 4HNO3 + 18HCl
- 13. Химические свойства простых веществ Взаимодействие с кислотами-окислителями: Pd + 2H2SO4 = PdSO4 + SO2 + 2H2O
- 14. Химические свойства простых веществ Окисление, сопровождающееся комплексообразованием: 3Pt(Pd) + 4HNO3 + 18HCl = 3H2[PtCl6] + 4NO
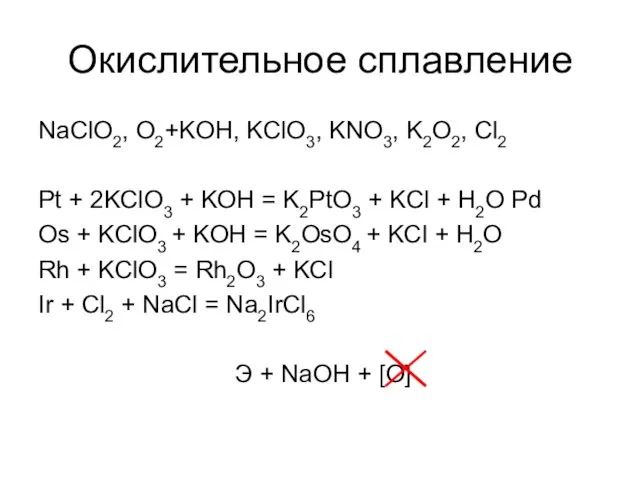
- 15. Окислительное сплавление NaClO2, O2+KOH, KClO3, KNO3, K2O2, Cl2 Pt + 2KClO3 + KOH = K2PtO3 +
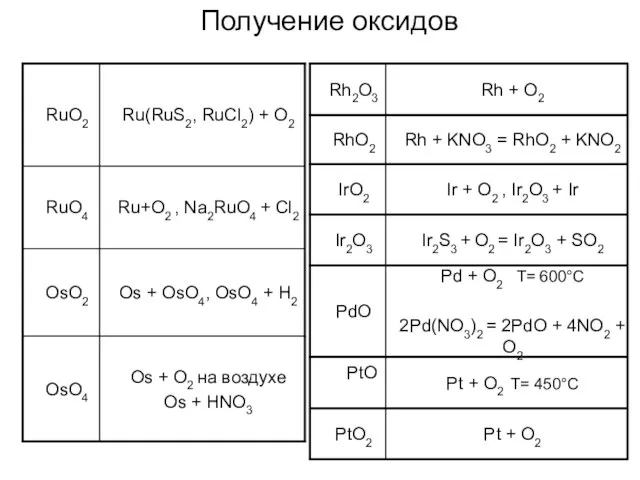
- 16. Получение оксидов
- 17. Поведение оксидов при нагревании
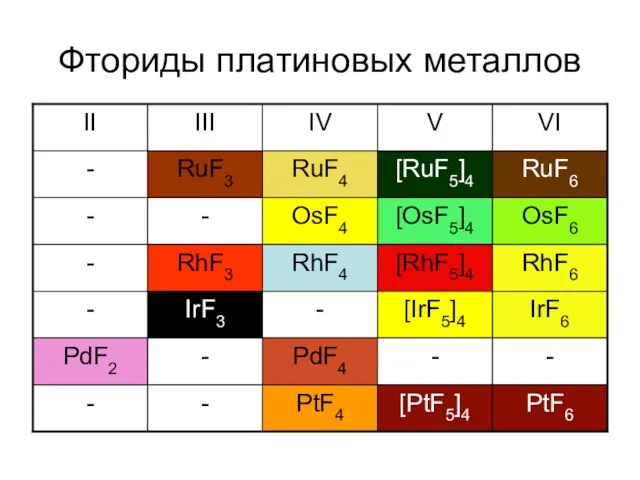
- 18. Фториды платиновых металлов
- 19. Фториды платиновых металлов Сильные окислители PtF6 самый сильный окислитель: O2 + PtF6 = O2+[PtF]6- Xe +
- 20. Ru, Os (+8) Слабые кислотные свойства: OsO4 + H2O = H2[OsO4(OH)2] K1= 10-12 OsO4+ KOH =
- 21. Ru, Os (+8) OsO4 , RuO4 OsO4 + HCl(конц.) = H2[OsCl6]+Cl2+H2O OsO4 + HCl(разб.) = RuO4
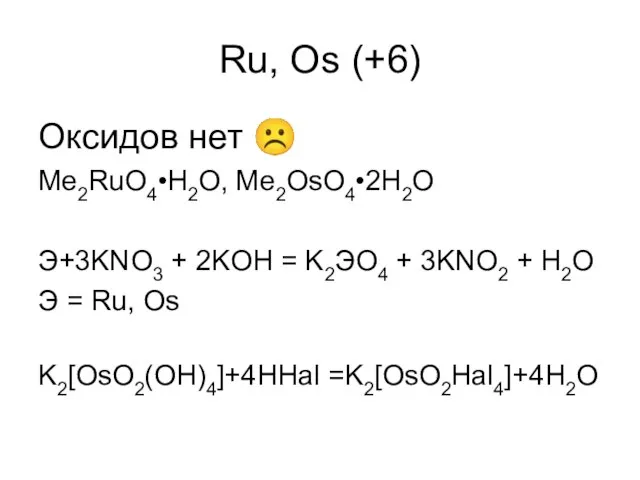
- 22. Ru, Os (+6) Оксидов нет ☹ Me2RuO4•H2O, Me2OsO4•2H2O Э+3KNO3 + 2KOH = K2ЭO4 + 3KNO2 +
- 23. Ru, Os (+6) Ru+6 окислители: 2K2RuO4+ 12HCl = 2K2[RuCl6] + Cl2 + 6H2O K2RuO4+ H2SO4 =
- 24. Ru, Os (+4) RuO2, OsO2 Кислотно-основные свойства: ЭO2 + 6HCl = H2[ЭCl6] + 2H2O ЭF4 +
- 25. Rh, Ir (+4) Получение: Ir + Na2CO3 + 2NaNO3 = Na2IrO3 + 2NaNO2 + CO2 K2IrF6
- 26. Rh, Ir (+4) IrO2 Прочная кристал. решетка низкая хим. активность RhO2 не устойчив Обменные реакции Характерны
- 27. Rh, Ir (+4) Rh+4 сильные окислители Cs2[RhCl6] = RhCl3 + CsCl + Cl2 2RhO2 + 8HCl
- 28. Rh, Ir (+3) Кислотно - основные свойства: Rh2O3 + 6HCl = H3[RhCl6] + 3H2O Ir2O3 +
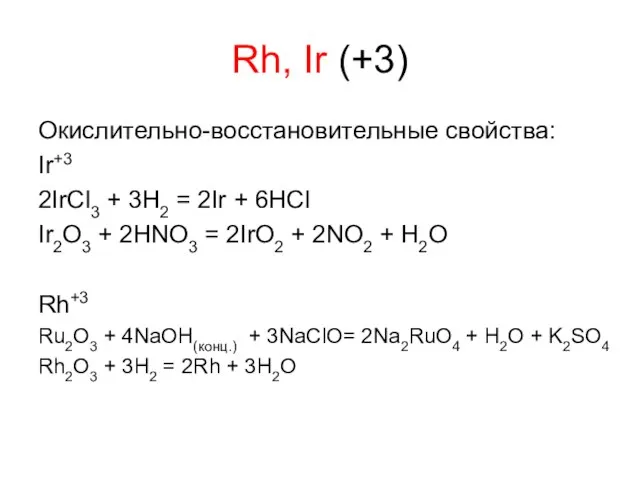
- 29. Rh, Ir (+3) Окислительно-восстановительные свойства: Ir+3 2IrCl3 + 3H2 = 2Ir + 6HCl Ir2O3 + 2HNO3
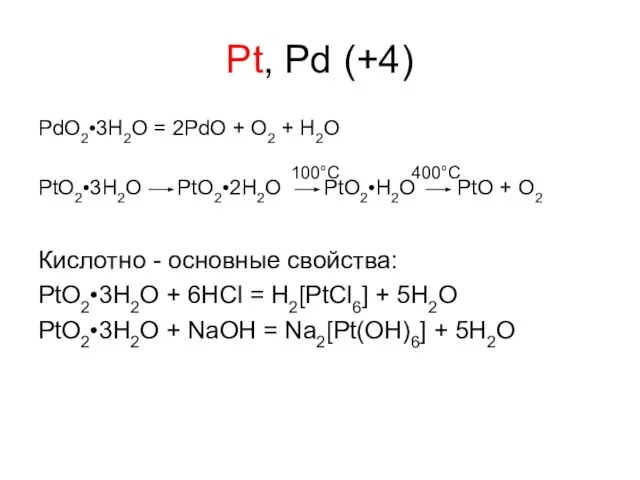
- 30. Pt, Pd (+4) PdO2•3H2O = 2PdO + O2 + H2O PtO2•3H2O PtO2•2H2O PtO2•H2O PtO + O2
- 31. H2[PtCl6] Гексахлороплатинат(IV) водорода Гексахлорплатиновая кислота Устойчивая, сильная Получение: Pt(OH)4 + HCl = H2[PtCl6] + H2O PtCl4
- 32. H2[Pt(OH)6] Гексагидроксоплатинат (IV) водорода Гексагидроксоплатиновая кислота Слабая, малорастворимая Получение: K2[Pt(OH)6] + HCl = H2[Pt(OH)6] + KCl
- 33. Pt, Pd (+4) Окислительно-восстановительные свойства Pd+4 сильный окислитель Pd(OH)4 = Pd(OH)2 + O2 + 2H2O Ткомн.
- 34. Pt, Pd (+2) Pd+2 в воде [Pd(H2O)6]2+ Pd(ClO4), PdSO4 Кислотно-основные свойства: PtO амфотерен PtO + HCl
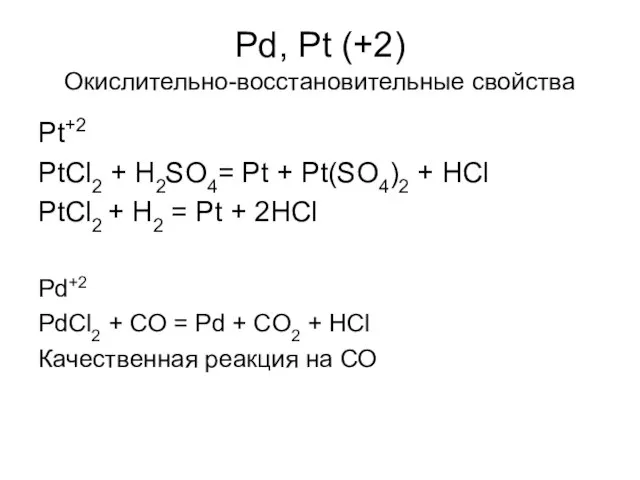
- 35. Pd, Pt (+2) Окислительно-восстановительные свойства Pt+2 PtCl2 + H2SO4= Pt + Pt(SO4)2 + HCl PtCl2 +
- 36. Применение Pd: Kat реакций гидрирования Pt: Kat Посуда Термопары Электроды Ювелирное и зубопротезное Rh, Os Добавки
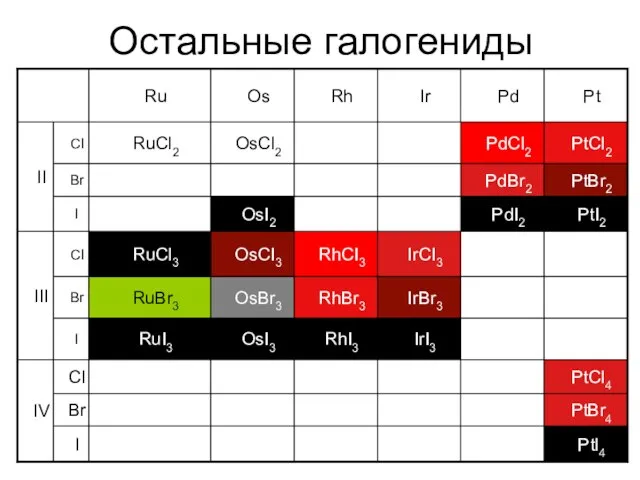
- 37. Остальные галогениды
- 38. Сульфиды, фосфиды и т.д. Ru2P – Co2P RhP3 – CoP3 RuP – FeP и CoP PdP3
- 39. Принципы разделения Os и Ru не растворяются ни в одной из кислот вплоть до Ткип, тогда
- 41. Скачать презентацию


![Получение аффинаж Смесь + «царская водка» = H2[ЭСl6], Os,Ir не растворяются 3Pt](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/378163/slide-11.jpg)




![Ru, Os (+8) Слабые кислотные свойства: OsO4 + H2O = H2[OsO4(OH)2] K1=](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/378163/slide-19.jpg)
![Ru, Os (+8) OsO4 , RuO4 OsO4 + HCl(конц.) = H2[OsCl6]+Cl2+H2O OsO4](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/378163/slide-20.jpg)
![Ru, Os (+6) Ru+6 окислители: 2K2RuO4+ 12HCl = 2K2[RuCl6] + Cl2 +](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/378163/slide-22.jpg)
![Ru, Os (+4) RuO2, OsO2 Кислотно-основные свойства: ЭO2 + 6HCl = H2[ЭCl6]](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/378163/slide-23.jpg)


![Rh, Ir (+4) Rh+4 сильные окислители Cs2[RhCl6] = RhCl3 + CsCl +](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/378163/slide-26.jpg)
![Rh, Ir (+3) Кислотно - основные свойства: Rh2O3 + 6HCl = H3[RhCl6]](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/378163/slide-27.jpg)
![H2[PtCl6] Гексахлороплатинат(IV) водорода Гексахлорплатиновая кислота Устойчивая, сильная Получение: Pt(OH)4 + HCl =](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/378163/slide-30.jpg)
![H2[Pt(OH)6] Гексагидроксоплатинат (IV) водорода Гексагидроксоплатиновая кислота Слабая, малорастворимая Получение: K2[Pt(OH)6] + HCl](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/378163/slide-31.jpg)

![Pt, Pd (+2) Pd+2 в воде [Pd(H2O)6]2+ Pd(ClO4), PdSO4 Кислотно-основные свойства: PtO](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/378163/slide-33.jpg)



 Школьное самоуправление: «Игра в демократию» или участие в школьной политике?
Школьное самоуправление: «Игра в демократию» или участие в школьной политике? Жизнь в моём городе в прошлых веках. Историческая тема в бытовом жанре. 7 класс
Жизнь в моём городе в прошлых веках. Историческая тема в бытовом жанре. 7 класс Ремонтно-реставрационные работы с приспособлением здания ГБУК г. Москвы МДТ им. А.С. Пушкина
Ремонтно-реставрационные работы с приспособлением здания ГБУК г. Москвы МДТ им. А.С. Пушкина Руководство преподавателя
Руководство преподавателя Архитектура страны фараонов (Египетские пирамиды)
Архитектура страны фараонов (Египетские пирамиды) Технология организации групповой работы в начальной школе
Технология организации групповой работы в начальной школе  Материалы и инструменты
Материалы и инструменты Манипуляция
Манипуляция Темы для докладов
Темы для докладов Leisure Activities
Leisure Activities Структура нормативных правовых актов РФ в области защиты информации
Структура нормативных правовых актов РФ в области защиты информации Достояние России. Занятие 35
Достояние России. Занятие 35 Marketing research
Marketing research Сленговая речь стала повседневной, но правильно ли это?
Сленговая речь стала повседневной, но правильно ли это? SEO или продвижение сайта в поисковых системах.
SEO или продвижение сайта в поисковых системах. Презентация на тему Зимний дворец
Презентация на тему Зимний дворец Reading Gum. Fed
Reading Gum. Fed Презентация на тему 20 век Век космонавтики
Презентация на тему 20 век Век космонавтики Красота и целесообразность. Вещь как сочетание объёмов и образ времени
Красота и целесообразность. Вещь как сочетание объёмов и образ времени Презентация на тему Александро-Невская Лавра
Презентация на тему Александро-Невская Лавра Rytsarskaya_kultura_v_Evrope (1)
Rytsarskaya_kultura_v_Evrope (1) Презентация СТК дистант
Презентация СТК дистант Презентация детского сада №108 Московского района
Презентация детского сада №108 Московского района Финансовый отчет за 2011 год
Финансовый отчет за 2011 год Служебные части речи. Предлог
Служебные части речи. Предлог Проверочная работа 11 апреля 2009 года Колесник Н.В. Московская финансово-промышленная академия Курс «Межцивилизационные коммуникации» 16 мая2009 ©
Проверочная работа 11 апреля 2009 года Колесник Н.В. Московская финансово-промышленная академия Курс «Межцивилизационные коммуникации» 16 мая2009 © Сергей Михайлович Эйзенштейн
Сергей Михайлович Эйзенштейн Презентация на тему Конвенция о правах ребенка и реалии детства в современной России
Презентация на тему Конвенция о правах ребенка и реалии детства в современной России