Содержание
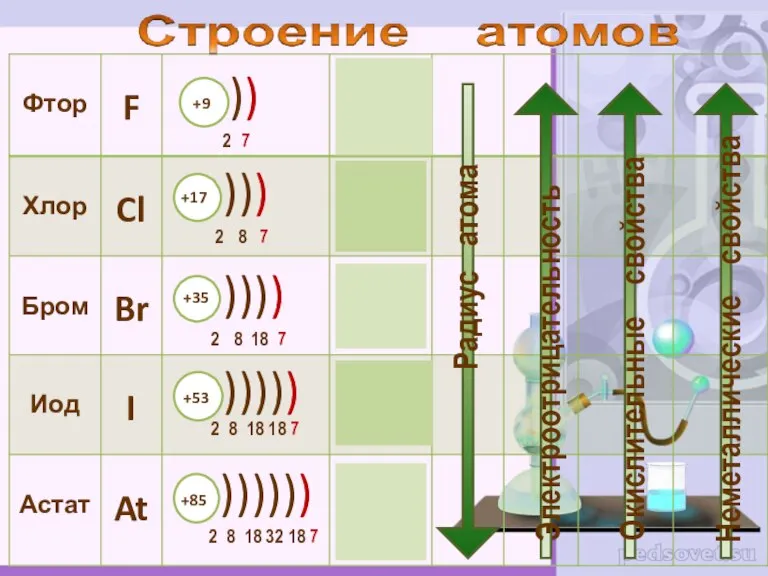
- 2. К элементам VII группы, главной подгруппы относятся фтор F, хлор Cl, бром Br, иод I, астат
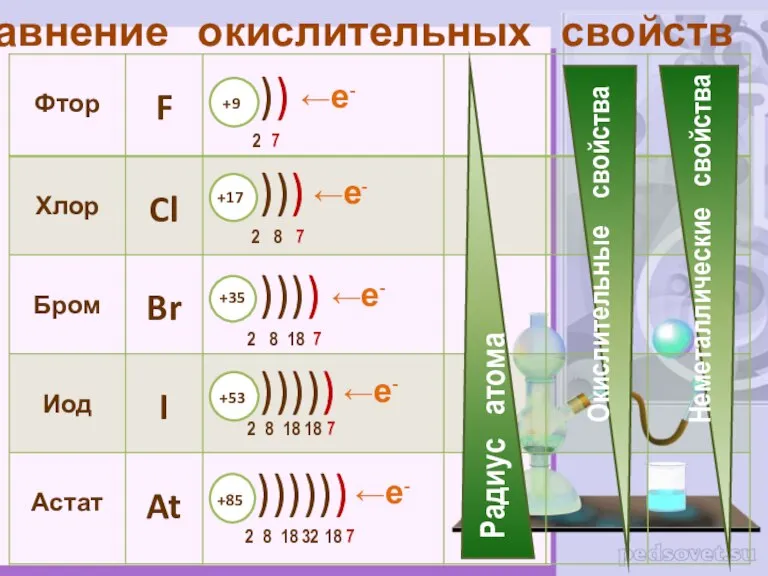
- 4. Сравнение окислительных свойств ←е- ←е- ←е- ←е- ←е-
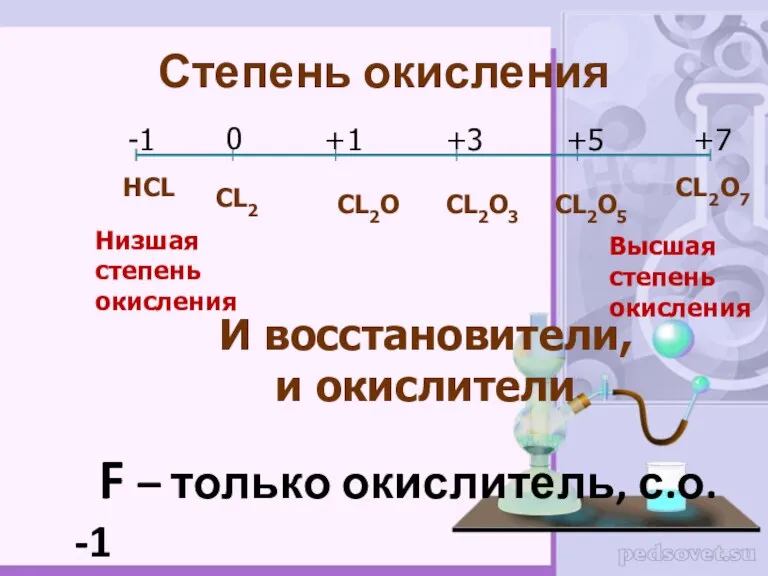
- 5. Степень окисления НCL CL2O7 F – только окислитель, с.о. -1 -1 0 +1 +3 +5 +7
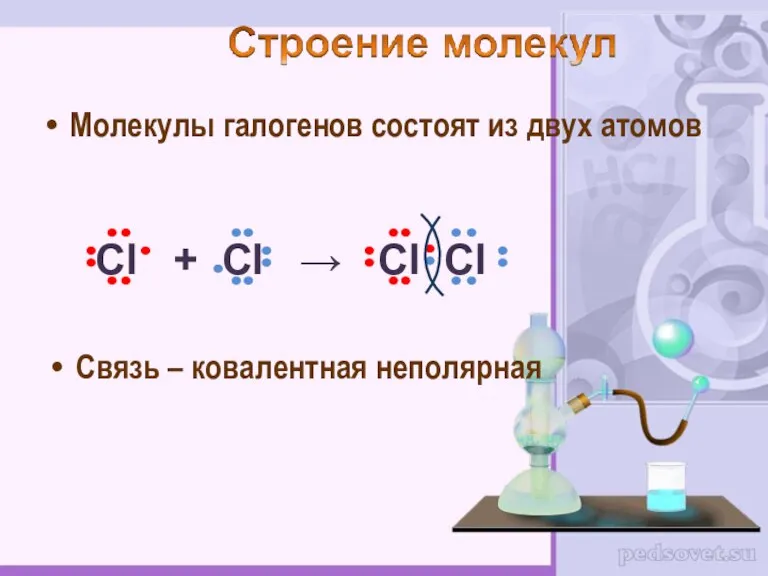
- 6. Молекулы галогенов состоят из двух атомов Связь – ковалентная неполярная
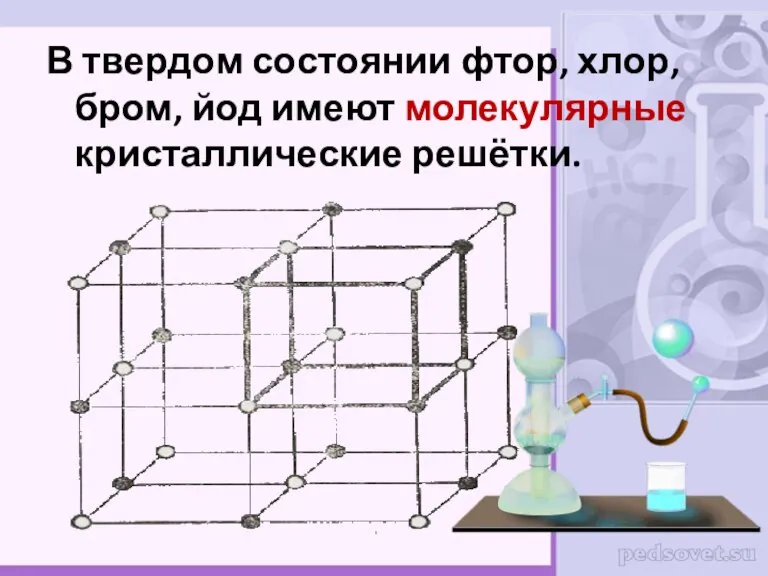
- 7. В твердом состоянии фтор, хлор, бром, йод имеют молекулярные кристаллические решётки.
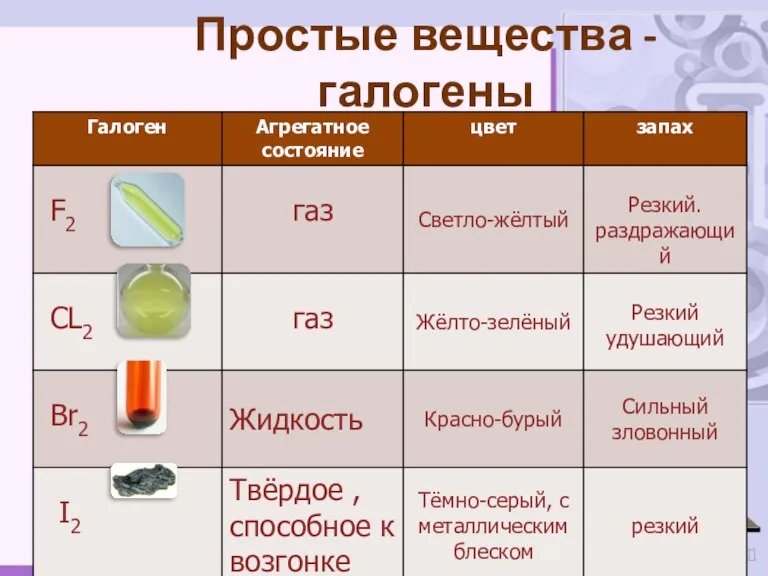
- 8. Простые вещества - галогены
- 9. 1. Взаимодействие с металлами Хлор непосредственно реагирует почти со всеми металлами (с некоторыми только в присутствии
- 10. H2 + F2 = 2HF (со взрывом) H2 + Cl2 = 2HCl (на свету) H2 +
- 11. 3. Взаимодействие с водой с образованием смеси кислот 4. Взаимодействие с солями других галогенов более активные
- 12. Историческая справка Слово «галогены» (“halogen”) ввел шведский химик Й.Я.Берцелиус галогены (греч. hals – соль, gen –
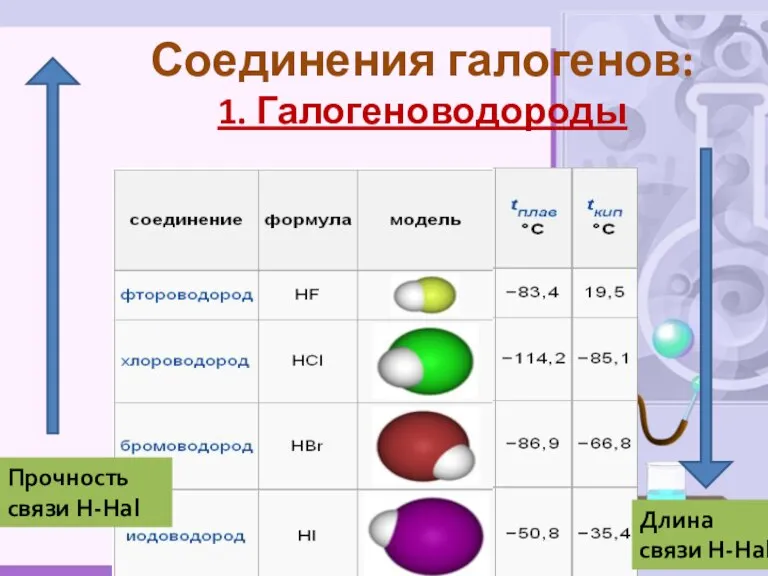
- 13. Соединения галогенов: 1. Галогеноводороды Длина связи Н-Hal Прочность связи Н-Hal
- 14. Бесцветные газы (HF при t С резким запахом Токсичны Хорошо растворяются в воде Дымят во влажном
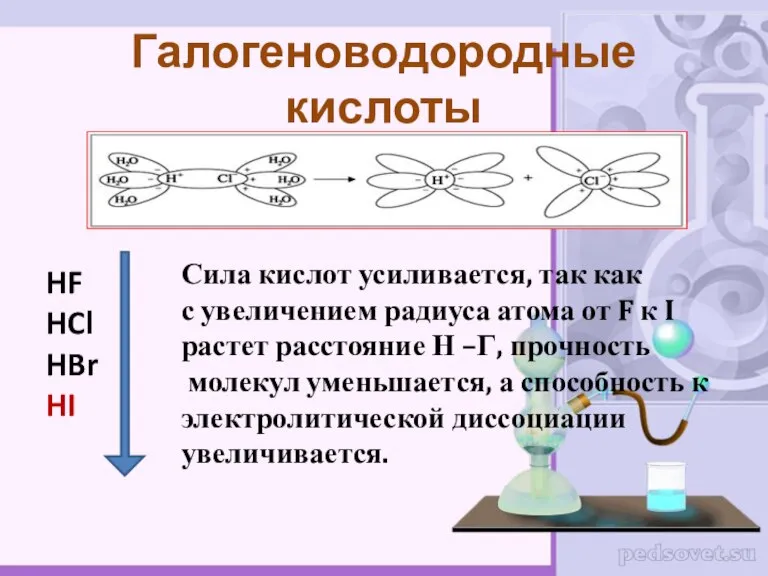
- 15. HF HCl HBr HI Галогеноводородные кислоты Сила кислот усиливается, так как с увеличением радиуса атома от
- 16. В промышленности: синтезом из водорода и хлора: H2 + Cl2 = 2HCl 2) В лаборатории: NaCl
- 17. Физические свойства: бесцветная, дымящая на воздухе жидкость, тяжелее воды Химические свойства: Типичная кислота Соляная кислота С
- 18. Используют для изготовления надписей и рисунков на стекле. SiO2 + 2HF = SiF4↑ + 2H2O Плавиковая
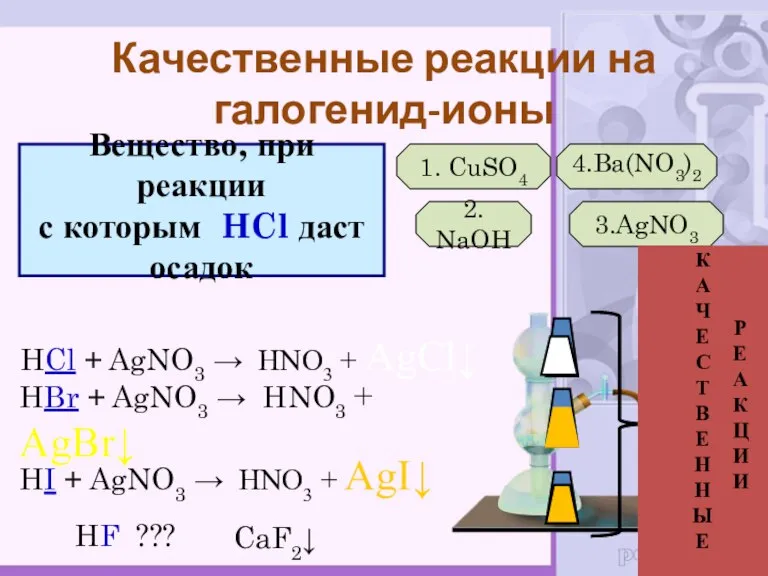
- 19. Вещество, при реакции с которым HCl даст осадок 1. CuSO4 2. NaOH 3.AgNO3 4.Ba(NO3)2 HCl +
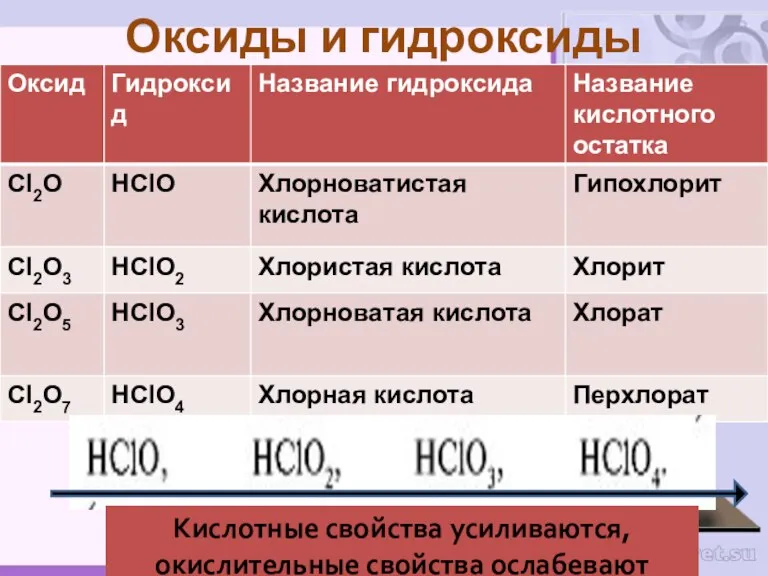
- 20. Оксиды и гидроксиды Кислотные свойства усиливаются, окислительные свойства ослабевают
- 21. Распространенность в природе галит NaCl сильвин KCl сильвинит KCl•NaCl Плавиковый шпат - флюорит CaF2
- 22. Получение галогенов: F2 и Cl2 в промышленности получают электролизом расплавов или растворов их солей: 2NaCl 2Na
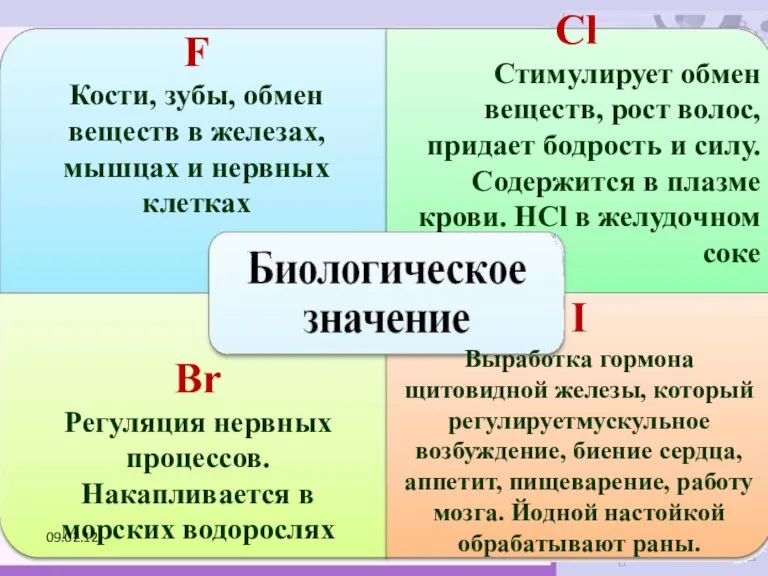
- 23. F Кости, зубы, обмен веществ в железах, мышцах и нервных клетках Сl Стимулирует обмен веществ, рост
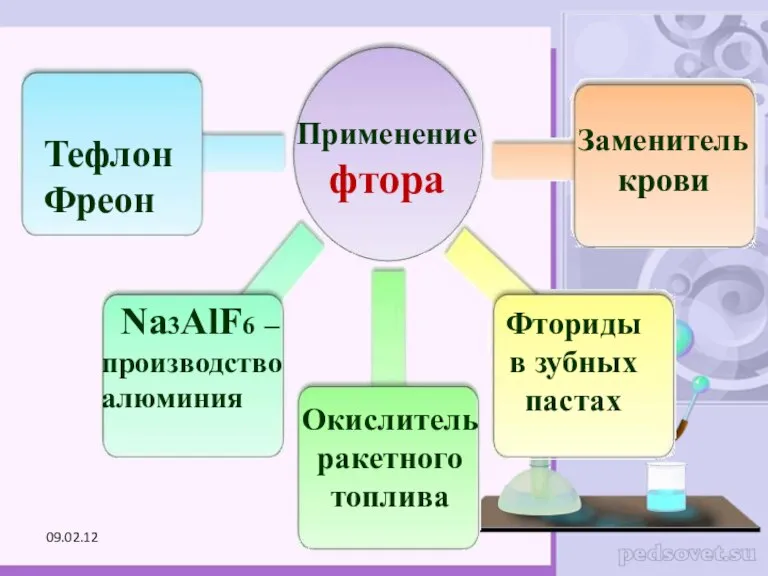
- 24. Применение фтора Тефлон Фреон Na3AlF6 – производство алюминия Окислитель ракетного топлива Заменитель крови Фториды в зубных
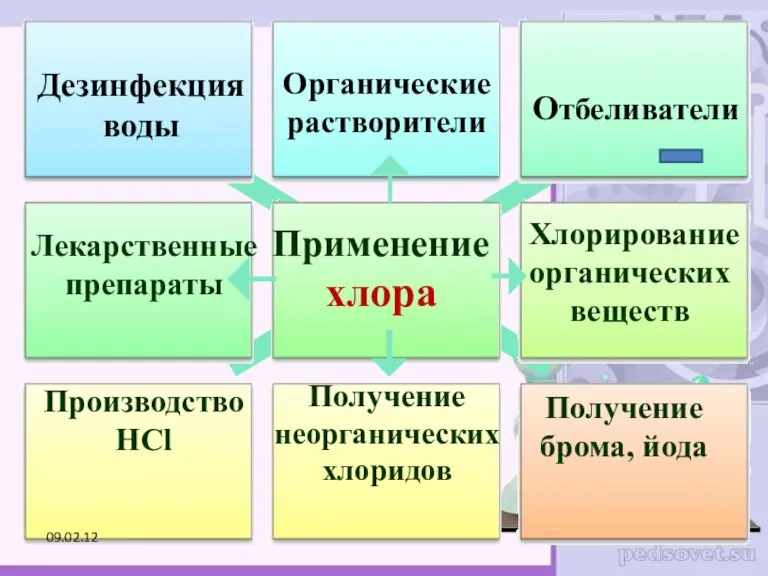
- 25. Применение хлора Отбеливатели Производство HCl Получение брома, йода Дезинфекция воды Органические растворители Лекарственные препараты Хлорирование органических
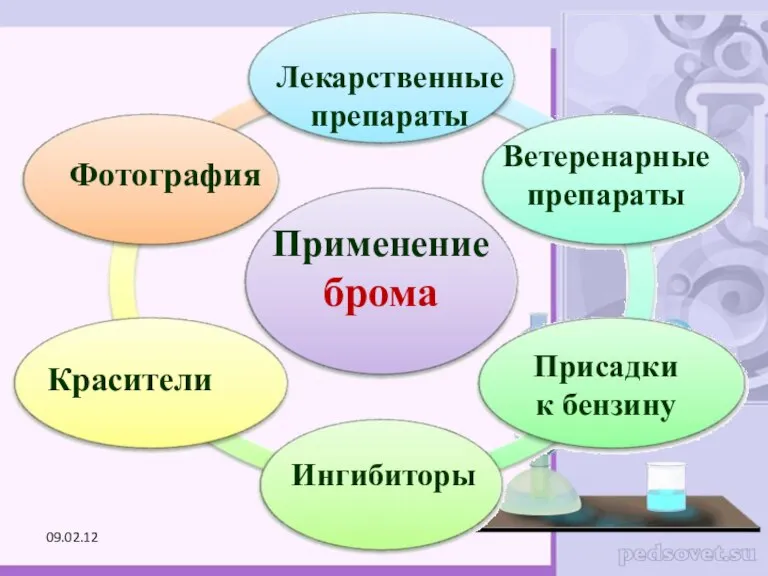
- 26. Применение брома Лекарственные препараты Красители Фотография Ветеренарные препараты Ингибиторы Присадки к бензину 09.02.12
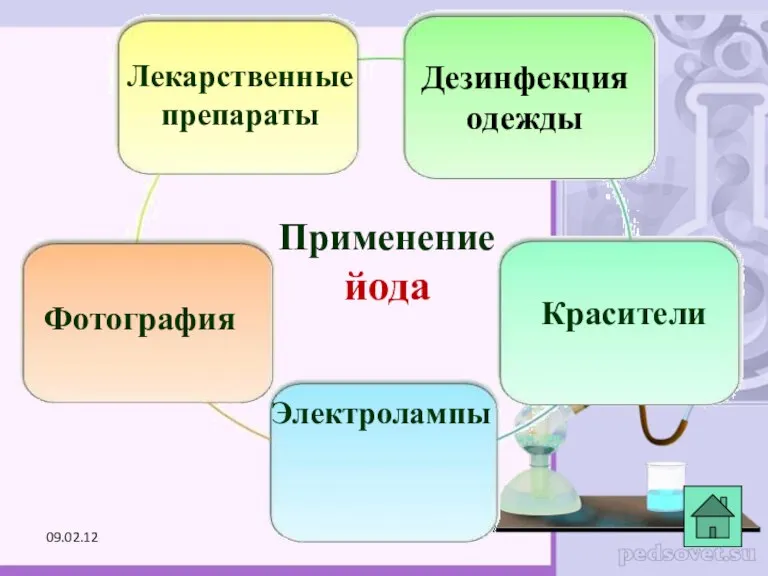
- 27. Применение йода Лекарственные препараты Фотография Красители Дезинфекция одежды Электролампы 09.02.12
- 28. Домашнее задание: П.19, №3-4 П.20, №1-3
- 30. Скачать презентацию












 Операционная система персонального компьютера
Операционная система персонального компьютера Католицизм: кнут и пряник
Католицизм: кнут и пряник Презентация на тему тренажер по английскому языку
Презентация на тему тренажер по английскому языку Публичный докладдиректора школы МОУ “СОШ № 10” Н.А. Давыдовой г.Биробиджан, ЕАО
Публичный докладдиректора школы МОУ “СОШ № 10” Н.А. Давыдовой г.Биробиджан, ЕАО Декларации пожарной безопасности
Декларации пожарной безопасности  Презентация на тему: Бородинская панорама
Презентация на тему: Бородинская панорама Заседание Совета кураторов
Заседание Совета кураторов Нутромер оборудование для измерения диаметра внутренних полостей
Нутромер оборудование для измерения диаметра внутренних полостей Music
Music Устройство увеличительных приборов. Строение клетки
Устройство увеличительных приборов. Строение клетки Реклама новых книг
Реклама новых книг Роль точечных мутаций гена RUNX1 в патогенезе миелодиспластических и миелопролиферативных заболеваний у детей
Роль точечных мутаций гена RUNX1 в патогенезе миелодиспластических и миелопролиферативных заболеваний у детей FLEXWORK project materials and their use in TELESOL
FLEXWORK project materials and their use in TELESOL Презентация на тему ПРИНЦИП ГЮЙГЕНСА. ЗАКОН ОТРАЖЕНИЯ СВЕТА
Презентация на тему ПРИНЦИП ГЮЙГЕНСА. ЗАКОН ОТРАЖЕНИЯ СВЕТА Выдающаяся личность
Выдающаяся личность урок
урок Презентация услуг компании «ГЛОБАЛ КОНСАЛТИНГ»
Презентация услуг компании «ГЛОБАЛ КОНСАЛТИНГ» Храм Святой Софии в Константинополе
Храм Святой Софии в Константинополе Сечение ударной электронной ионизации. Оже-электроны
Сечение ударной электронной ионизации. Оже-электроны Россия на политической карте мира. Особенности развития на современном этапе
Россия на политической карте мира. Особенности развития на современном этапе Животные и растения Северной Америки
Животные и растения Северной Америки Иконки автомобильные
Иконки автомобильные The dark matter power complex
The dark matter power complex Система академика Л.Занкова
Система академика Л.Занкова “Практика внедрения международного стандарта ISО 14001 в ОАО “Концерн Стирол”
“Практика внедрения международного стандарта ISО 14001 в ОАО “Концерн Стирол” АООП НОО для обучающихся с НОДА
АООП НОО для обучающихся с НОДА Лига Индиго. Интеллектуально-развлекательная игра. Разрыв шаблона о корпоративных праздниках
Лига Индиго. Интеллектуально-развлекательная игра. Разрыв шаблона о корпоративных праздниках Компания МИКРОБОР НАНОТЕХ
Компания МИКРОБОР НАНОТЕХ