Слайд 3Діаграма станів сплаву
це графічне відображення залежності температур фазових перетворень у сплавах

від їх складу, а також рівноважного та не рівноважного стану цих сплавів
Слайд 4Рівноважний стан
відповідає мінімальному значенню енергії Гіббса
він досягається тільки при малих швидкостях

охолодження та тривалому нагріванні
Слайд 5Не рівноважний стан
( метастабільний )
обумовлює обмежену стійкість сплавів і під впливом зовнішніх

факторів вони переходять у більш стабільний стан
забезпечує сплавам високі механічні та інші властивості
притаманний переважній більшості сплавів
Слайд 6Діаграма станів сплаву
для 2-х компонентних металевих сплавів будують діаграми в координатах температура

- концентрація (вісь абсцис – концентрація; вісь ординат –температура)
крайні ординати відповідають чистим 100% компонентам
загальний вміст компонентів у будь-якій точці дорівнює 100%
кожна точка на діаграмі вказує концентрацію сплаву при певній температурі.
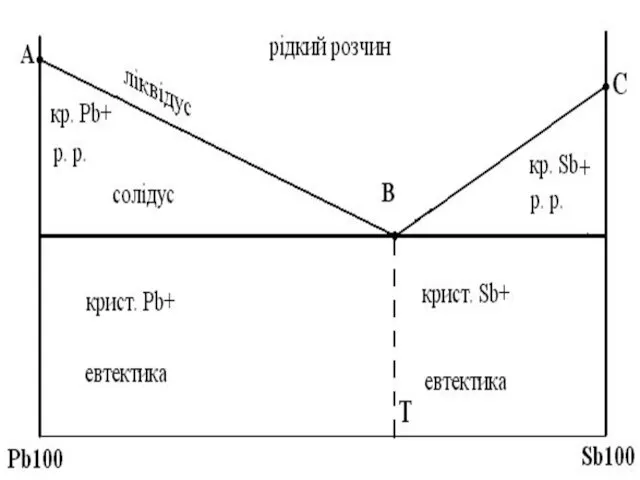
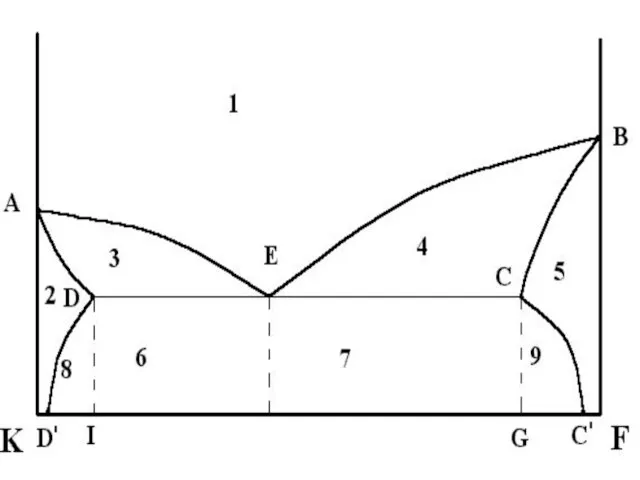
Слайд 8ЕВТЕКТИКА
в перекладі з грецької “легко плавиться”
механічна суміш двох або більше видів

кристалів, що одночасно кристалізуються із рідини
чисті метали та евтектичний сплав мають по одній критичній точці (A для Pb; C для Sb; B для евтектики)
сплави мають по дві критичні точки, які лежать на лініях початку та кінця кристалізації
Слайд 9Діаграма станів сплаву
ліквідус - лінія початку кристалізації
солідус - лінія кінця кристалізації

сплав у точці евтектики (В) називають евтектичним
сплав до точки евтектики (В) називають до евтектичним
після точки евтектики (В) – заевтектичними.
Слайд 10Діаграма станів сплаву
Розрізняють чотири типи:
механічна суміш
твердий розчин з необмеженою розчинністю
твердий розчин

з обмеженою розчинністю
хімічна сполука
Слайд 11
Механічна суміш
це сплави компоненти яких у рідкому стані необмежено розчинні

один в одному
у твердому стані нерозчинні
не утворюють хімічні сполуки:
Pb – Sb , Pb – Sn , Zn – Sn тощо
Слайд 12
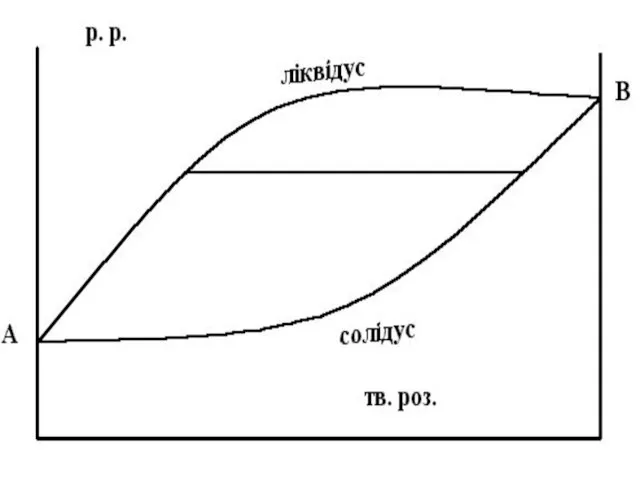
Твердий розчин з необмеженою розчинністю
компоненти сплаву мають повну взаємну розчинність як у

рідкому, так і у твердому стані
не утворюють хімічних з’єднань
(Cu – Ni; Fe – Ni; Fe – Cr; Bi– Sb).
Слайд 14
КОНОДА
лінія, що поєднує склад фаз, які знаходяться у рівновазі і

проходить паралельно осі концентрацій
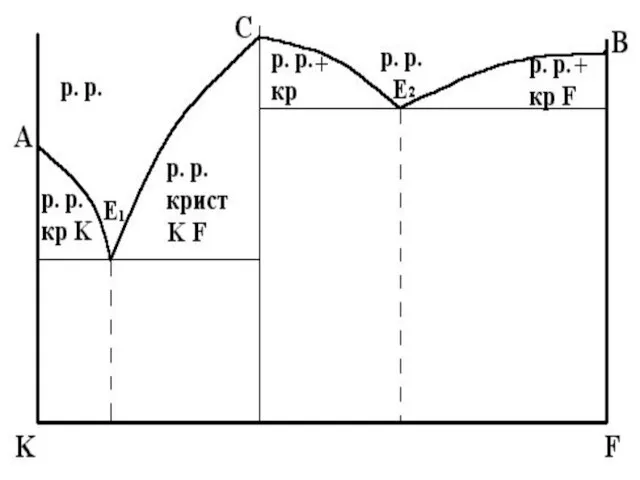
Слайд 15Твердий розчин з обмеженою розчинністю
компоненти необмежено розчинні у рідкому стані
обмежено –

у твердому
утворюють при кристалізації евтектику
(Al – Cu; Fe – C; Mg – Al ; Mg – Zn).
Слайд 17- рідкий розчин К та F ;
– кристали твердого α - розчину

речовини К;
– кристали α - твердого розчину + рідкий розчин речовин К та F ;
– кристали β-твердого розчину + рідкий розчин речовин К та F;
– кристали β-твердого розчину речовини F;
– кристали α - твердого розчину + евтектика + кристали β11-твердого розчину ;
- кристали β-твердого розчину + евтектика + кристали α 11- твердого розчину;
– кристали α + β11 твердого розчину;
– кристали β +α11 твердого розчину.
Слайд 18Хімічна сполука
компоненти яких необмежено розчинні у рідкому стані
нерозчинні у твердому
утворюють

стійкі хімічні сполуки
( Mg – Сu )
Слайд 21Правило фаз
використовується для виявлення факторів, які можна змінювати без зміни числа

фаз у системі
Фазами можуть бути:
рідкі розчини
тверді розчини
хімічні сполуки
Слайд 22ФАЗИ відрізняються
за фазовим станом :
рідкий Аl
твердий Аl
за хімічним складом :

концентрацією компонентів у кожній фазі
за типом кристалічної гратки:
Fe ОЦК та Fe ГЦК дві фази
Слайд 23ПРАВИЛО ФАЗ
встановлює кількісну залежність між числом ступенів свободи ( зовнішніх та внутрішніх

факторів) системи, що знаходяться у рівноважному стані та числом фаз і компонентів (закон Гіббса)
Слайд 24ПРАВИЛО ФАЗ
для металічних систем :
С = К - Ф + В

, де
С – число ступенів свободи
Ф – кількість компонентів
В – число зовнішніх факторів (температура та тиск)
Слайд 25ПРАВИЛО ФАЗ
Якщо прийняти, що всі перетворення відбуваються при сталому тиску, тоді рівняння

прийме вигляд:
С = К - Ф + 1
Слайд 26Число ступенів свободи
(варіантність) системи - це число зовнішніх та внутрішніх факторів (

температура, тиск, концентрація ), які можна змінювати без зміни числа фаз у системі
Слайд 27
Для однокомпонентної системи (чистого металу):
розплавлений чистий метал :
К=1 Ф=1 С

= 1 – 1 + 1, тобто температуру можна змінювати без зміни кількості фаз
Стан системи є МОНОВАРІАНТНИМ
Слайд 28
Для однокомпонентної системи (чистого металу):
кристалізація чистого металу:
К = 1 Ф

= 2 С = 1 – 2 + 1 = 0, тобто, дві фази знаходяться у рівновазі при чітко визначеній температурі (температурі плавлення) і вона не може бути змінена, поки одна із фаз не зникне
Стан системи є НОНВАРІАНТНИМ
Слайд 29Для двокомпонентної системи
- рідкий розчин :
К =2 Ф =1 С

=2 - 1 + 1 = 2
тобто, можлива зміна двох факторів (температури та концентрації ) без зміни кількості фаз у системі
Стан системи є БІВАРІАНТНИМ
Слайд 30Для двокомпонентної системи
– рідкий та твердий розчин в системі:
К = 2

Ф = 2 С = 2 – 2 + 1 = 1
тобто, із зміною температури концентрація повинна бути чітко визначена
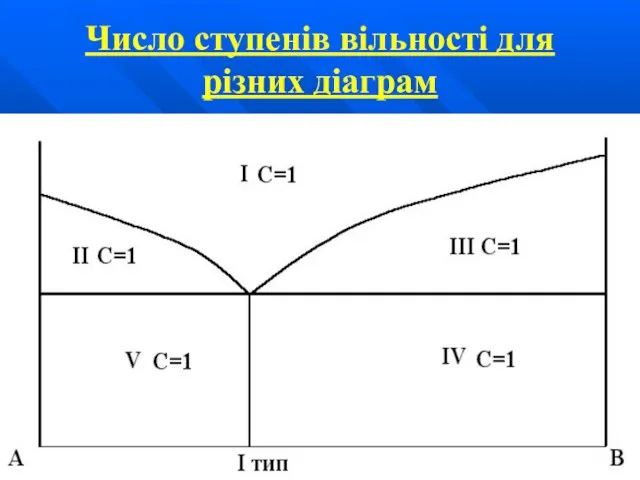
Слайд 31Число ступенів вільності для різних діаграм
Слайд 32Число ступенів вільності для різних діаграм
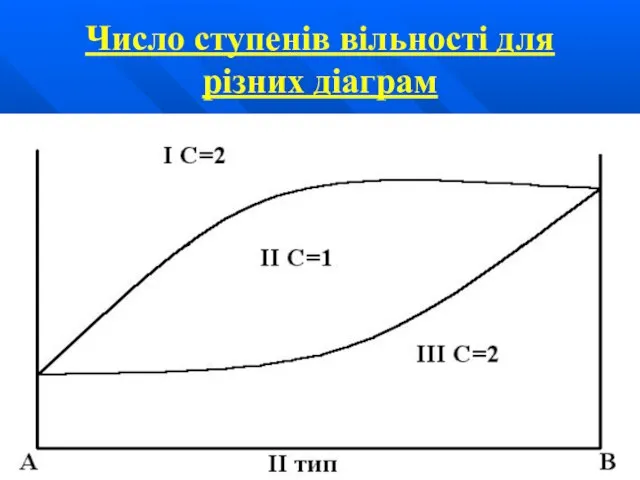
Слайд 33Число ступенів вільності для різних діаграм
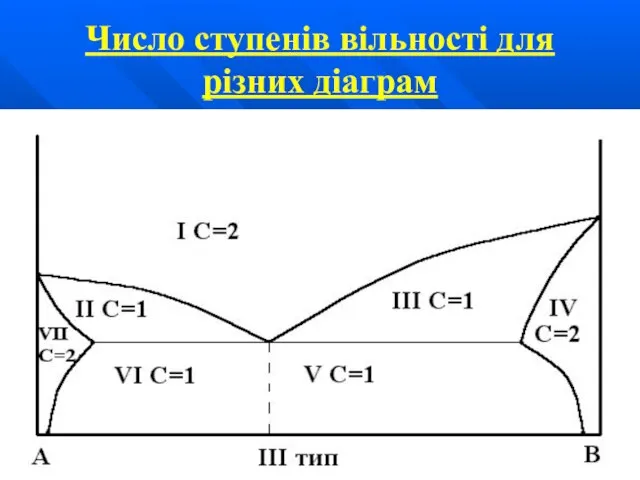
Слайд 34Число ступенів вільності для різних діаграм
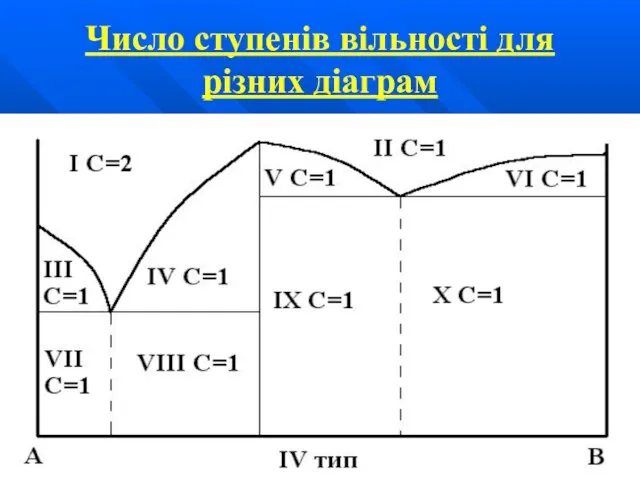
Слайд 35ПРАВИЛО ВІДРІЗКІВ
для визначення МАСОВОЇ та ОБЄМНОЇ кількості фази у заданій точці двофазної

області
для визначення КОНЦЕНТРАЦІЇ КОМПОНЕНТІВ у фазах
Слайд 36МАСОВА та ОБ’ЄМНА
кількість фаз
Кількість рідкої фази :
Р = ( ТО : ТЕ
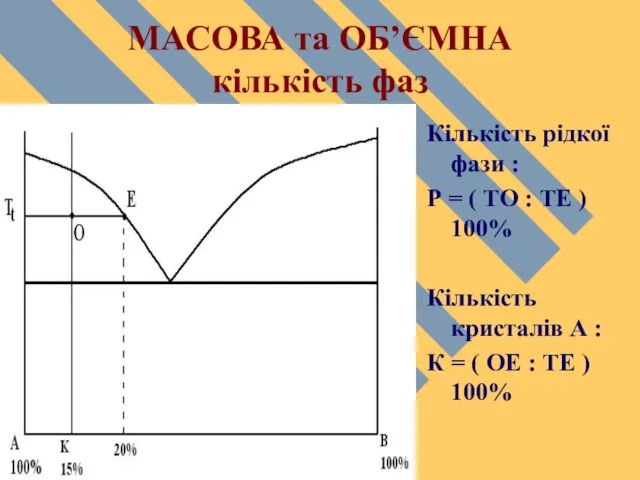
) 100%
Кількість кристалів А :
К = ( ОЕ : ТЕ ) 100%
Слайд 37
КОНЦЕНТРАЦІЯ КОМПОНЕНТІВ у фазах
Концентрація
рідкої фази буде відповідати проекції точки n на
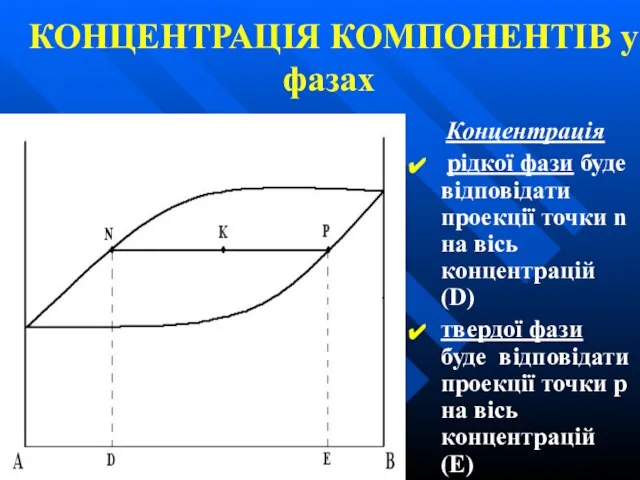
вісь концентрацій (D)
твердої фази буде відповідати проекції точки p на вісь концентрацій (Е)
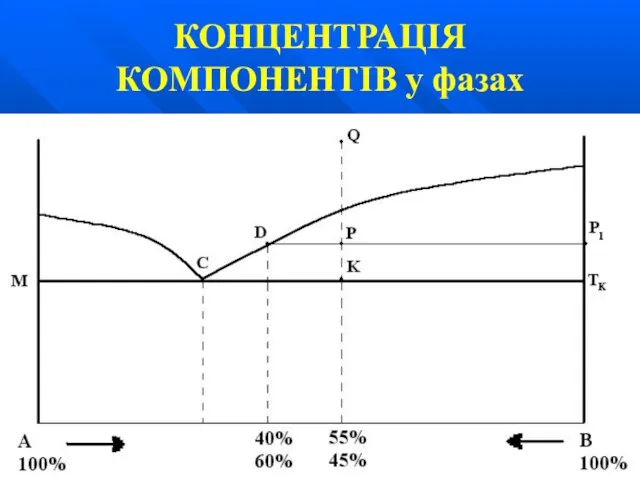
Слайд 38
КОНЦЕНТРАЦІЯ КОМПОНЕНТІВ у фазах
Слайд 395.Зв’язок між властивостями та типом діаграм сплавів

Слайд 40Курнаковим М.С. та Бочваром А.А.
було встановлено:
1.У сплавах , що мають структуру

механічних сумішей (I типу) , властивості змінюються прямолінійно:
Деякі механічні властивості ( такі як міцність та твердість) збільшуються особливо у зоні евтектичних сплавів, де фази мають мілко зернисту структуру
Слайд 41Курнаковим М.С. та Бочваром А.А.
було встановлено:
2.У сплавах – твердих розчинах (IIтипу)

властивості змінюються криволінійно:
вже при невеликих домішках другого компоненту такі характеристики як твердість, електроопір тощо стають вищими, ніж властивості компонентів
електропровідність та магнітна проникність знижуються
Слайд 42Курнаковим М.С. та Бочваром А.А.
було встановлено:
3.У сплавах – твердих розчинах з

обмеженою розчинністю (IIIтипу) властивості для :
однофазних твердих розчинів змінюються криволінійно
двофазних - прямолінійно
Слайд 43
Курнаковим М.С. та Бочваром А.А.
було встановлено:
4.У сплавах, що утворюють хімічні сполуки

(IY типу) властивості змінюються стрибком
Слайд 44ОДНОФАЗНІ СПЛАВИ
мають кращі властивості, ніж двофазні
краще деформуються у холодному та гарячому

стані
більш корозійностійкі, ніж двофазні
Слайд 45ОДНОФАЗНИЙ ТВЕРДИЙ РОЗЧИН
має погану здатність до лиття
пластичний
добре прокатується, пресується
твердість,

міцність та електроопір вище ніж у чистих металів
електропровідність та коефіцієнт електроопору менше ніж у чистих металів
Слайд 46ДВОФАЗНІ СПЛАВИ
легше обробляються різанням
мають погану здатність до лиття
чим більша відстань

між лініями ліквідус та солідус, тим менше рідкоплинність
Слайд 47ЕВТЕКТИЧНІ СПЛАВИ
добре формуються литтям та різанням











































 ОБМАНИ МЕНЯ ЕСЛИ СМОЖЕШЬ
ОБМАНИ МЕНЯ ЕСЛИ СМОЖЕШЬ Пришкольный лагерь «Солнышко»
Пришкольный лагерь «Солнышко» МОУ СОШ № 4 . г. Всеволожск Ленинградская область Тема. Дисциплина Ученица 7 класса «Б» Матвейчук Антонина Учитель Потапова О.Н.
МОУ СОШ № 4 . г. Всеволожск Ленинградская область Тема. Дисциплина Ученица 7 класса «Б» Матвейчук Антонина Учитель Потапова О.Н. Презентация на тему Оплодотворение и развитие зародыша
Презентация на тему Оплодотворение и развитие зародыша математический диктантпроверь себя и оцени
математический диктантпроверь себя и оцени Мониторинг комплексных проектов модернизации образования: отслеживать ход реализации
Мониторинг комплексных проектов модернизации образования: отслеживать ход реализации The Art of Delegation_How to Increase Manager's Efficiency_Marharyta Kotelevets
The Art of Delegation_How to Increase Manager's Efficiency_Marharyta Kotelevets наречие
наречие Галогены
Галогены Физкультура и спорт
Физкультура и спорт Презентация к уроку истории России 9 кл.
Презентация к уроку истории России 9 кл. Инвестиционная стратегия ПАО ФК Открытие
Инвестиционная стратегия ПАО ФК Открытие Казань в судьбе Сергея Тимофеевича Аксакова
Казань в судьбе Сергея Тимофеевича Аксакова Crown Jewels
Crown Jewels Развитие у школьников умений исследовательской деятельности
Развитие у школьников умений исследовательской деятельности Румыния и Венгрия во второй половине 20 в
Румыния и Венгрия во второй половине 20 в Комплексне рішення по датацентрам від компанії Інком. Проект в ПАТ «Кредобанк»
Комплексне рішення по датацентрам від компанії Інком. Проект в ПАТ «Кредобанк» Профилактика кризисных ситуаций в подростковом возрасте
Профилактика кризисных ситуаций в подростковом возрасте butterflies
butterflies Шрифт надписи
Шрифт надписи Командитне підприємство
Командитне підприємство Деревянная архитектура
Деревянная архитектура Лесные и торфяные пожары
Лесные и торфяные пожары Корзиночки, тарталетки
Корзиночки, тарталетки Транспортная безопасность
Транспортная безопасность Предлагаем услуги следующих видов наружной рекламы: - Термоформовка - Ателье (пошив униформы, палаток, тентов и т.д.)
Предлагаем услуги следующих видов наружной рекламы: - Термоформовка - Ателье (пошив униформы, палаток, тентов и т.д.) 1
1 Канада
Канада