Содержание
- 2. ядро електрони “+” “-” Атом - найдрібніша складова речовини Атом (з грецької “неподільний”) – найдрібніша, хімічно
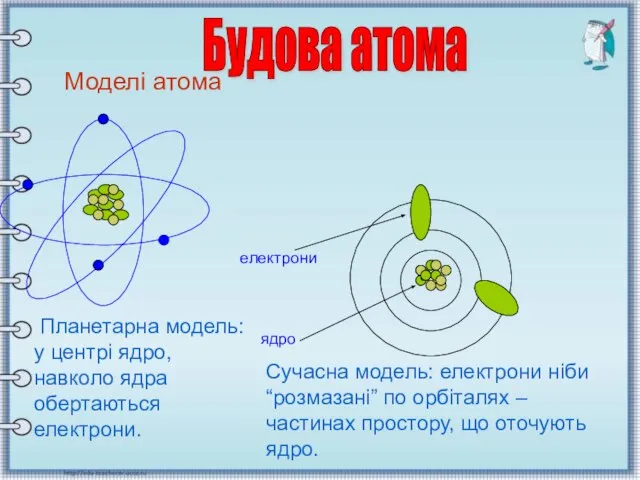
- 3. Моделі атома Моделі атома Планетарна модель: у центрі ядро, навколо ядра обертаються електрони. електрони ядро Сучасна
- 4. Будова атома Атоми надзвичайно малі, а їх ядро ще у 10-100 разів менші за сам атом.
- 5. Ім’я: Атом – найдрібніша частинка речовини. Батьки: Демокріт, Левкіпп – 2500р. тому, давньогрецькі вчені (гіпотеза про
- 6. Розміри атомів приблизно дорівнюють 0,0000000001м. Розміри атомів приблизно дорівнюють 0,0000000001м. Якби всі люди нашої планети проводили
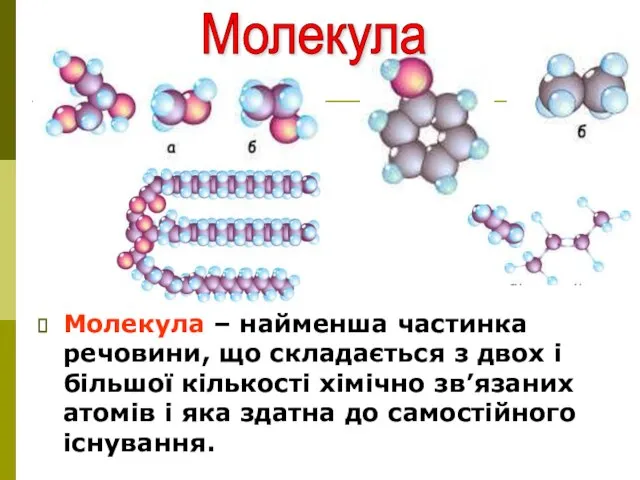
- 7. Молекула – найменша частинка речовини, що складається з двох і більшої кількості хімічно зв’язаних атомів і
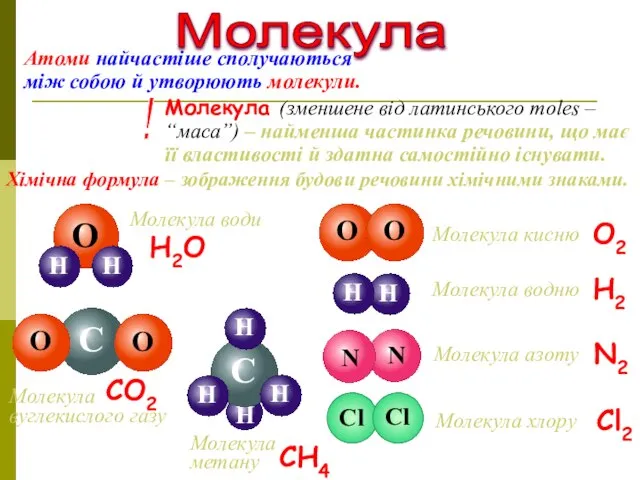
- 8. Молекула Молекула (зменшене від латинського moles – “маса”) – найменша частинка речовини, що має її властивості
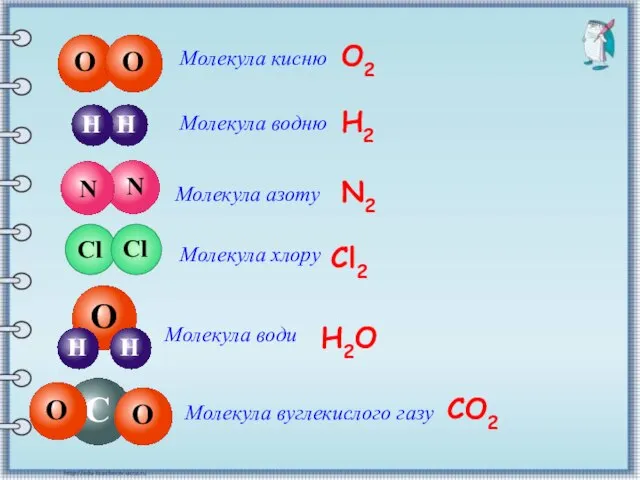
- 9. О Молекула кисню Молекула водню Молекула азоту Молекула хлору О2 Н2 N2 Cl2 Молекула води Н2O
- 10. 1. Всі тіла складаються з частинок. 2. Ці частинки перебувають у безперервному хаотичному русі. 3. Частинки
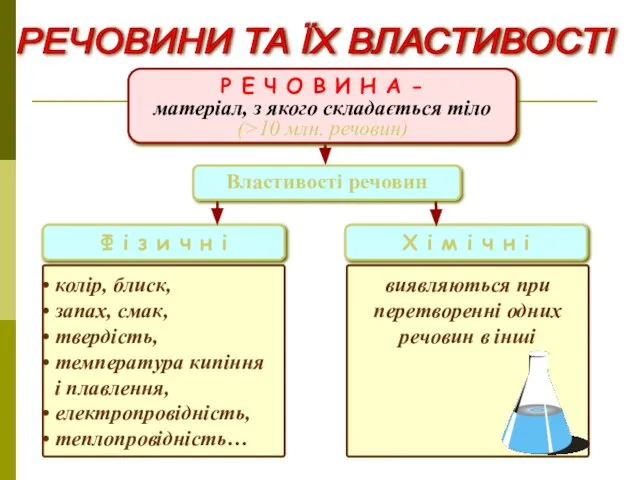
- 11. РЕЧОВИНИ ТА ЇХ ВЛАСТИВОСТІ Р Е Ч О В И Н А - матеріал, з якого
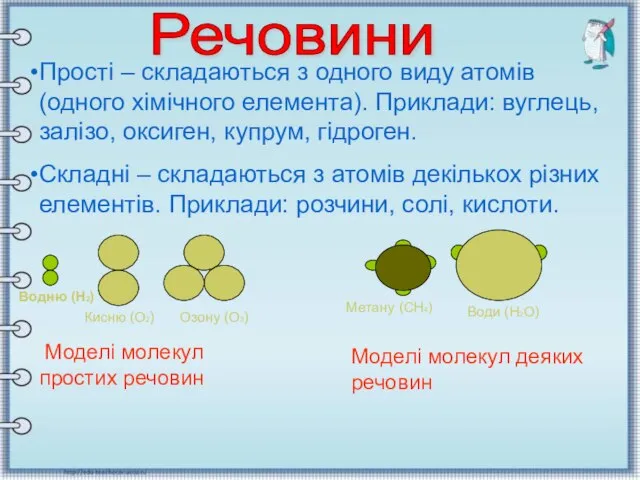
- 12. Прості – складаються з одного виду атомів (одного хімічного елемента). Приклади: вуглець, залізо, оксиген, купрум, гідроген.
- 13. Хімічні елементи Хімічний елемент (з латинської “стихія”, “первинна речовина”) – певний за будовою тип атома. Йєнс
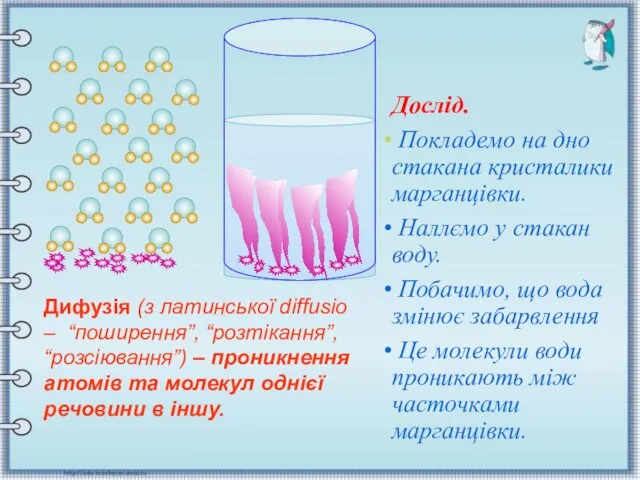
- 14. Англійський ботанік Броун (ХІХст.) Англійський ботанік Броун (ХІХст.) Дифузією називають взаємне проникнення дотичних речовин одна в
- 15. Дослід. Покладемо на дно стакана кристалики марганцівки. Наллємо у стакан воду. Побачимо, що вода змінює забарвлення
- 16. Між молекулами є проміжки. Молекули рухаються хаотично. Зі збільшенням температури збільшується швидкість молекул. Явище дифузії існує
- 17. * Усі речовини складаються з: води; повітря; з молекул і атомів. Речовина – це: те, з
- 19. Скачать презентацию









 Квиллинг-Необычные возможности обычной бумаги
Квиллинг-Необычные возможности обычной бумаги Презентация на тему Наш друг светофор
Презентация на тему Наш друг светофор г.Донецк
г.Донецк MAPLE
MAPLE Металлургия в Китае
Металлургия в Китае Фрезы для педикюра
Фрезы для педикюра Закон Ома для участка цепи
Закон Ома для участка цепи Герои Советского Союза Петуховского района к 65- летию Великой Победы
Герои Советского Союза Петуховского района к 65- летию Великой Победы Дидактическое пособие по формированию финансовой грамотности старших дошкольников Банковский терминал
Дидактическое пособие по формированию финансовой грамотности старших дошкольников Банковский терминал FOREIGN TRADE
FOREIGN TRADE  Применение компрессорно- конденсаторных блоков с плавным регулированием производительности компрессора в технологическом охлаж
Применение компрессорно- конденсаторных блоков с плавным регулированием производительности компрессора в технологическом охлаж МАРКЕТИНГОВА ЦІНОВА ПОЛІТИКА
МАРКЕТИНГОВА ЦІНОВА ПОЛІТИКА  Symbology of the Russian Federation
Symbology of the Russian Federation Роль системы развития персонала организации
Роль системы развития персонала организации Поиск творческого решения
Поиск творческого решения Применение специальных упражнений для восстановления зрения, исправления осанки и снижения веса9_urok_fizkultury
Применение специальных упражнений для восстановления зрения, исправления осанки и снижения веса9_urok_fizkultury База данных (БД) – основа информационных систем(ИС)
База данных (БД) – основа информационных систем(ИС) ГОСТ 102-75. Фанера березовая авиационная. Технические условия
ГОСТ 102-75. Фанера березовая авиационная. Технические условия Японская символика
Японская символика Надежность и долговечность автомобиля. Техническое обслуживание и ремонт машин
Надежность и долговечность автомобиля. Техническое обслуживание и ремонт машин Разработка масштабируемой системы диагностирования технологического оборудования
Разработка масштабируемой системы диагностирования технологического оборудования Урок истории России в 7 классе
Урок истории России в 7 классе Презентация на тему фразеологизмы
Презентация на тему фразеологизмы  Основные положения теории деятельности А. Н. Леонтьева
Основные положения теории деятельности А. Н. Леонтьева 13
13 Учитель математики МОУ СОШ 1 Тупикова Л. М.. «Мне приходится делить время между политикой и уравнениями. Однако уравнения, по-моему,
Учитель математики МОУ СОШ 1 Тупикова Л. М.. «Мне приходится делить время между политикой и уравнениями. Однако уравнения, по-моему,  Презентация на тему Молдавия
Презентация на тему Молдавия  Eyebrow tremor
Eyebrow tremor