Содержание
- 2. В 1903 году английским ученым Томсоном была предложена модель атома, которую в шутку назвали «булочкой с
- 3. Опыт Резерфорда: предложение своей модели атома В своих опытах Резерфорд пропускал пучок альфа-частиц сквозь тонкую золотую
- 4. То есть было установлено, что внутри атома существует нечто твердое и небольшое, от чего и отскакивали
- 5. Планетарная модель строения атома Резерфорд предположил, что атом устроен подобно планетарной системе. Как вокруг Солнца на
- 6. Планетарная модель атома объясняет основные закономерности рассеяния заряженных частиц. Так как большая часть пространства в атоме
- 8. Скачать презентацию
Слайд 2В 1903 году английским ученым Томсоном была предложена модель атома, которую в
В 1903 году английским ученым Томсоном была предложена модель атома, которую в
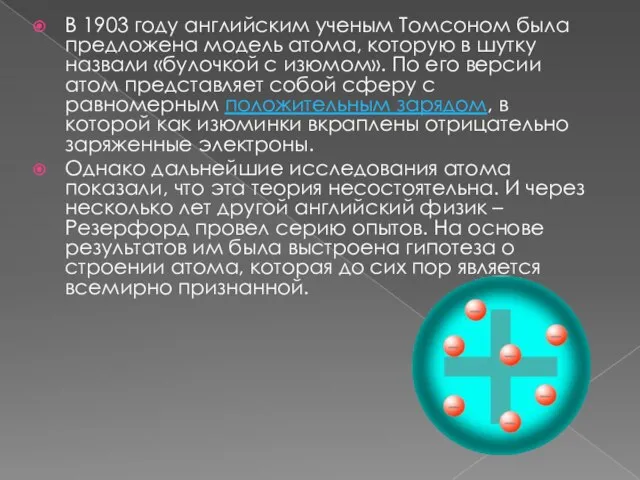
шутку назвали «булочкой с изюмом». По его версии атом представляет собой сферу с равномерным положительным зарядом, в которой как изюминки вкраплены отрицательно заряженные электроны.
Однако дальнейшие исследования атома показали, что эта теория несостоятельна. И через несколько лет другой английский физик – Резерфорд провел серию опытов. На основе результатов им была выстроена гипотеза о строении атома, которая до сих пор является всемирно признанной.
Однако дальнейшие исследования атома показали, что эта теория несостоятельна. И через несколько лет другой английский физик – Резерфорд провел серию опытов. На основе результатов им была выстроена гипотеза о строении атома, которая до сих пор является всемирно признанной.
Слайд 3
Опыт Резерфорда: предложение своей модели атома
В своих опытах Резерфорд пропускал пучок альфа-частиц сквозь тонкую
Опыт Резерфорда: предложение своей модели атома
В своих опытах Резерфорд пропускал пучок альфа-частиц сквозь тонкую

золотую фольгу. Золото было выбрано за пластичность, которая позволила создать очень тонкую фольгу, толщиной едва ли не в один слой молекул. За фольгой располагался специальный экран, подсвечивавшийся при бомбардировке попадающими на него альфа частицами. По теории Томсона альфа-частицы должны были беспрепятственно проходить сквозь фольгу, совсем немного отклоняясь в стороны. Однако, оказалось, что часть частиц так и вела себя, а совсем небольшая часть отскакивала назад, как будто ударившись во что-то.
Слайд 4То есть было установлено, что внутри атома существует нечто твердое и небольшое,
То есть было установлено, что внутри атома существует нечто твердое и небольшое,

от чего и отскакивали альфа-частицы. Тогда-то Резерфорд и предложил планетарную модель строения атома. Планетарная модель атома по Резерфорду объясняла результаты проведения как его экспериментов, так и опытов его коллег. До сего дня не предложено лучшей модели, хотя некоторые аспекты этой теории все равно не согласуются с практикой в некоторых очень узких областях науки. Но в основном, планетарная модель атома самая пригодная из всех. В чем же состоит эта модель?
Слайд 5Планетарная модель строения атома
Резерфорд предположил, что атом устроен подобно планетарной системе. Как
Планетарная модель строения атома
Резерфорд предположил, что атом устроен подобно планетарной системе. Как
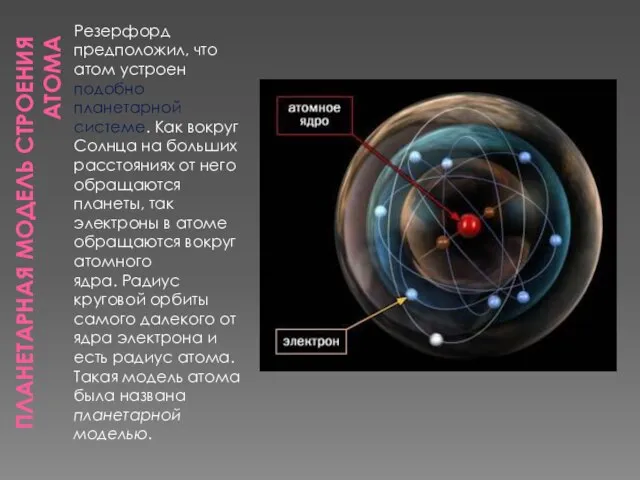
вокруг Солнца на больших расстояниях от него обращаются планеты, так электроны в атоме обращаются вокруг атомного ядра. Радиус круговой орбиты самого далекого от ядра электрона и есть радиус атома. Такая модель атома была названа планетарной моделью.
Слайд 6Планетарная модель атома объясняет основные закономерности рассеяния заряженных частиц.
Так как большая часть
Планетарная модель атома объясняет основные закономерности рассеяния заряженных частиц.
Так как большая часть

пространства в атоме между атомным ядром и обращающимися вокруг него электронами пуста, быстро заряженные частицы могут почти свободно проникать через довольно значительные слои вещества, содержащие несколько тысяч слоев атомов.
При столкновениях с отдельными электронами быстрые заряженные частицы испытывают рассеяние на очень большие углы, так как масса электрона мала. Однако в тех редких случаях, когда быстрая заряженная частица пролетает на очень близком расстоянии от одного из атомных ядер, под действием силы электрического поля атомного ядра может произойти рассеяние заряженной частицы на любой угол до 180°
При столкновениях с отдельными электронами быстрые заряженные частицы испытывают рассеяние на очень большие углы, так как масса электрона мала. Однако в тех редких случаях, когда быстрая заряженная частица пролетает на очень близком расстоянии от одного из атомных ядер, под действием силы электрического поля атомного ядра может произойти рассеяние заряженной частицы на любой угол до 180°
Следующая -
Презентация на тему Фотоэффект (11 класс)  Основы работы на ЭВМЗанятие 3: протоколы передачи данных
Основы работы на ЭВМЗанятие 3: протоколы передачи данных Кафедра МПТЭ
Кафедра МПТЭ Конкурс:Лучший преподаватель медицинского вуза. Золотые кадры медицины
Конкурс:Лучший преподаватель медицинского вуза. Золотые кадры медицины Социология, социальная психология
Социология, социальная психология ЭФФЕКТ КАЗИМИРА: ОТ НАНОТЕХНОЛОГИЙ ДО ФИЗИКИ ВСЕЛЕННОЙ
ЭФФЕКТ КАЗИМИРА: ОТ НАНОТЕХНОЛОГИЙ ДО ФИЗИКИ ВСЕЛЕННОЙ Аниме
Аниме Квартирная металлическая дверь
Квартирная металлическая дверь Объединенная Консалтинговая Компания“Клиентс Риджинал Компани.”Полный Спектр Консалтинга и Услуг на территории Российской Фе
Объединенная Консалтинговая Компания“Клиентс Риджинал Компани.”Полный Спектр Консалтинга и Услуг на территории Российской Фе Гигиена зрения
Гигиена зрения Презентация на тему Русская история и русская литература XIX века
Презентация на тему Русская история и русская литература XIX века  Понимание красоты человека в европейском и русском искусстве
Понимание красоты человека в европейском и русском искусстве "Классный руководитель- родители-дети: искусство жить вместе"
"Классный руководитель- родители-дети: искусство жить вместе" ПРЕДСТАВЛЯЕТ
ПРЕДСТАВЛЯЕТ Елочка
Елочка Процессы управления стоимостью
Процессы управления стоимостью Linguistic aspect of political language
Linguistic aspect of political language О мерах социальной поддержки и организации социального обслуживания граждан с ограниченными возможностями в Тихвинском районе
О мерах социальной поддержки и организации социального обслуживания граждан с ограниченными возможностями в Тихвинском районе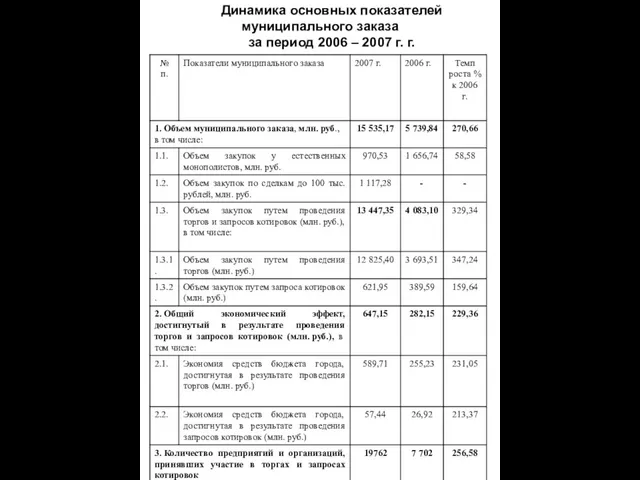 Динамика основных показателей муниципального заказа за период 2006 – 2007 г. г.
Динамика основных показателей муниципального заказа за период 2006 – 2007 г. г. Маршрутная карта
Маршрутная карта ?
? Формы государственно-управленческих решений
Формы государственно-управленческих решений Испьзование Sanako 1200 в учебной среде школы Наброски слушателя семинара
Испьзование Sanako 1200 в учебной среде школы Наброски слушателя семинара “Четыре основы в построении отношений, которые служат залогом хорошего брака” (и не только)
“Четыре основы в построении отношений, которые служат залогом хорошего брака” (и не только) ЮАР
ЮАР 5 Доконаний i недоконаний вид дiєслова
5 Доконаний i недоконаний вид дiєслова Праздник и карнавал
Праздник и карнавал  Вставь пропущенные окончания.
Вставь пропущенные окончания. Психологическое консультирование жертв насилия
Психологическое консультирование жертв насилия