Слайд 2Соли угольной кислоты-карбонаты и гидрокарбонаты.
Na2CO3 –карбонат натрия
NaHCO3 -гидрокарбонат натрия
CaCO3 -карбонат кальция
Ca(HCO3)2 –гидрокарбонат

кальция
Слайд 3Карбонат натрия.
Карбона́т на́трия — химическое соединение Na2CO3, натриевая соль угольной кислоты.
Карбонат натрия представляет

собой бесцветный кристаллический порошок.
Слайд 4Получение карбоната натрия.
Способ 1.
Способ Леблана.
Уголь восстанавливает сульфат натрия до сульфида:
Na2SO4 + 2C

→ Na2S + 2CO2↑.
Сульфид натрия реагирует с карбонатом кальция:
Na2S + СаСО3 → Na2CO3 + CaS.
Слайд 5Способ 2.
Промышленный аммиачный способ (способ Сольве).
NH3 + CO2 + H2O + NaCl

→ NaHCO3 + NH4Cl
2NaHCO3 →(t) Na2CO3 + CO2↑ + H2O
2NH4Cl + Ca(OH)2 → CaCl2 + 2NH3↑ + 2H2O
Слайд 6Способ 3.
Способ Хоу.
Отличается от процесса Леблана тем, что не использует карбонат кальция.

Слайд 9Реакция с кислотами.
Гидрокарбонат натрия реагирует с кислотами, с образованием соли и угольной

кислоты, которая тут же распадается на углекислый газ и воду:
NaHCO3 + HCl → NaCl + H2CO3 H2CO3 → H2O + CO2↑ В быту чаще встречается такая реакция с уксусной кислотой, с образованием ацетата натрия:
NaHCO3 + CH3COOH → CH3COONa + H2O + CO2↑
Слайд 10Карбонат кальция.
Карбонат кальция (мел, углекислый кальций, известняк) — неорганическое химическое соединение, соль угольной

кислоты и кальция. В природе встречается в виде минералов — кальцита, арагонита и ватерита. Карбонат кальция является главной составной частью известняка, мела и мрамора. Нерастворим в воде и этаноле.
Зарегистрирован как белый пищевой краситель (E170).
Слайд 12Химические свойства.
При нагревании до 900−1000 °C расщепляется на кислотный оксид — углекислый газ CO2

и оксид — негашёную известь CaO.
В воде с углекислым газом растворяется, образуя кислую соль — гидрокарбонат кальция Ca(HCO3)2.
Слайд 13Гидрокарбонат кальция.
Все гидрокарбонаты в воде растворимы. Гидрокарбонат кальция обусловливает временную жёсткость воды.

В организме гидрокарбонаты выполняют важную физиологическую роль — регулируют постоянство реакций в крови. При нагревании раствора гидрокарбоната кальция он разлагается:












 Презентация на тему Эдуард Мане
Презентация на тему Эдуард Мане 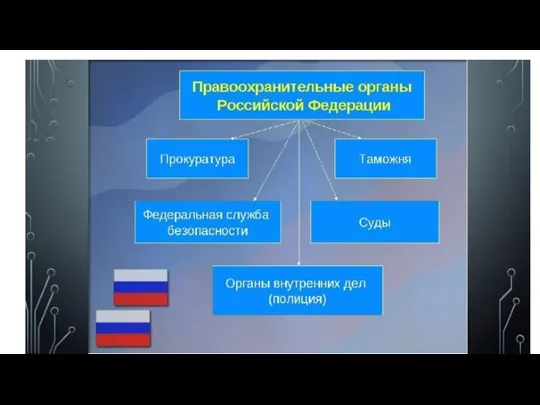 Правоохранительные органы Российской Федерации
Правоохранительные органы Российской Федерации Организация сопровождаемого проживания граждан с нарушениями
Организация сопровождаемого проживания граждан с нарушениями 学校
学校 Типы сварных швов
Типы сварных швов Отчет о размещении вакансий
Отчет о размещении вакансий СОВРЕМЕННОЕ ПРОФЕССИОНАЛЬНОЕ ОБРАЗОВАНИЕДЛЯ РОССИЙСКОЙ ИННОВАЦИОННОЙ СИСТЕМЫВ ОБЛАСТИ ЭЛЕКТРОНИКИ
СОВРЕМЕННОЕ ПРОФЕССИОНАЛЬНОЕ ОБРАЗОВАНИЕДЛЯ РОССИЙСКОЙ ИННОВАЦИОННОЙ СИСТЕМЫВ ОБЛАСТИ ЭЛЕКТРОНИКИ Сравнительный анализ развития лыжероллеров
Сравнительный анализ развития лыжероллеров Прыжки в длину
Прыжки в длину Презентация на тему Механические колебания 11 класс
Презентация на тему Механические колебания 11 класс  Понятия частей речи
Понятия частей речи Презентация Нагрузки и воздействия
Презентация Нагрузки и воздействия Презентация на тему Разнообразие животных
Презентация на тему Разнообразие животных  English theater
English theater  Класс Однодольные, характерные признаки растений семейства злаковых
Класс Однодольные, характерные признаки растений семейства злаковых Еңбек нормасы. Өнім нормасы
Еңбек нормасы. Өнім нормасы Формы и методы профессиональной ориентации
Формы и методы профессиональной ориентации e70f443261a743aba5fb4ba5defd798a
e70f443261a743aba5fb4ba5defd798a Функциональные стили речи
Функциональные стили речи Комплексная программа развития и воспитания дошкольников в Образовательной системе "Школа 2100"
Комплексная программа развития и воспитания дошкольников в Образовательной системе "Школа 2100" Презентация на тему Вельможи Древнего ЕГИПТА
Презентация на тему Вельможи Древнего ЕГИПТА  Маршалы Великой Отечественной войны
Маршалы Великой Отечественной войны Исторические лица земли Тверской, их жизнь и деяния, составляющие гордость региона
Исторические лица земли Тверской, их жизнь и деяния, составляющие гордость региона Природный газ
Природный газ Михайленко Юлия Борисовна учитель начальных классов ГБОУ гимназии № 1518 г. Москвы
Михайленко Юлия Борисовна учитель начальных классов ГБОУ гимназии № 1518 г. Москвы Оркестр. Инструменты симфонического оркестра
Оркестр. Инструменты симфонического оркестра МАТЕРИАЛЫ ДЛЯ ЖБК. АРМАТУРА
МАТЕРИАЛЫ ДЛЯ ЖБК. АРМАТУРА  Богиня Молва (Фама, Осса)
Богиня Молва (Фама, Осса)