Содержание
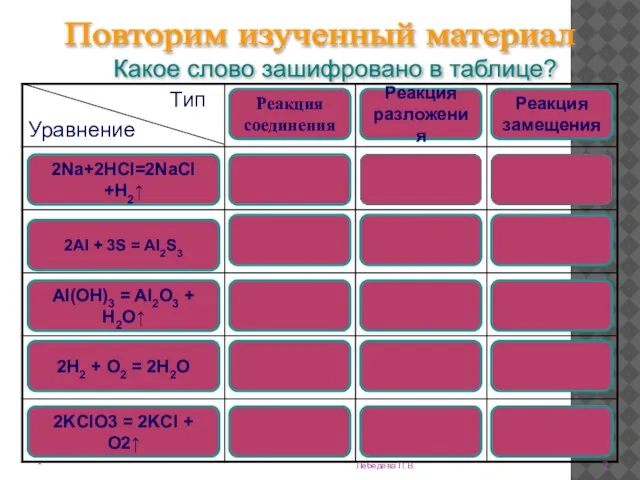
- 2. * Лебедева Л.В. Повторим изученный материал Какое слово зашифровано в таблице? 2Na+2HCl=2NaCl +H2↑ 2Al + 3S
- 3. Реакции соединения - это реакции, при которых из нескольких веществ образуется одно сложное. Реакции замещения -
- 4. Как расставить коэффициенты в реакциях с нечётным числом атомов? 5 10 Обратите внимание! Р + О
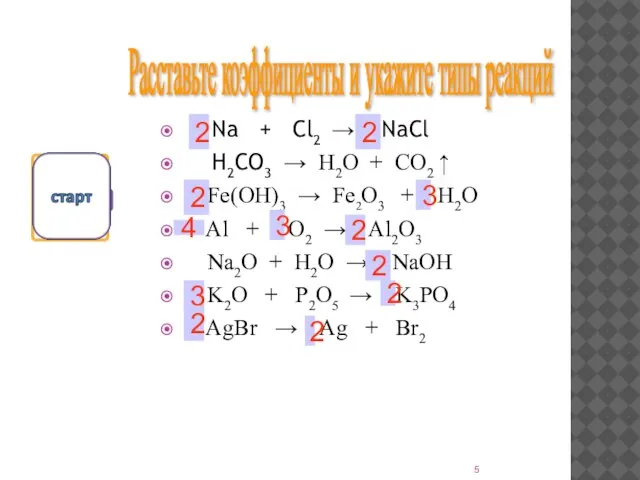
- 5. Na + Cl2 → NaCl H2CO3 → H2O + CO2 ↑ Fe(OH)3 → Fe2O3 + H2O
- 6. Цель урока: -познакомиться с реакциями обмена, дать определение данным реакциям -установить условия протекания реакций обмена до
- 7. Химические уравнения. Реакции обмена. Правила техники безопасности Реакция нейтрализации Лабораторные опыты Условия течения реакций идущих до
- 8. NaOH + HCl = NaCl + H2O Запишите уравнение подобной реакции между серной кислотой и гидроксидом
- 9. Не брать вещества руками Осторожно! ..При попадании на руки кислоты и щелочи вызывают ожог Сыпучие химические
- 10. Получите нерастворимый Fe(OH)3↓. В пробирку налейте 1 мл гидроксида натрия и прилейте несколько капель хлорида железа
- 11. На дне стакана равномерно разместите ложечку соды (карбоната натрия) и прилейте 2 мл раствора серной кислоты,
- 12. А если бы в пробирках проходила реакция нейтрализации между NaCl и H2SO4 ? 2NaCl + H2SO4
- 14. Скачать презентацию









 Презентация на тему Эдуард Мане
Презентация на тему Эдуард Мане 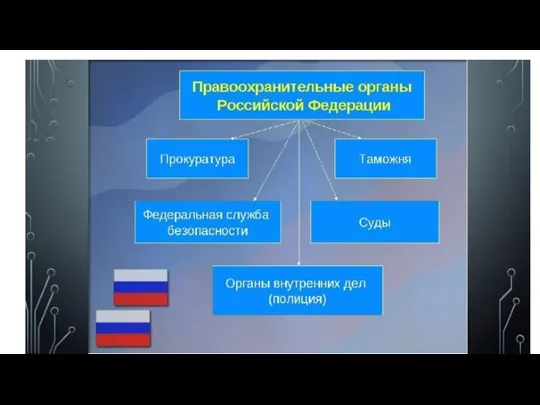 Правоохранительные органы Российской Федерации
Правоохранительные органы Российской Федерации Организация сопровождаемого проживания граждан с нарушениями
Организация сопровождаемого проживания граждан с нарушениями 学校
学校 Типы сварных швов
Типы сварных швов Отчет о размещении вакансий
Отчет о размещении вакансий СОВРЕМЕННОЕ ПРОФЕССИОНАЛЬНОЕ ОБРАЗОВАНИЕДЛЯ РОССИЙСКОЙ ИННОВАЦИОННОЙ СИСТЕМЫВ ОБЛАСТИ ЭЛЕКТРОНИКИ
СОВРЕМЕННОЕ ПРОФЕССИОНАЛЬНОЕ ОБРАЗОВАНИЕДЛЯ РОССИЙСКОЙ ИННОВАЦИОННОЙ СИСТЕМЫВ ОБЛАСТИ ЭЛЕКТРОНИКИ Сравнительный анализ развития лыжероллеров
Сравнительный анализ развития лыжероллеров Прыжки в длину
Прыжки в длину Презентация на тему Механические колебания 11 класс
Презентация на тему Механические колебания 11 класс  Понятия частей речи
Понятия частей речи Презентация Нагрузки и воздействия
Презентация Нагрузки и воздействия Презентация на тему Разнообразие животных
Презентация на тему Разнообразие животных  English theater
English theater  Класс Однодольные, характерные признаки растений семейства злаковых
Класс Однодольные, характерные признаки растений семейства злаковых Еңбек нормасы. Өнім нормасы
Еңбек нормасы. Өнім нормасы Формы и методы профессиональной ориентации
Формы и методы профессиональной ориентации e70f443261a743aba5fb4ba5defd798a
e70f443261a743aba5fb4ba5defd798a Функциональные стили речи
Функциональные стили речи Комплексная программа развития и воспитания дошкольников в Образовательной системе "Школа 2100"
Комплексная программа развития и воспитания дошкольников в Образовательной системе "Школа 2100" Презентация на тему Вельможи Древнего ЕГИПТА
Презентация на тему Вельможи Древнего ЕГИПТА  Маршалы Великой Отечественной войны
Маршалы Великой Отечественной войны Исторические лица земли Тверской, их жизнь и деяния, составляющие гордость региона
Исторические лица земли Тверской, их жизнь и деяния, составляющие гордость региона Природный газ
Природный газ Михайленко Юлия Борисовна учитель начальных классов ГБОУ гимназии № 1518 г. Москвы
Михайленко Юлия Борисовна учитель начальных классов ГБОУ гимназии № 1518 г. Москвы Оркестр. Инструменты симфонического оркестра
Оркестр. Инструменты симфонического оркестра МАТЕРИАЛЫ ДЛЯ ЖБК. АРМАТУРА
МАТЕРИАЛЫ ДЛЯ ЖБК. АРМАТУРА  Богиня Молва (Фама, Осса)
Богиня Молва (Фама, Осса)