Содержание
- 2. Закрепление и обобщение материала по теме: «Железо и его соединения» 9 класс
- 3. Путешествие по стране химических вопросов
- 4. ЗНАНИЯ - ЭТО ИСТИННЫЕ СОКРОВИЩА, КОТОРЫЕ ПОЛУЧАЕТ И НАКАПЛИВАЕТ ЧЕЛОВЕК...
- 5. Для того, чтоб умным стать, Надо много понимать, материал запоминать. Что такое водород? Как реакция пойдет?
- 6. Станция 1 "Быстрая"
- 7. Станция 2 "Разминочная"
- 8. 1. В магнитном железняке содержится много железа. 2. Железо реагирует и с простыми веществами, и со
- 9. Станция 3 "Отгадай-ка!"
- 10. FeCl3 Fe(NO3)2 Fe2O3 FeS FeSO4 FeCO3
- 11. Станция 4 "Исчезнувшие слова"
- 12. 1. Металлические руды содержат …… железа. 2. …… сульфата железа(2) вступают в реакцию с медью. 3.
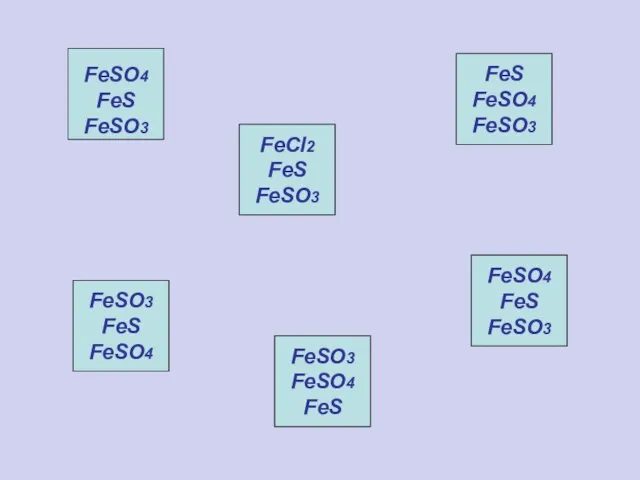
- 13. Станция 5 "Двойняшки"
- 14. FeCl2 FeS FeSO3 FeS FeSO4 FeSO3 FeSO3 FeS FeSO4 FeSO3 FeSO4 FeS FeSO4 FeS FeSO3 FeSO4
- 15. Станция 6 "Внимательная"
- 16. Станция 7 "Уравнения реакций"
- 17. Закончить схемы реакций: Железо + соляная кислота (У железа взять валентность (ll) Железо + сульфат меди(ll)
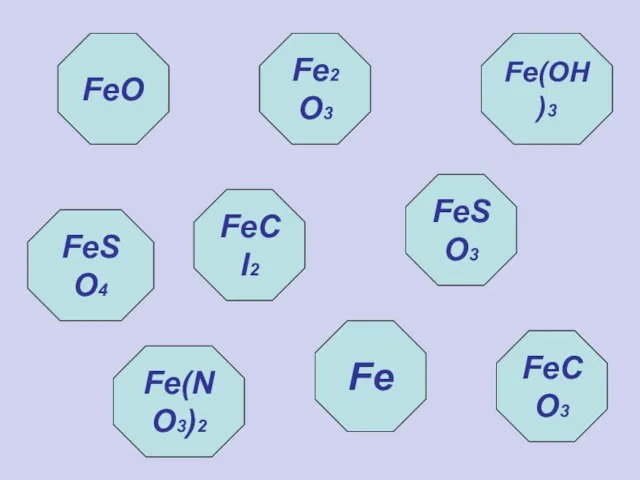
- 18. Станция 8 "Эрудит"
- 19. FeO Fe(OH)3 Fe2O3 FeSO4 FeCl2 Fe(NO3)2 Fe FeSO3 FeCO3
- 20. Станция 9 "Домашняя"
- 21. Определите массу выпавшего осадка, если нитрат железа(lll) реагирует с 600 г 40%-ного раствора гидроксида натрия Задача
- 22. всем спасибо за работу
- 24. Скачать презентацию



















 Терроризм
Терроризм  Государственные символы России
Государственные символы России РОССИЯв XVII векеСистема властии управления
РОССИЯв XVII векеСистема властии управления Класс Птицы. СОВООБРАЗНЫЕ
Класс Птицы. СОВООБРАЗНЫЕ Озера Евразии. Онежское озеро
Озера Евразии. Онежское озеро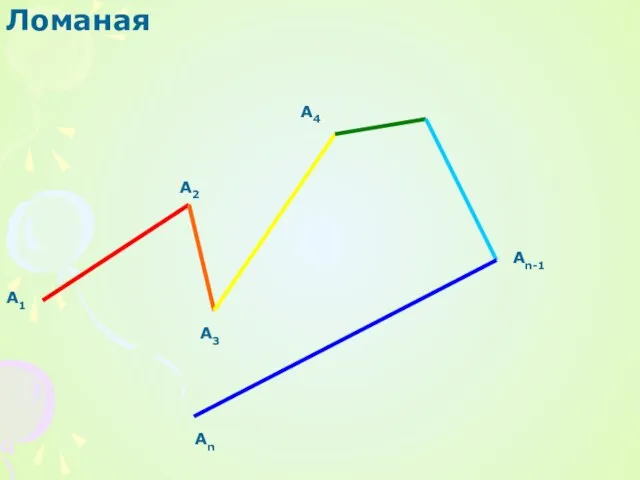 Презентация на тему Ломаная
Презентация на тему Ломаная профессиональноЕ самоопределениЕ молодежи в учреждениях начального и среднего профессионального образования
профессиональноЕ самоопределениЕ молодежи в учреждениях начального и среднего профессионального образования Пожарная безопасность
Пожарная безопасность Нарушения родительско-детских отношений как фактор риска развития патологии у детей
Нарушения родительско-детских отношений как фактор риска развития патологии у детей Traficante de drogas. Жанр игры: RPG, драма
Traficante de drogas. Жанр игры: RPG, драма Умножение вектора на число
Умножение вектора на число Народы Юго-Восточной Азии
Народы Юго-Восточной Азии Способы быстрого набора энергии. Курс Управление карьерой
Способы быстрого набора энергии. Курс Управление карьерой Рождение Иисуса и его версии
Рождение Иисуса и его версии Презентация на тему Саграда Фамилия
Презентация на тему Саграда Фамилия Гололед
Гололед по информатике
по информатике Информация вокруг нас
Информация вокруг нас Исследовательская
Исследовательская яна шапкина и данила гриднев
яна шапкина и данила гриднев Бабочки 3 класс
Бабочки 3 класс Влияние вредных привычек на внутриутробное развитие плода
Влияние вредных привычек на внутриутробное развитие плода Общероссийские антидопинговые правила
Общероссийские антидопинговые правила Медиакультура современного общества
Медиакультура современного общества Всероссийский телевизионный интернет-марафон "Финансовое просвещение из региона в регион" NON STOP
Всероссийский телевизионный интернет-марафон "Финансовое просвещение из региона в регион" NON STOP Анатомия конфликта. Конструктивные и деструктивные конфликты и пути преодаления
Анатомия конфликта. Конструктивные и деструктивные конфликты и пути преодаления Дидактические материалы к обобщающему уроку по курсу «ВОКРУГ ТЕБЯ – МИР…» АВТОР: Воронина Лариса Вячеславовна, учитель русского
Дидактические материалы к обобщающему уроку по курсу «ВОКРУГ ТЕБЯ – МИР…» АВТОР: Воронина Лариса Вячеславовна, учитель русского Концертная фотография
Концертная фотография