Содержание
- 2. Железо - один из семи металлов древности. Весьма вероятно, что человек познакомился с железом метеоритного происхождения
- 3. Многие древние народы познакомились с железом, как с металлом, упавшим с неба, т. е. как с
- 4. В древности и в средние века семь известных тогда металлов сопоставляли с семью планетами, что символизировало
- 5. Железо – второй по распространённости металл на планете(после алюминия). Содержание в земной коре составляет 4,65% по
- 6. В периодической системе железо находится в четвертом периоде, в побочной подгруппе VIII группы. Химический знак Fe
- 7. Физические свойства Чистое железо - серебристо-белый металл, обладает большой ковкостью, пластичностью и сильными магнитными свойствами. Плотность
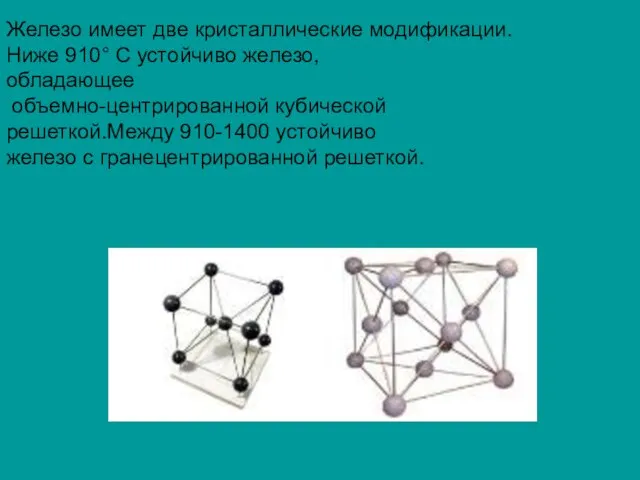
- 8. Железо имеет две кристаллические модификации. Ниже 910° С устойчиво железо, обладающее объемно-центрированной кубической решеткой.Между 910-1400 устойчиво
- 9. Получение железа. В промышленности железо получают восстановлением его из железных руд углеродом (коксом) и оксидом углерода
- 10. Химические свойства. В реакциях железо является восстановителем. Однако при обычной температуре оно не взаимодействует даже с
- 11. Железо находится в середине электрохимического ряда напряжений металлов, поэтому является металлом средней активности. Восстановительная способность у
- 12. При обычной температуре железо не взаимодействует с концентрированной серной кислотой, так как пассивируется ею. При нагревании
- 13. Из растворов солей железо вытесняет металлы, которые расположены правее его в электрохимическом ряду напряжений Fe +
- 14. Оксид железа (III) Fe2O3 порошок бурого цвета, не растворяется в воде. Оксид железа (III) получают разложением
- 15. Гидрооксид железа (II) Fe(OH)2 порошок белого цвета, не растворяется в воде. Получают его из солей железа
- 16. Железо реагирует с разбавленными серной и соляной кислотами, вытесняя из кислот водород Fe + 2HCl =FeCl2
- 17. Металлическое железо взаимодействует при нагревании с концентрированными (более 30%) растворами щелочей, образуя гидроксокомплексы. Под действием сильных
- 18. Применение и биологическая роль железа и его соединений. Важнейшие сплавы железа: чугуны и стали являются основными
- 19. Хлорид железа (III) FeCl3 применяется для очистки воды. В органическом синтезе FeCl3 применяется как катализатор. Нитрат
- 20. Железо является одним из важнейших микроэлементов в организме человека и животных (в организме взрослого человека содержится
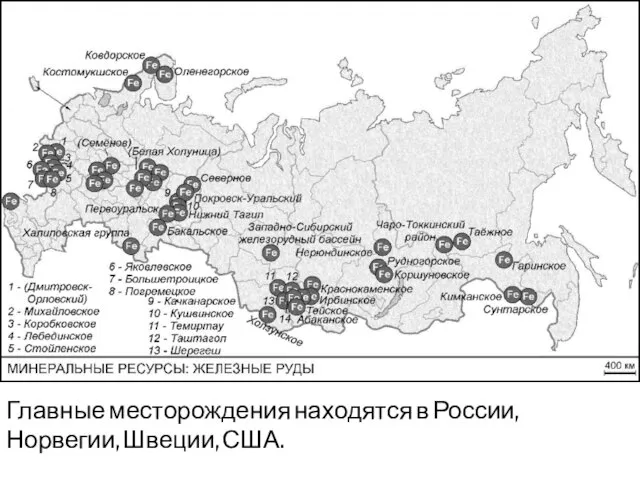
- 21. Главные месторождения находятся в России, Норвегии, Швеции, США.
- 23. Скачать презентацию


















 Родной угол. К уроку изобразительного искусства 4 класс
Родной угол. К уроку изобразительного искусства 4 класс Натюрморт из геометрических тел. Рисование с натуры. 6 класс
Натюрморт из геометрических тел. Рисование с натуры. 6 класс НАЗНАЧЕНИЕ И КЛАССИФИКАЦИЯ СИСТЕМ ВЕНТИЛЯЦИИ И КОНДИЦИОНИРОВАНИЯ
НАЗНАЧЕНИЕ И КЛАССИФИКАЦИЯ СИСТЕМ ВЕНТИЛЯЦИИ И КОНДИЦИОНИРОВАНИЯ Уважаемые друзья!
Уважаемые друзья! Музей Романтизма
Музей Романтизма Письмо МО «О формировании региональной базы данных дошкольных образовательных учреждений» № 55-37-6837/11 от 23.09.2011 Письмо МО «О формир
Письмо МО «О формировании региональной базы данных дошкольных образовательных учреждений» № 55-37-6837/11 от 23.09.2011 Письмо МО «О формир Влияние идей марксизма на изменение систем западного права в XX столетии
Влияние идей марксизма на изменение систем западного права в XX столетии Презентация на тему Расы человека
Презентация на тему Расы человека  Планы блога о счастье www.superhappy.ruна 2012 год
Планы блога о счастье www.superhappy.ruна 2012 год Факторы, влияющие на успех спортивной команды
Факторы, влияющие на успех спортивной команды Олимпийские игры история
Олимпийские игры история Западно Сибирский экономический район
Западно Сибирский экономический район Предпринимательская деятельность. Тема 1.1
Предпринимательская деятельность. Тема 1.1 Высокоскоростные магистрали в Германии
Высокоскоростные магистрали в Германии Диковина
Диковина Всё о курении, как оно есть: истоки, сущность, последствия
Всё о курении, как оно есть: истоки, сущность, последствия Частная охранная организация Рубин В
Частная охранная организация Рубин В подготовке мероприятий, посвящённых празднованию Дня России в городе Ярославле
подготовке мероприятий, посвящённых празднованию Дня России в городе Ярославле Презентация на тему Роль педагогической оценки в воспитании ребенка
Презентация на тему Роль педагогической оценки в воспитании ребенка Pedagogicheskie_osnovy_prepodavania_tvorcheskikh_distsiplin
Pedagogicheskie_osnovy_prepodavania_tvorcheskikh_distsiplin Интерактивный медиа –центр как инновационная форма сотрудничества
Интерактивный медиа –центр как инновационная форма сотрудничества Устаревшие и новые слова
Устаревшие и новые слова Компания колмар
Компания колмар Табличный процессор EXCEL
Табличный процессор EXCEL Сетевые технологии: терминология, устройства
Сетевые технологии: терминология, устройства Навечно в северных лесах Работу выполнила Нетбайло Екатерина, ученица 8 класса МОУ «Лицей №129» Руководитель: Нет
Навечно в северных лесах Работу выполнила Нетбайло Екатерина, ученица 8 класса МОУ «Лицей №129» Руководитель: Нет Базовые компоненты сетей
Базовые компоненты сетей Тема проекта
Тема проекта