Содержание
- 2. колебания атомов катализ связывание лигандов конформационные переходы вращение групп Временная шкала динамических событий в ферментах и
- 3. 102 10-10 100 10-5 Время, с Spectroscopic methods Hand mixing Flash and T jump EPR and
- 4. Изучение исходных компонентов, продуктов, их соотношений не даёт информации ни о механизме, ни о скорости реакции,
- 5. В 1872 году бывший губернатор Калифорнии Леланд Стэнфорд (Leland Stanford), бизнесмен и владелец скаковых лошадей, сделал
- 6. Eadweard Muybridge, 1878
- 7. Eadweard James Muggeridge Edward J. Muybridge (Helios) 9 April 1830 – 8 May 1904
- 8. Методы регистрации неравновесной кинетики в применении для физико-химической биологии Stopped-Flow technique Continuous flow method Quench-Flow technique
- 9. Метод «остановленной струи» Mechanical mixing-spectroscopic observation Usual deadtime ~ 1 ms; time resolution is less than
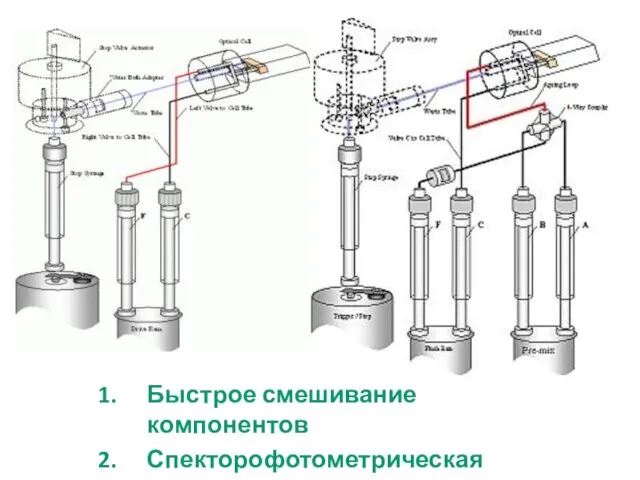
- 10. Быстрое смешивание компонентов Спекторофотометрическая детекция
- 11. Первая аппаратура для stopped-flow Britton Chance (July 24, 1913 – November 16, 2010) Chance B. The
- 12. Britton Chance and his "magic machine" for studying stop-flow kinetics, 1947
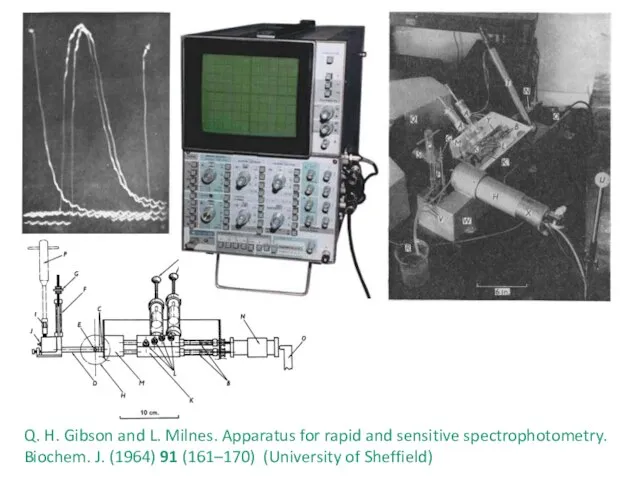
- 13. Q. H. Gibson and L. Milnes. Apparatus for rapid and sensitive spectrophotometry. Biochem. J. (1964) 91
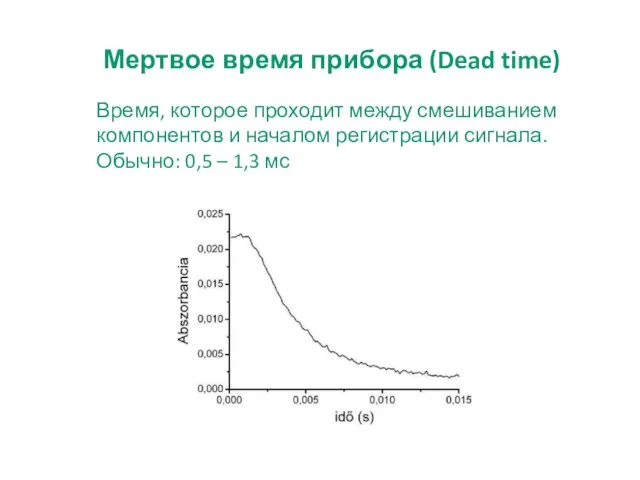
- 14. Мертвое время прибора (Dead time) Время, которое проходит между смешиванием компонентов и началом регистрации сигнала. Обычно:
- 15. Современное оборудование
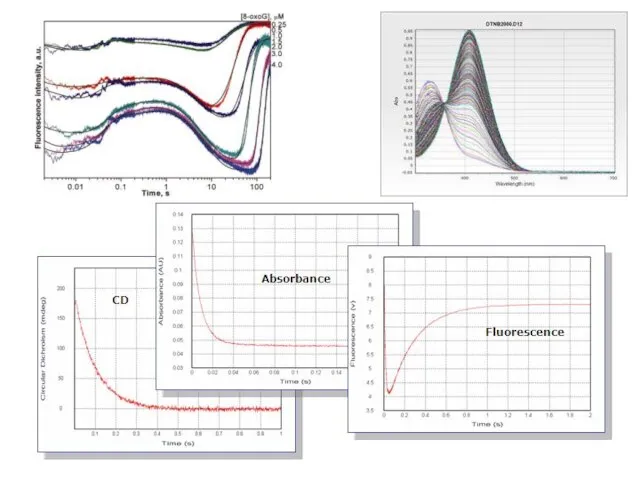
- 16. Детекторы UV/Vis поглощение PDA – весь спектр за один скан Изменение флуоресценции (флуорофоры белков/введённые флуорофоры в
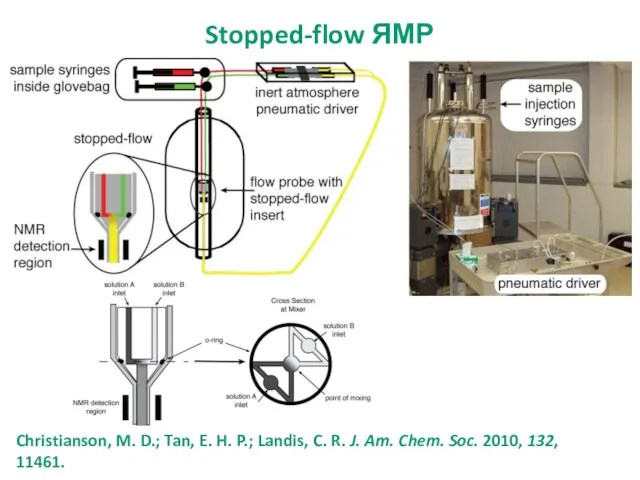
- 18. Stopped-flow ЯМР NMR is the most information-rich type of spectroscopy Hand-mixing of reagents –useful to get
- 19. Christianson, M. D.; Tan, E. H. P.; Landis, C. R. J. Am. Chem. Soc. 2010, 132,
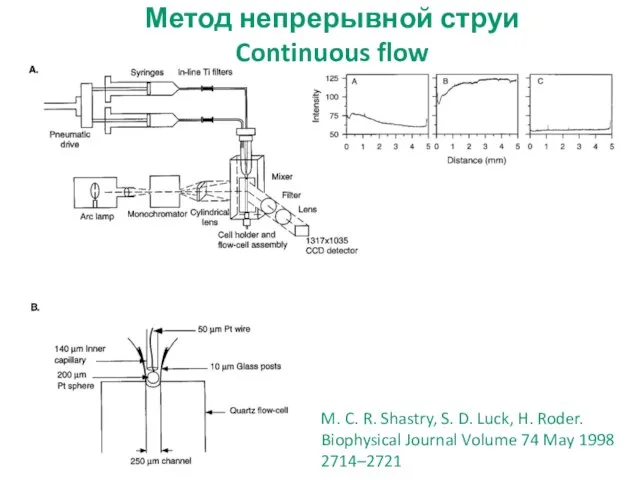
- 20. M. C. R. Shastry, S. D. Luck, H. Roder. Biophysical Journal Volume 74 May 1998 2714–2721
- 21. UV/Vis поглощение Изменения в ИК-спектрах Изменение оптического спектра Изменения в спектрах КД ЯМР и ЭПР-спектрометры Детекторы
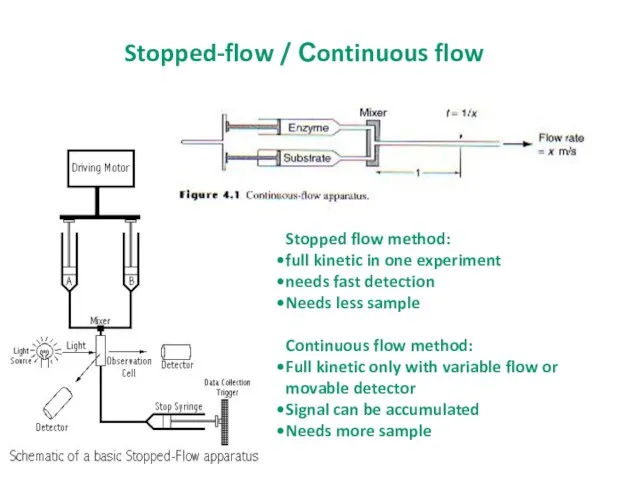
- 22. Stopped flow method: full kinetic in one experiment needs fast detection Needs less sample Continuous flow
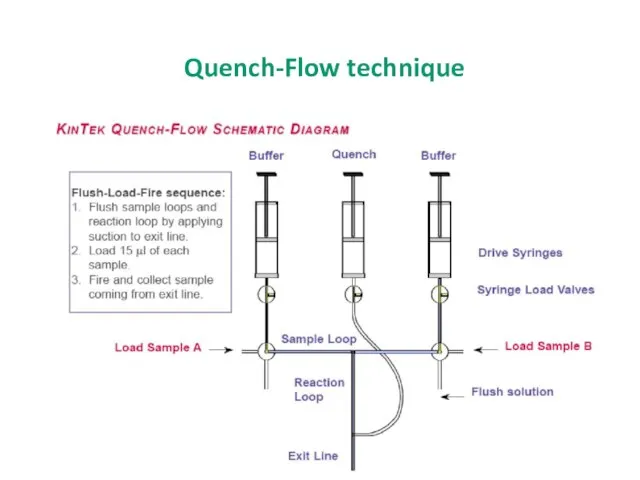
- 23. Quench-Flow technique
- 25. Остановка реакции Хаотропные агенты Детергенты Стоп-аналоги субстратов Щёлочи/кислоты Высокие концентрации немеченых субстратов
- 26. Последующий анализ продуктов Жидкостная хроматография + MS Электрофорез РСА ЯМР/ЭПР
- 27. Fast freeze quench
- 28. ЯМР и ЭПР-спектроскопия UV-Vis-, ИК- спектроскопия в «стёклах» XAFS Анализ промежуточных продуктов после Fast freeze quench
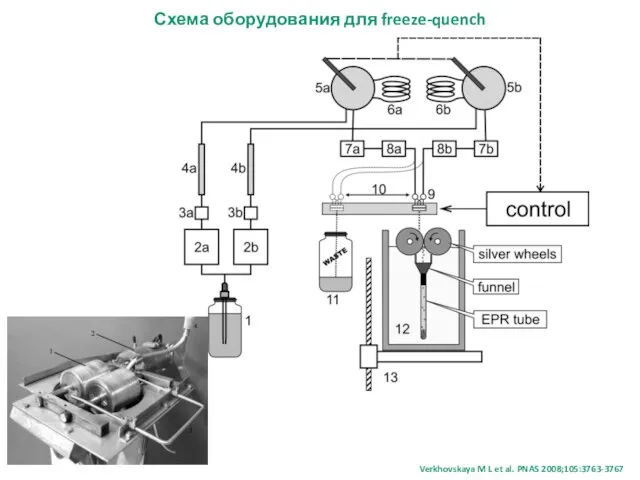
- 29. Схема оборудования для freeze-quench Verkhovskaya M L et al. PNAS 2008;105:3763-3767
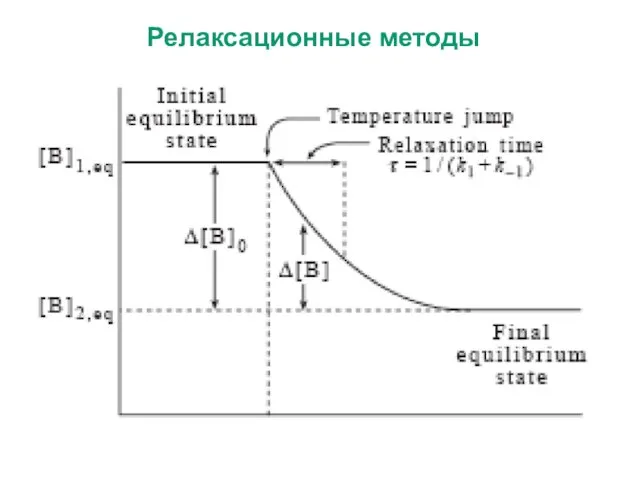
- 30. Релаксационные методы
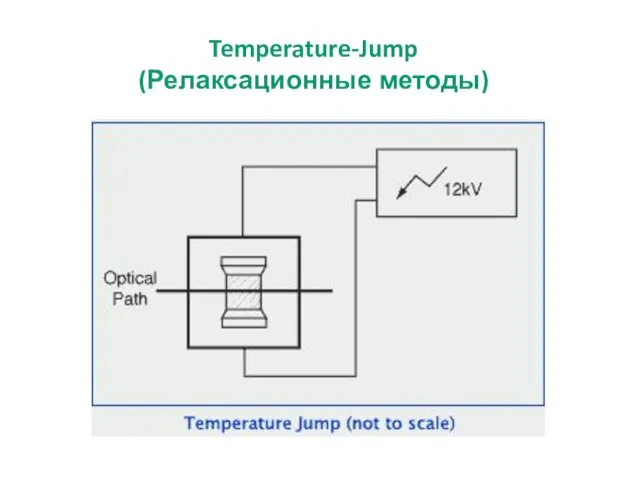
- 31. Temperature-Jump (Релаксационные методы)
- 32. Аппаратура для Temperature-Jump
- 33. Метод T-Jump позволяет регистрировать ход быстрых реакций со временем полупревращения порядка нескольких микросекунд. Реакционную смесь поддерживают
- 34. Temperature Dependence of Reaction Rates Svante Arrhenius observed that reaction rate constants had a temperature dependence
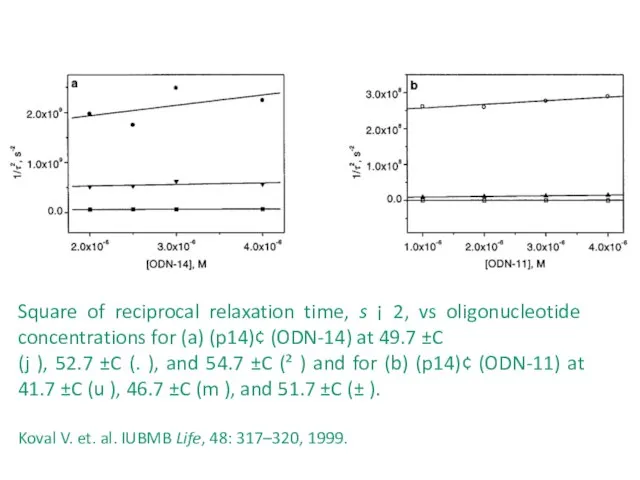
- 35. Square of reciprocal relaxation time, s ¡ 2, vs oligonucleotide concentrations for (a) (p14)¢ (ODN-14) at
- 36. Pressure-jump (Релаксационные методы) Скачок давления - метод, используемый в исследовании химической кинетики. Она включает в себя
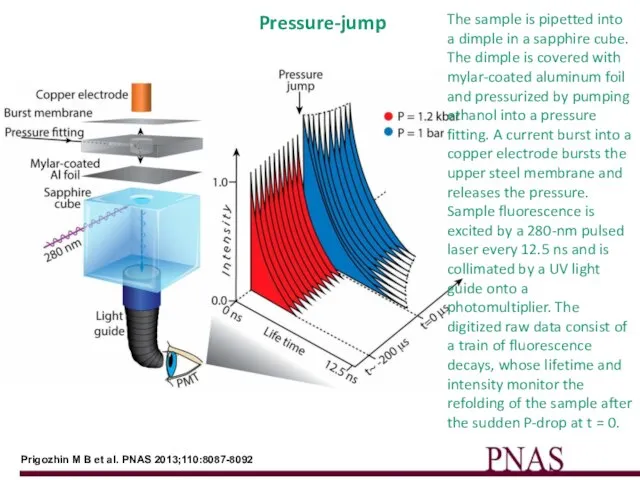
- 37. Prigozhin M B et al. PNAS 2013;110:8087-8092 Pressure-jump The sample is pipetted into a dimple in
- 38. Laser Flash Photolysis
- 39. Лазерный импульсный фотолиз является одной из самых эффективных для исследования путем прямых измерений быстропротекающих химических и
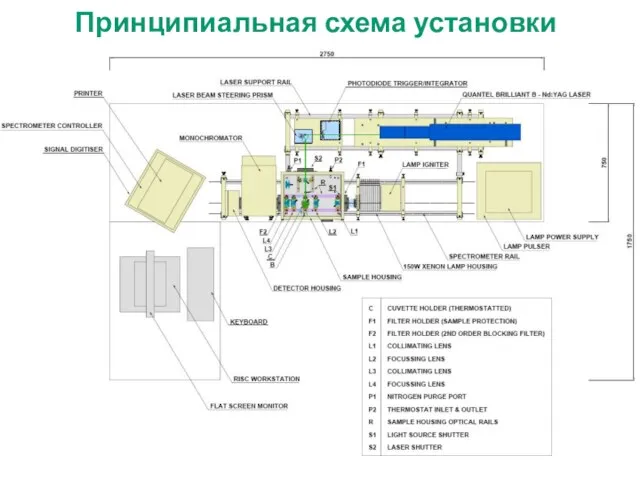
- 40. Принципиальная схема установки для laser flash photolysis
- 42. Скачать презентацию
























 Электрический ток
Электрический ток Капитальный ремонт общего имущества многоквартирного дома за счет субсидий по 185-ФЗ от 21.07.2007 (часть 1)
Капитальный ремонт общего имущества многоквартирного дома за счет субсидий по 185-ФЗ от 21.07.2007 (часть 1) Слепокурова Лилия Григорьевна
Слепокурова Лилия Григорьевна Планирование производственной программы
Планирование производственной программы ОСНОВНЫЕ КОМПОНЕНТЫ И УЗЛЫ ЭЛЕКТРОННЫХ УСТРОЙСТВ
ОСНОВНЫЕ КОМПОНЕНТЫ И УЗЛЫ ЭЛЕКТРОННЫХ УСТРОЙСТВ  JUVENILE justice
JUVENILE justice Zajęcia
Zajęcia Зимующие птицы 1 класс
Зимующие птицы 1 класс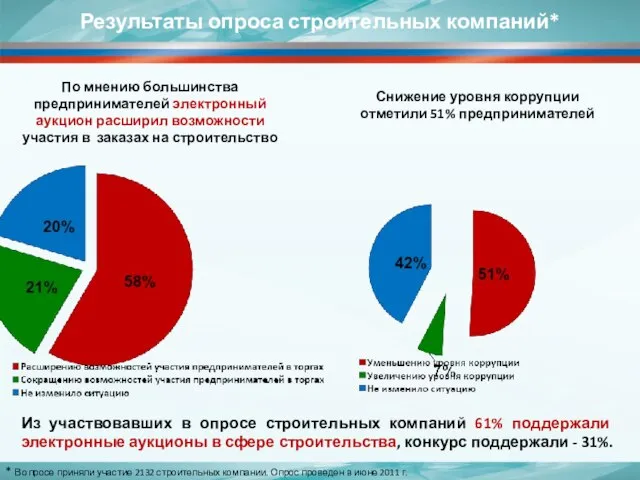 Результаты опроса строительных компаний*
Результаты опроса строительных компаний* Вопросы информационного обеспечения системы ОМС
Вопросы информационного обеспечения системы ОМС Жилой дом, Брюсов переулок
Жилой дом, Брюсов переулок Мировая наркополитика
Мировая наркополитика Презентация на тему Начало создания колониальных империй
Презентация на тему Начало создания колониальных империй  Неделя начальных классов ноябрь 2021
Неделя начальных классов ноябрь 2021 Характеристики современных ПК. Устройства и принцип действие ЭВМ
Характеристики современных ПК. Устройства и принцип действие ЭВМ Презентация на тему Учебные материалы к уроку литературы в 5 классе по рассказу И.С.Тургенева «Муму»
Презентация на тему Учебные материалы к уроку литературы в 5 классе по рассказу И.С.Тургенева «Муму» 1. Универсальная смазка Long-Lub EP заменяет большое количество смазок применяемых, для обслуживания различных узлов: автомобилей, инст
1. Универсальная смазка Long-Lub EP заменяет большое количество смазок применяемых, для обслуживания различных узлов: автомобилей, инст Доктрина снятия корпоративной вуали в зарубежном праве
Доктрина снятия корпоративной вуали в зарубежном праве New food wave
New food wave Вместе против коррупции
Вместе против коррупции Экономика и экономическая наука
Экономика и экономическая наука Основы промышленной автоматизации
Основы промышленной автоматизации  Арифметические действия в двоичной системе счисления
Арифметические действия в двоичной системе счисления Презентация_1
Презентация_1 Сказка в художестве
Сказка в художестве Тема 1
Тема 1 Хабаровский край
Хабаровский край Рекомендации по использованию фирменного стиля Казанского федерального университета при составлении презентации. Шаблон
Рекомендации по использованию фирменного стиля Казанского федерального университета при составлении презентации. Шаблон