Содержание
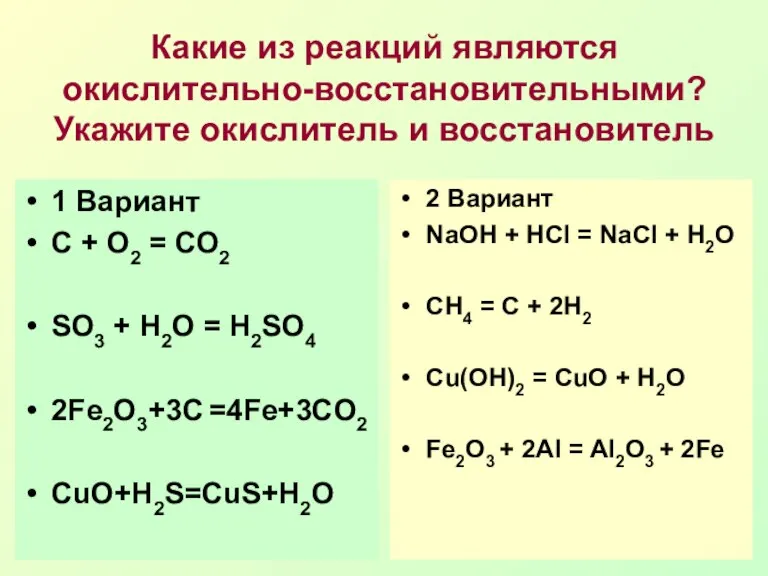
- 2. Какие из реакций являются окислительно-восстановительными? Укажите окислитель и восстановитель 1 Вариант С + О2 = СО2
- 3. 1 Вариант С0 + О20 = С+4О2-2 C0 - 4e = C+4 - ок-ие, в-ль O0
- 4. 2Fe2+3O3+3C0 = Fe0+ C+4O2 C0 - 4e = C+4- ок-ие, в-ль Fe+3 + 3e = Fe0-
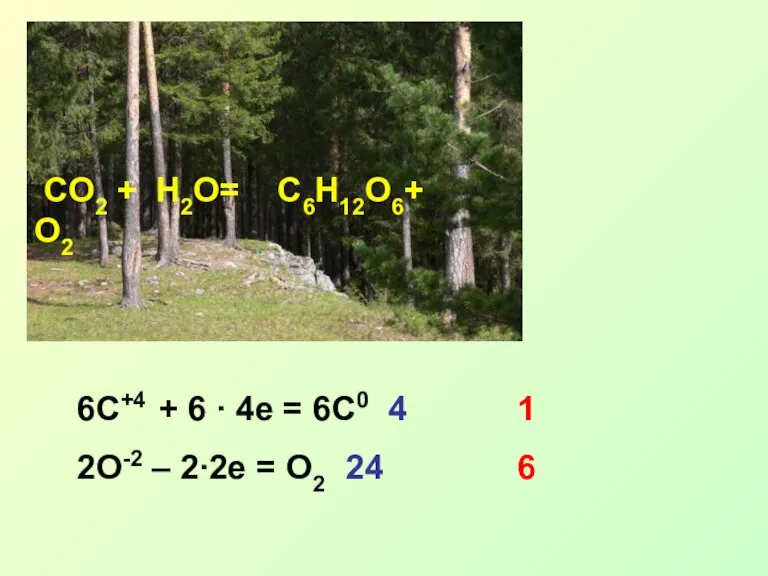
- 5. CO2 + H2O= C6H12O6+ O2 6C+4 + 6 ∙ 4e = 6C0 4 2O-2 – 2∙2e
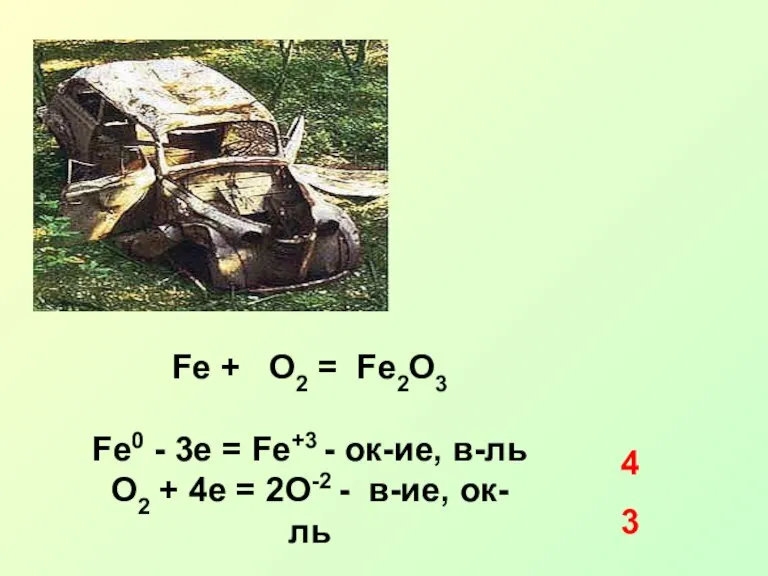
- 6. Fe + O2 = Fe2O3 Fe0 - 3e = Fe+3 - ок-ие, в-ль O2 + 4e
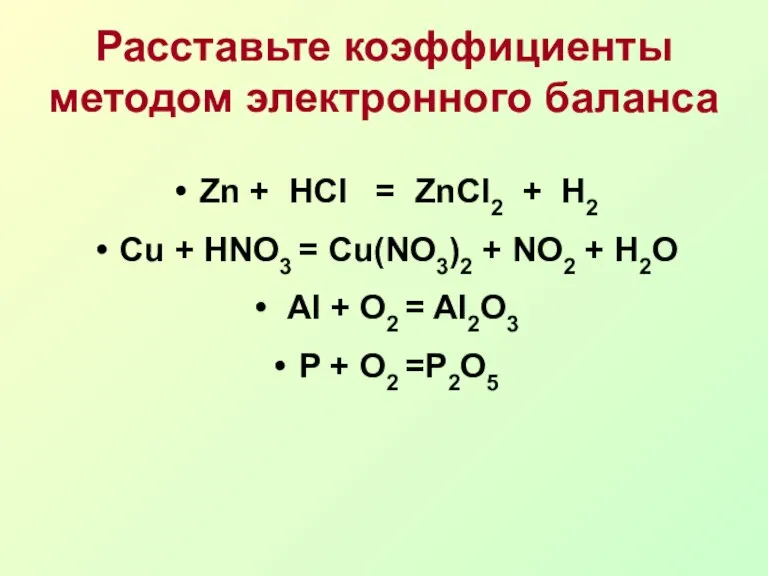
- 7. Расставьте коэффициенты методом электронного баланса Zn + HCl = ZnCl2 + H2 Cu + HNO3 =
- 9. Скачать презентацию


 Навчальний пункт аварійнорятувального загону спеціального призначення Головного управління, місто Рубіжне, Луганська область
Навчальний пункт аварійнорятувального загону спеціального призначення Головного управління, місто Рубіжне, Луганська область 9
9 КОНТЕКСТНАЯ РЕКЛАМА.ПРАКТИЧЕСКИЕ РЕКОМЕНДАЦИИ
КОНТЕКСТНАЯ РЕКЛАМА.ПРАКТИЧЕСКИЕ РЕКОМЕНДАЦИИ АВСТРАЛИЯ
АВСТРАЛИЯ Alpe. Медицинские пластыри
Alpe. Медицинские пластыри День государственного флага Российской Федерации
День государственного флага Российской Федерации К вопросу о Национальной лекарственной политике в России
К вопросу о Национальной лекарственной политике в России Улицы в лицах
Улицы в лицах Замятин
Замятин «Не стыдно не знать,
«Не стыдно не знать, ФИЗИОЛОГИЯ МЫШЦ
ФИЗИОЛОГИЯ МЫШЦ  МОБИЛЬНЫЕ ТЕЛЕФОНЫ SONIM:РЕШЕНИЯ ДЛЯ БИЗНЕСА
МОБИЛЬНЫЕ ТЕЛЕФОНЫ SONIM:РЕШЕНИЯ ДЛЯ БИЗНЕСА Толерантность в школе
Толерантность в школе Группа компаний Стройкомплект
Группа компаний Стройкомплект ОБЪЕДИНЕННАЯ РАБОЧАЯ ГРУППА ПО РЕФОРМИРОВАНИЮ СФЕР ЖКХ, СТРОИТЕЛЬСТВА И ЭНЕРГЕТИКИ
ОБЪЕДИНЕННАЯ РАБОЧАЯ ГРУППА ПО РЕФОРМИРОВАНИЮ СФЕР ЖКХ, СТРОИТЕЛЬСТВА И ЭНЕРГЕТИКИ Буква ю
Буква ю Презентация на тему Колумбия
Презентация на тему Колумбия Презентация на тему Вавилонский царь Хаммурапи и его законы
Презентация на тему Вавилонский царь Хаммурапи и его законы  Презентация на тему Полные квадратные уравнения (общая формула)
Презентация на тему Полные квадратные уравнения (общая формула)  Сущность и функции денег
Сущность и функции денег Раскадровка Презентации телеканала Семерка
Раскадровка Презентации телеканала Семерка Urok_15_Skazka_Fontan_kotory_umel_plavat
Urok_15_Skazka_Fontan_kotory_umel_plavat Итоги заседания общего собрания РАО 17.05.2018
Итоги заседания общего собрания РАО 17.05.2018 Международное право. Международно-правовые средства разрешения споров
Международное право. Международно-правовые средства разрешения споров «Вся гордость мира – от матери!»
«Вся гордость мира – от матери!» Педагогическая родословная моей семьи
Педагогическая родословная моей семьи Презентация на тему омонимы 3 класс
Презентация на тему омонимы 3 класс  Детская организация Тенгрин герл
Детская организация Тенгрин герл