Слайд 2Быть может, эти электроны-
Миры, где пять материков,
Искусства, званья, войны, троны
И память сорока

веков.
Еще, быть может, каждый атом-
Вселенная, где сто планет;
Там всё, что здесь, в объёме сжатом,
Но также то, чего здесь нет.
В. Брюсов «Мир электрона»
Слайд 3Самойленко
Марина
Тьеровна
Учитель химии,
Биологии.
Анучинский район,
С. Гражданка
МОУ СОШ № 12.

Слайд 4СОДЕРЖАНИЕ
Цели урока
Атом-сложная нейтральная частица
Основные характеристики элементарных частиц
Орбитали электрона
S-орбиталь
P-орбиталь
Закрепление материала

Слайд 5Цели урока
Сформировать знания в области строения атома
Развитие памяти,мышления
Умение работать в коллективе

Слайд 6 Атом – сложная нейтральная
частица
Понятие атом возникло еще
в античном мире для обозна-чения

частиц вещества.
В переводе с греческого атом
означает «неделимый».
Атом любого химического
элемента-как бы крохотная
Солнечная система.
Слайд 7Основные характеристики элементарных частиц

Слайд 8О Р Б И Т А Л И
Орбитали могут иметь разную форму.
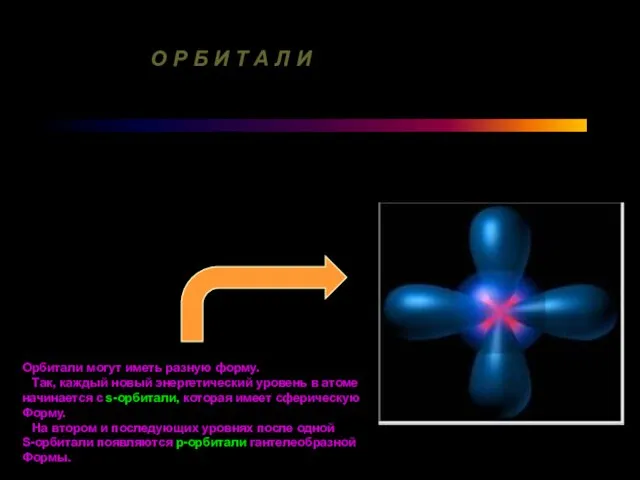
Так, каждый новый энергетический уровень в атоме
начинается с s-орбитали, которая имеет сферическую
Форму.
На втором и последующих уровнях после одной
S-орбитали появляются p-орбитали гантелеобразной
Формы.
Слайд 9ОРБИТАЛЬ ЭЛЕКТРОНА
.
Электроны, двигаясь вокруг
ядра атома, образуют в со-
вокупности его электронную
оболочку. Число

электронов
в оболочке атома равно
числу протонов в ядре
атома и определяется
порядковым или атомным
номером элемента в таблице
Д. И. Менделеева.
Слайд 10Закрепление материала
Дописать предложения.
Вся масса атома сосредоточена в
………., так как массой ……………..
Ничтожно малой,

можно пренебречь.
Заряд ядра атома Z всегда
……………………………………. и
равен числу …………….. в нем.









 Фармацевтический рынок Анализ и прогнозы 2010 – 2012
Фармацевтический рынок Анализ и прогнозы 2010 – 2012 Семейные праздники как одна из форм исторической памяти
Семейные праздники как одна из форм исторической памяти ТЕМА УРОКА:ТЕКСТ И ЕГО СТРУКТУРА
ТЕМА УРОКА:ТЕКСТ И ЕГО СТРУКТУРА Презентация на тему Люби и знай свой родной край. О Красноярском крае
Презентация на тему Люби и знай свой родной край. О Красноярском крае Презентация на тему Сверхпроводимость(11 класс)
Презентация на тему Сверхпроводимость(11 класс) Тест-тренажер: «НРАВСТВЕННОЕ СОЗНАНИЕ» Автор: Назаретьянц Надежда Хачатуровна, педагог-психолог высшей квалификационной категор
Тест-тренажер: «НРАВСТВЕННОЕ СОЗНАНИЕ» Автор: Назаретьянц Надежда Хачатуровна, педагог-психолог высшей квалификационной категор Известняк
Известняк Краевой конкурс «Лучший совместный урок - 2011»
Краевой конкурс «Лучший совместный урок - 2011» Диагностика компании перед слияние
Диагностика компании перед слияние Дидактические основы межпредметных связей в предметном обучении
Дидактические основы межпредметных связей в предметном обучении Матросов Александр
Матросов Александр Социальные, управленческие, экологические и экономические аспекты развития человека в условиях Крайнего Севера. Шаблон
Социальные, управленческие, экологические и экономические аспекты развития человека в условиях Крайнего Севера. Шаблон Узорочья Севера
Узорочья Севера ВКР: Разработка технологического процесса изготовления днищевой секции ледокола
ВКР: Разработка технологического процесса изготовления днищевой секции ледокола Безопасная дорога
Безопасная дорога , = (1 класс)">Равенства. Неравенства. Знаки
, = (1 класс)">Равенства. Неравенства. Знаки Шарады, метаграммы и логогрифы
Шарады, метаграммы и логогрифы Медиаразмещенияв Украине
Медиаразмещенияв Украине Путешествие в удивительный мир окаменелостей
Путешествие в удивительный мир окаменелостей Рекомендации по подбору
Рекомендации по подбору Динамика
Динамика Структурные схемы устройств преобразования энергии первичных источников в электрическую. (Лекция 5)
Структурные схемы устройств преобразования энергии первичных источников в электрическую. (Лекция 5) Кто такой герой
Кто такой герой Актуальные направления сферы дополнительного образования детей в Республике Коми: итоги, перспективы и новые возможности
Актуальные направления сферы дополнительного образования детей в Республике Коми: итоги, перспективы и новые возможности Моя семья. Рисунок
Моя семья. Рисунок Право в системе социальных норм
Право в системе социальных норм ЛЕГКАЯ АТЛЕТИКА
ЛЕГКАЯ АТЛЕТИКА ПЕДАГОГИЧЕСКИЙ ФОРУМ(школа повышения квалификации)
ПЕДАГОГИЧЕСКИЙ ФОРУМ(школа повышения квалификации)