Содержание
- 2. Задачи урока: Изучить состав и классификацию кислот Дать начальные сведения о кислотах
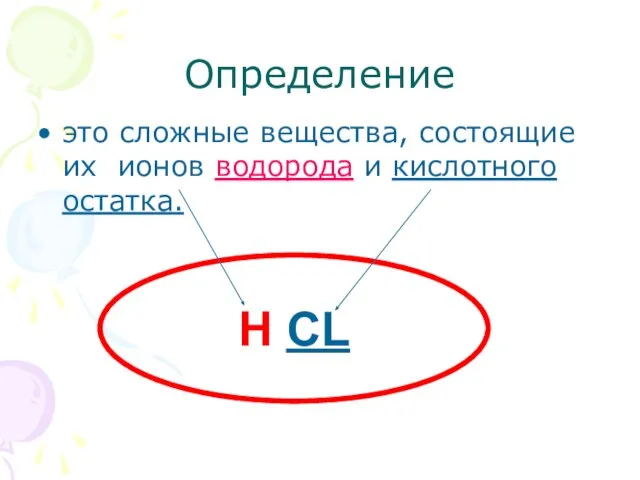
- 3. Определение это сложные вещества, состоящие их ионов водорода и кислотного остатка. Н CL
- 4. Названия распространенных кислот HCl - хлороводородная (соляная) HF - фтороводородная (плавиковая) HBr - бромоводородная HI -
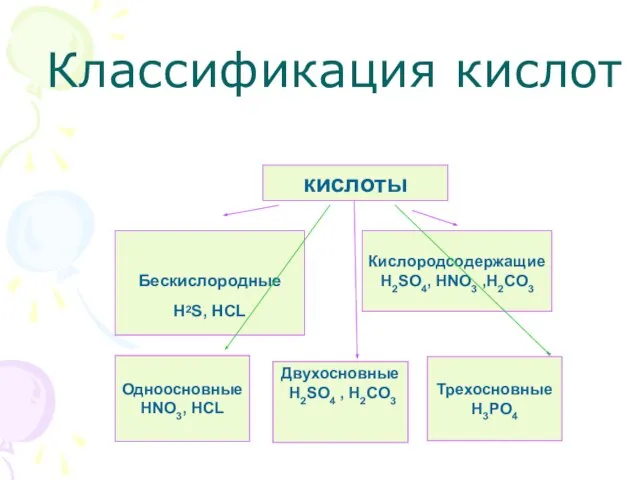
- 5. Классификация кислот
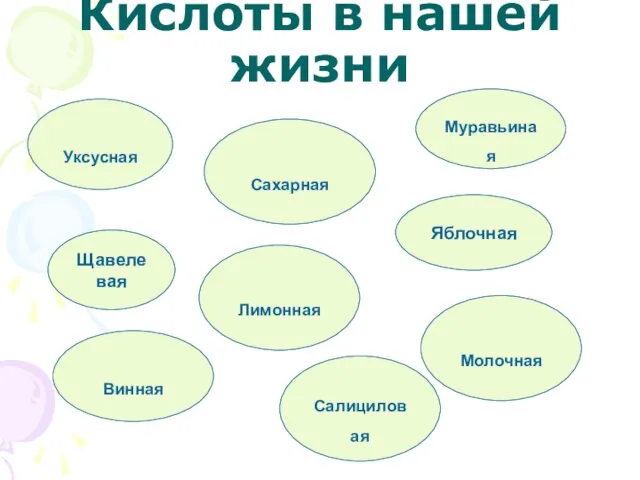
- 6. Кислоты в нашей жизни Муравьиная Щавелевая Яблочная Уксусная Сахарная Лимонная Молочная Винная Салициловая
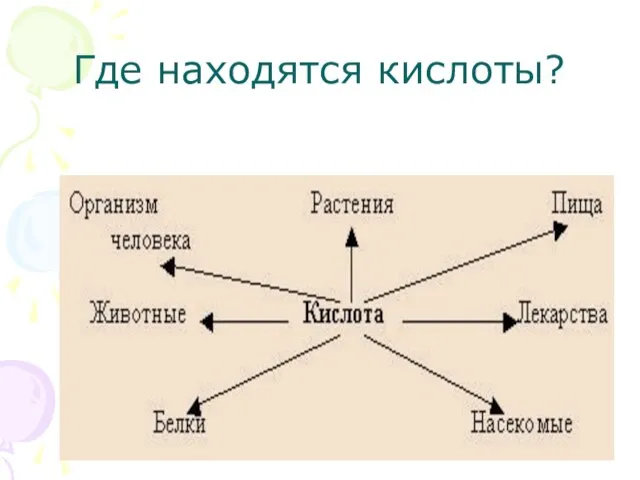
- 7. Где находятся кислоты?
- 8. H2SO4 -серная кислота тяжелая маслянистая жидкость, сильный окислитель, электролит. Издавна её называют «матерью всех кислот», «Купоросное
- 9. Разбавление серной кислоты водой С давних пор существует строгое правило: «Сначала вода, потом кислота, иначе случится
- 10. Алхимикам удалось получить серную кислоту еще в X веке при прокаливании солей - сульфатов (купоросов). Отсюда
- 11. Самые важные кислоты HNO3 -азотная кислота Бесцветная летучая жидкость с резким запахом, дымит на воздухе, сильный
- 12. Самые важные кислоты HCl – соляная (хлороводородная кислота) Соляная кислота входит в состав желудочного сока В
- 13. Биологическая роль соляной кислоты Соляная кислота - сильный бактерицид. Большинство бактерий, попавших в желудок с пищей,
- 14. Уксусная кислота - самая древняя . Упоминания о ней содержатся в древнейших рукописях. Впервые она получена
- 15. Самые важные кислоты HF – Фтороводородная кислота (плавиковая) Плавиковая кислота обладает оригинальными свойствами: она легко реагирует
- 16. Кислоты в природе Кислоты постоянно присутствуют вокруг нас. Например, дождевая вода на первый взгляд кажется чистой.
- 17. Кислоты в организме человека Аскорбиновая, фолиевая, оротовая, пангамовая, никотиновая и другие кислоты являются витаминами. Аминокислоты, соединяясь
- 18. Кислоты нашей пище Немало кислот в нашей пище. Фрукты, овощи, молочные продукты, лекарства поставляют целый букет
- 19. Кислоты в животном мире Если вы присядете вблизи муравейника, то надолго запомните жгучие укусы его обитателей.
- 20. Кислоты в растительном мире Многие растения содержат кислоты и используют их как «Химическое оружие» Мухоморы в
- 22. Скачать презентацию















 Игровая зависимость
Игровая зависимость Групповой психоанализ
Групповой психоанализ О РАБОТЕ СЕКЦИИ ПРОМЫШЛЕННОЙ ЭКОЛОГИИ И РАЦИОНАЛЬНОГО ПРИРОДОПОЛЬЗОВАНИЯ ПО ВОПРОСАМ ВОДОПОЛЬЗОВАНИЯ В ОРЕНБУРГСКОЙ ОБЛАСТИ
О РАБОТЕ СЕКЦИИ ПРОМЫШЛЕННОЙ ЭКОЛОГИИ И РАЦИОНАЛЬНОГО ПРИРОДОПОЛЬЗОВАНИЯ ПО ВОПРОСАМ ВОДОПОЛЬЗОВАНИЯ В ОРЕНБУРГСКОЙ ОБЛАСТИ Animals in the ABC
Animals in the ABC План реализации проекта
План реализации проекта Константин Симонов
Константин Симонов Презентация на тему Малые тела солнечной системы
Презентация на тему Малые тела солнечной системы Заповеди любви
Заповеди любви Вальдорфская школа
Вальдорфская школа Во что верят люди? Религия. Тема №2
Во что верят люди? Религия. Тема №2 Тициан. Жизнь и творчество.. Жизнь Тициана: Жизнь Тициана:ТИЦИАН (1476/77 –1576), венецианский живописец эпохи Возрождения. Родился в гор
Тициан. Жизнь и творчество.. Жизнь Тициана: Жизнь Тициана:ТИЦИАН (1476/77 –1576), венецианский живописец эпохи Возрождения. Родился в гор Йо-йо
Йо-йо Привет, Весна!
Привет, Весна! Совместная маркетинговая программа «Сервис Плюс» для партнеров
Совместная маркетинговая программа «Сервис Плюс» для партнеров Кровотечения. Первая медицинская помощь
Кровотечения. Первая медицинская помощь Предпрофильная подготовка
Предпрофильная подготовка Проект: Юный проповедник 2017
Проект: Юный проповедник 2017 Металлургический комплекс России
Металлургический комплекс России Право + Защита прав людей, живущих с ВИЧ
Право + Защита прав людей, живущих с ВИЧ Грин стар
Грин стар Грамматика со смешариками
Грамматика со смешариками Эпоха ХХ века - эра великих людей и изобретений
Эпоха ХХ века - эра великих людей и изобретений Презентация на тему Исторический обзор садово-паркового искусства
Презентация на тему Исторический обзор садово-паркового искусства Авиация Советского Союза
Авиация Советского Союза Элетронная таблица Excel
Элетронная таблица Excel Гороскоп первоклассника
Гороскоп первоклассника Модели смертности
Модели смертности «Государственно-частное партнерство: региональный аспект»
«Государственно-частное партнерство: региональный аспект»