Слайд 2Закон сохранения энергии
Энергия не возникает из ничего и не исчезает бесследно, а

только переходит из одного состояния в другое.
Энергия объекта складывается из: кинетической, потенциальной, внутренней.
Какой вид энергии важен при рассмотрении химической реакции?
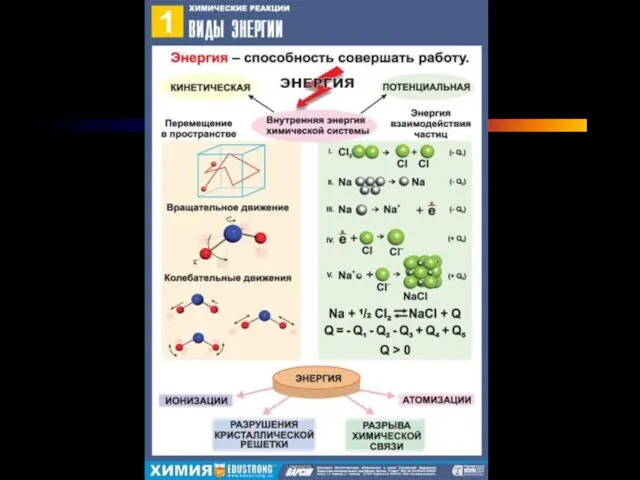
Слайд 3Внутренняя энергия Е:
кинетическая энергия движения атомов, молекул, ионов;
энергия взаимного притяжения и оттталкивания

атомов, молекул, ионов;
энергия движения электронов, притяжения их к ядру, взаимного отталкивания электронов и ядер;
внутриядерная энергия.
Слайд 5Вопросы:
Какие реакции называются экзотермическими?
Какие реакции называются эндотермическими?
Что называют тепловым эффектом реакции?
В каких

единицах он измеряется?
Слайд 6Изменяется ли внутренняя энергия системы в ходе химической реакции?
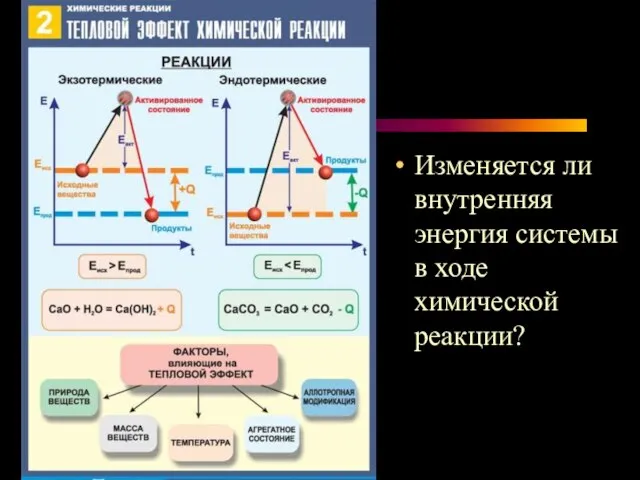
Слайд 7Термохимическое уравнение
- это уравнение химической реакции, в котором указан тепловой эффект в

кДж.
2Н2 + О2 = 2Н2О + 484 кДж
Тепловой эффект – это сумма энергии, затраченной на разрыв химических связей и энергии, которая выделяется при их образовании.
Слайд 8Теплота образования Qобраз
- это тепловой эффект реакции образования одного моля соединения из

простых веществ, устойчивых в стандартных условиях (250С, 1 атм).
Теплота образования простых веществ равна нулю.
Будет ли численно совпадать тепловой эффект реакции и теплота образования?
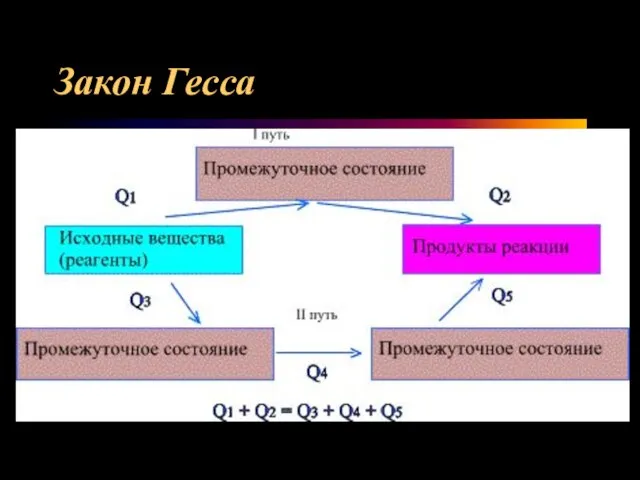
Слайд 10Закон Гесса
Гесс Генрих Иванович – петербургский академик
(1802-1850)

Слайд 12Закон Гесса
Тепловой эффект химической реакции не зависит от промежуточных стадий (при условии,

что исходные вещества и продукты одинаковые.
Тепловой эффект реакции равен сумме Qобраз всех продуктов реакции минус сумма Qобраз всех исходных веществ.
Слайд 13Решение задач
№1-4 на стр.125 базовый уровень.
№ 5-8 на стр. 126 профильный уровень.











 Симметрия и окружающий мир
Симметрия и окружающий мир Готовность к проведению торжественных мероприятий, посвящённых празднованию вручения аттестатов, и выпускных вечеров
Готовность к проведению торжественных мероприятий, посвящённых празднованию вручения аттестатов, и выпускных вечеров Презентация на тему Сульфатредуцирующие бактерии
Презентация на тему Сульфатредуцирующие бактерии  Чехия и чехи
Чехия и чехи ИНТЕЛЛЕКТУАЛЬНАЯ ЛИТЕРАТУРНАЯ ИГРА
ИНТЕЛЛЕКТУАЛЬНАЯ ЛИТЕРАТУРНАЯ ИГРА Применение пиринговой системы электронной наличности для покупок в Премиум магазине wargaming.net
Применение пиринговой системы электронной наличности для покупок в Премиум магазине wargaming.net Лихтенштейн
Лихтенштейн Оценка эффективности инновационной деятельности организации
Оценка эффективности инновационной деятельности организации Australian financial services consulting company (fintech)
Australian financial services consulting company (fintech) Профилактика суицидального поведения у подростков
Профилактика суицидального поведения у подростков Зимние забавы
Зимние забавы Возможности. Взаимодействие родителей и детей по финансовой грамотности. (5)
Возможности. Взаимодействие родителей и детей по финансовой грамотности. (5) Реклама по страницам прочитанных книг
Реклама по страницам прочитанных книг Летняя исследовательская практика школьников
Летняя исследовательская практика школьников Теплые и холодные цвета
Теплые и холодные цвета Понятие и сущность коммуникации
Понятие и сущность коммуникации Как придать лицу параметры более молодого возраста, не делая вредоносных косметологических процедур?
Как придать лицу параметры более молодого возраста, не делая вредоносных косметологических процедур? Психологическое сопровождение учащихся как фактор сохранения психологического здоровья
Психологическое сопровождение учащихся как фактор сохранения психологического здоровья 8 клас Географічні дослідження території України (1)
8 клас Географічні дослідження території України (1) Возможности технологической карты
Возможности технологической карты Презентация на тему Как человек открывал Землю
Презентация на тему Как человек открывал Землю  Информационный проект Молодёжная редакция. Православная молодёжь Томска
Информационный проект Молодёжная редакция. Православная молодёжь Томска 20140204_baobab
20140204_baobab Проблема перевода интернациональных слов с английского языка на русский язык
Проблема перевода интернациональных слов с английского языка на русский язык Фотография и компьютер. 8 класс
Фотография и компьютер. 8 класс ENGLISH GRAMMAR Сильные глаголы
ENGLISH GRAMMAR Сильные глаголы Школы. Планировка. Конструкция
Школы. Планировка. Конструкция СТАТИСТИЧЕСКИЕ ПОКАЗАТЕЛИ И ВЕЛИЧИНЫ
СТАТИСТИЧЕСКИЕ ПОКАЗАТЕЛИ И ВЕЛИЧИНЫ