Содержание
- 2. Уравнение состояния R - универсальная газовая постоянная p=nkT
- 4. уравнение Менделеева -Клапейрона
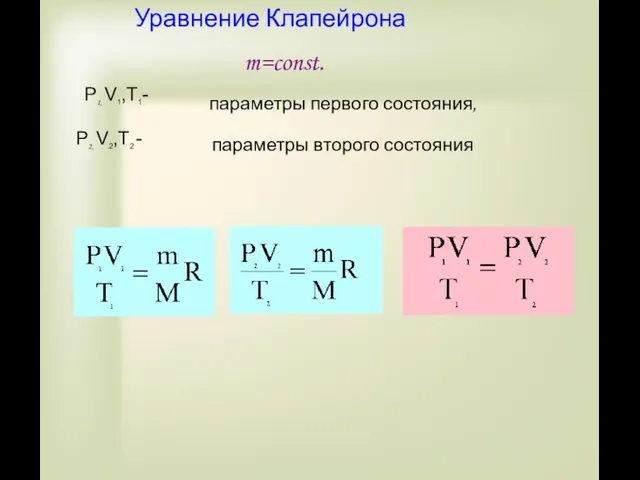
- 5. Уравнение Клапейрона m=const. P1, V1,T1- P2, V2,T2 - параметры первого состояния, параметры второго состояния
- 7. Бенуа Клапейрон Бенуа Поль Эмиль (26.I.1799–28.I.1864) ·Французский химик и физик, член Парижской АН (1858). Окончил Политехническую
- 8. Менделеев Дмитрий(8.II.1834–2.II.1907) Дмитрий Иванович Менделеев родился в феврале 1834 г. в городе Тобольске, в семье директора
- 9. Процессы, протекающие при неизменном значении одного из параметров, называют изопроцессами. Законы, описывающие эти процессы, называют газовыми
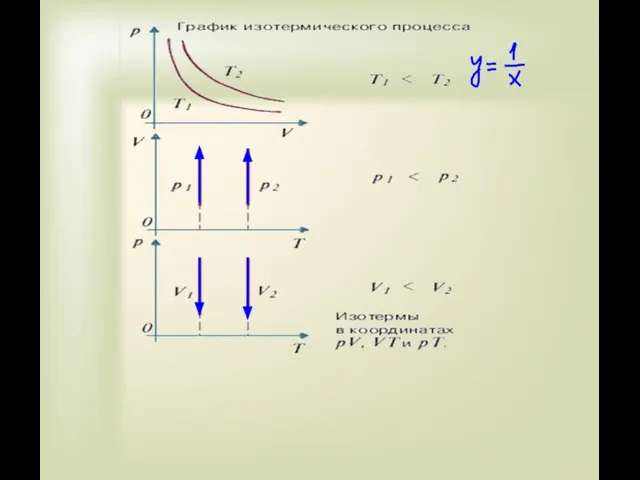
- 10. T=const Изотермический процесс – процесс изменения состояния определенной массы идеального газа при постоянной температуре “термо”(греч.) -
- 11. Давление газа зависит от числа ударов молекул о стенки сосуда . При сжатии газа объем уменьшается,
- 12. Закон Бойля - Мариотта
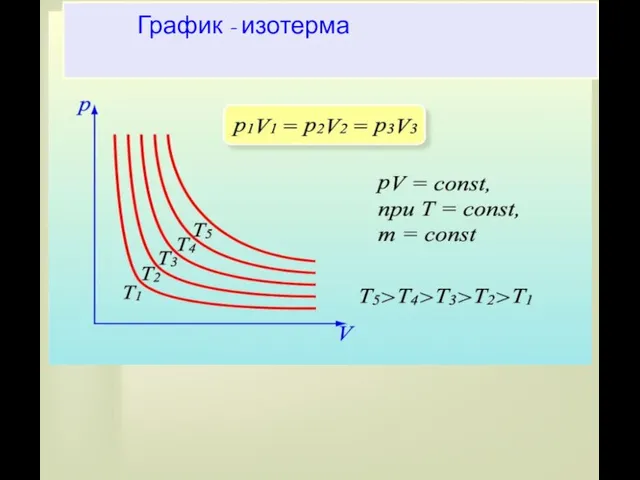
- 13. Закон Бойля - Мариотта Для газа данной массы при постоянной температуре произведение давления газа на его
- 14. График - изотерма
- 16. Роберт Бойль (Boyle) (25.I.1627–30.XII.1691) ·Роберт Бойль, четырнадцатый ребенок графа Корка, родился в его имении в Лисморе,
- 17. Мариотт Эдм.(Mariotte) (1620 - 12.V 1684) ·Французский физик, член Парижской АН со дня её основания (1666).
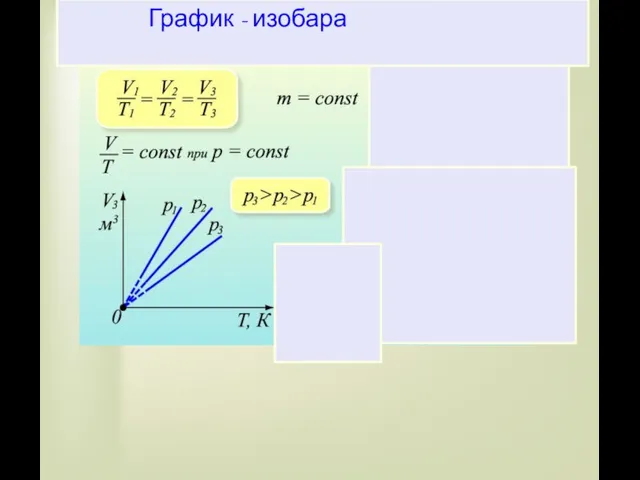
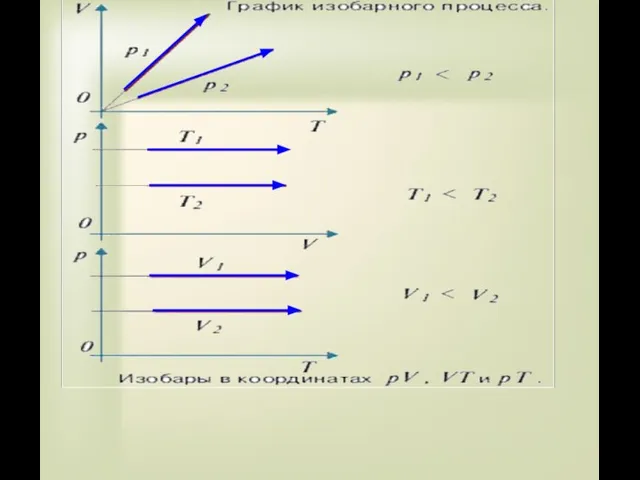
- 18. P=const Изобарный процесс – процесс изменения состояния определенной массы газа при постоянном давлении “барос”(греч.) - давление
- 19. Изобарный процесс При нагревании газ расширяется т.е. его объем увеличивается
- 20. Закон Гей-Люссака
- 21. Для газа данной массы при постоянном давлении отношение объема газа к его температуре постоянно: Закон Гей-Люссака
- 24. Жозеф Гей-Люссак(Gay-Lussac) Жозеф Луи (6.XII.1778–9.V.1850) Французский химик и физик, член АН в Париже (1806). В 1802,
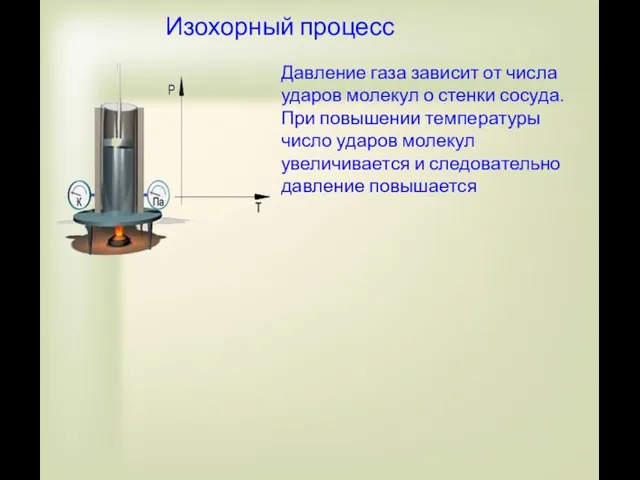
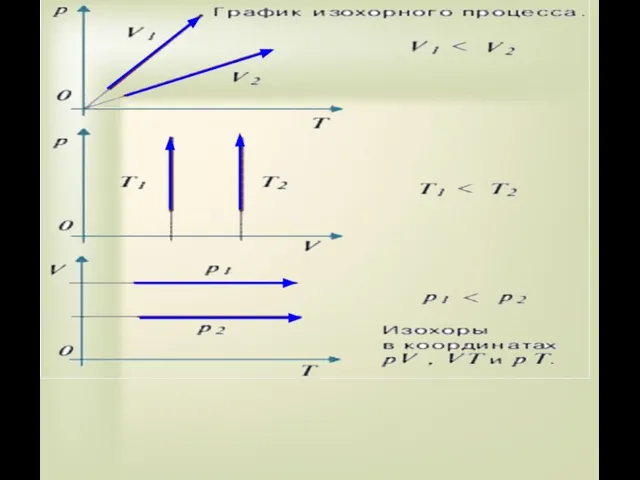
- 25. V=const Изохорный процесс – процесс изменения состояния определенной массы газа при постоянном объеме. “хорос”(греч.) - объем
- 26. Изохорный процесс Давление газа зависит от числа ударов молекул о стенки сосуда. При повышении температуры число
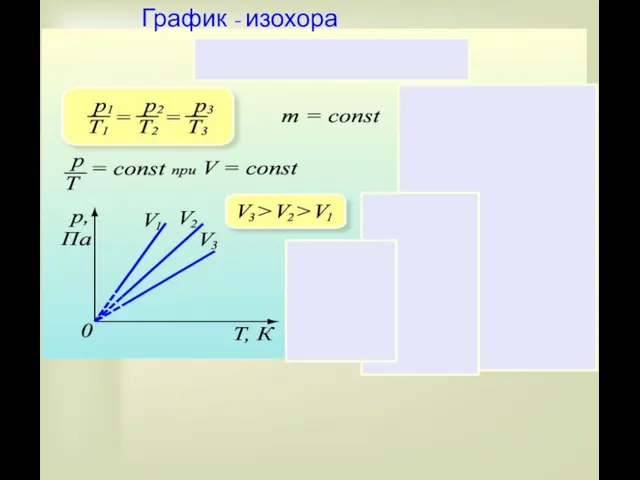
- 27. Закон Шарля
- 28. Закон Шарля Для газа данной массы отношение давления газа к его температуре постоянно:
- 31. ШАРЛЬ, ЖАК АЛЕКСАНДР СЕЗАР (Charles, Jacques-Alexandre-Csar) (1746–1823), ·Французский физик и изобретатель. Родился 12 ноября 1746 в
- 33. Скачать презентацию






















 Государственное регулирование транспортной системы в городе федерального значения Москве
Государственное регулирование транспортной системы в городе федерального значения Москве Хозяин, задание выполнено! Решает ли сайт свои задачи и как повысить его эффективность
Хозяин, задание выполнено! Решает ли сайт свои задачи и как повысить его эффективность Крестовые походы
Крестовые походы Анализ хозяйственной деятельности предприятия
Анализ хозяйственной деятельности предприятия  HAPPY BIRTHDAY MY LOVE!!!
HAPPY BIRTHDAY MY LOVE!!! Разработка графической среды создания сценариев информационных услуг для проекта «Персональный агент»
Разработка графической среды создания сценариев информационных услуг для проекта «Персональный агент» Лекция - Качество кода (1)
Лекция - Качество кода (1) Врачи, Пациенты, Здравоохранение: От Эскулапа и Гиппократа до современности Венедиктов Д.Д. 27.11.2010 г.
Врачи, Пациенты, Здравоохранение: От Эскулапа и Гиппократа до современности Венедиктов Д.Д. 27.11.2010 г. ОРКСЭ. Праздники как одна из форм исторической памяти
ОРКСЭ. Праздники как одна из форм исторической памяти Будущее Ирака после 2003 года и его положение на Ближнем Востоке
Будущее Ирака после 2003 года и его положение на Ближнем Востоке Презентация семинара-практикума
Презентация семинара-практикума Омонимы и омографы
Омонимы и омографы Координация движений. Тест на координацию
Координация движений. Тест на координацию Виват, интеллектуалы школы №6 г. Беслана!
Виват, интеллектуалы школы №6 г. Беслана! дыхание
дыхание Удивительные числа
Удивительные числа Жизнь Акакия Акакиевича до и после появления новой шинели
Жизнь Акакия Акакиевича до и после появления новой шинели Презентация образовательного учреждения
Презентация образовательного учреждения Военные страницы истории моей семьи
Военные страницы истории моей семьи Центр комплексної реабілітації для дітей з інвалідністю Пролісок
Центр комплексної реабілітації для дітей з інвалідністю Пролісок Die Bayer Aktiengesellschaft (Bayer AG) ist die Holding-Gesellschaft des Bayer- Konzerns
Die Bayer Aktiengesellschaft (Bayer AG) ist die Holding-Gesellschaft des Bayer- Konzerns Управление электронной подпиской в Белорусском национальном техническом университете Скалабан А.В. директор Научной библиотеки
Управление электронной подпиской в Белорусском национальном техническом университете Скалабан А.В. директор Научной библиотеки  Презентация на тему Взаимоотношения между организмами
Презентация на тему Взаимоотношения между организмами государство
государство Gracia ceramica
Gracia ceramica ВОДА В ПРИРОДЕ
ВОДА В ПРИРОДЕ Культура управлять. Онлайн-программа по формированию управленческой культуры начинающих руководителей ОАО РЖД
Культура управлять. Онлайн-программа по формированию управленческой культуры начинающих руководителей ОАО РЖД Научно- образовательный центр "Нейробиологическая диагностика детей и подростков"
Научно- образовательный центр "Нейробиологическая диагностика детей и подростков"