Содержание
- 2. Открытие фосфора Гамбургский алхимик Хеннинг Бранд 1669 год «Фосфор» - от греческого «светоносный»
- 3. Фосфор – простое вещество. 1.Химическая формула – Р. 2.Mr(Р) =31 3. М (Р) = 31г/моль 4.
- 4. Фосфин – фосфористый водород, ядовитый газ с чесночным запахом, легко воспламеняется на воздухе. Поэтому огни на
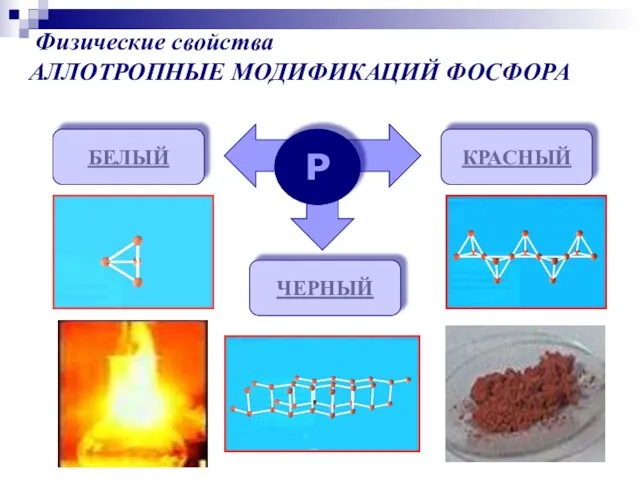
- 5. Р БЕЛЫЙ КРАСНЫЙ ЧЕРНЫЙ Физические свойства АЛЛОТРОПНЫЕ МОДИФИКАЦИЙ ФОСФОРА
- 6. с бертолетовой солью при ударе взрывается, воспламеняется: KClO3 + P = P2O5 + KCl
- 7. Продукты, содержащие фосфор Бобовые (горох, фасоль) Кукуруза; Дрожжи; Сыр; Отруби; Молоко (цельное и сгущенное) Молочные продукты;
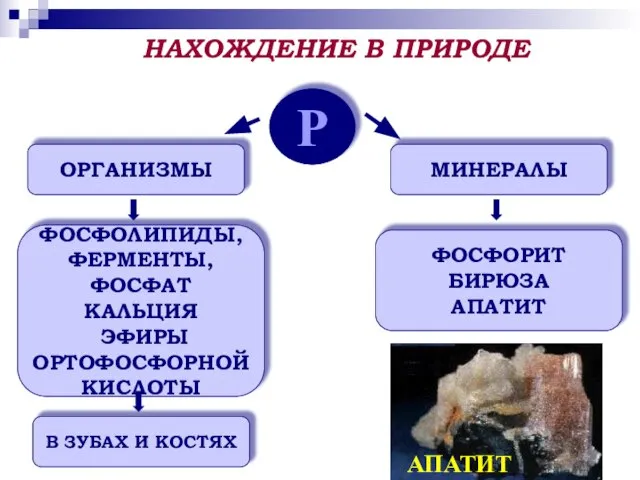
- 8. Р ОРГАНИЗМЫ МИНЕРАЛЫ ФОСФОЛИПИДЫ, ФЕРМЕНТЫ, ФОСФАТ КАЛЬЦИЯ ЭФИРЫ ОРТОФОСФОРНОЙ КИСЛОТЫ В ЗУБАХ И КОСТЯХ ФОСФОРИТ БИРЮЗА
- 9. Физиологическое действие белого фосфора Результат применения чрезмерного количества фосфора Появление лягушек с уродствами -результат применения фосфорных
- 10. Суточная потребность в фосфоре Суточной нормой фосфора для взрослого человека считают 1600 мг, потребность у беременных
- 11. Соединения фосфора. Оксид фосфора (V) 1.Р2О5 2. Mr(P2O5) = 142 3. M (P2O5) = 142г/моль 4.
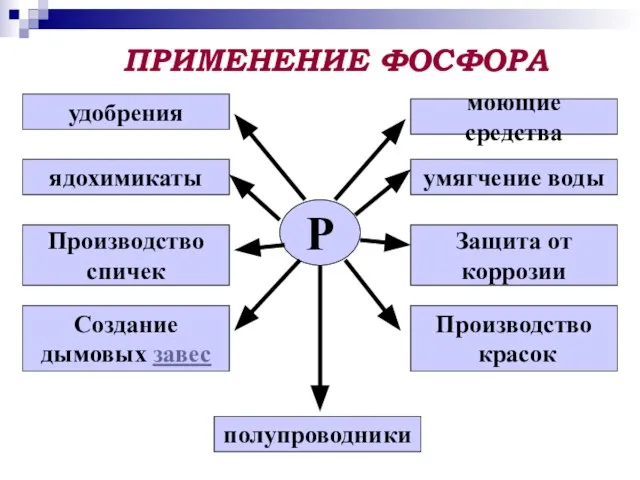
- 12. ПРИМЕНЕНИЕ ФОСФОРА Р удобрения ядохимикаты Производство спичек Создание дымовых завес полупроводники Производство красок Защита от коррозии
- 13. Войска США использовали фосфорные Бомбы в Ираке, 2004 г.
- 14. Молекулы P4 имеют форму тетраэдра. Это легкоплавкое t(пл)=44,1оС, t(кип)=275оС, мягкое, бесцветное воскообразное вещество. Хорошо растворяется в
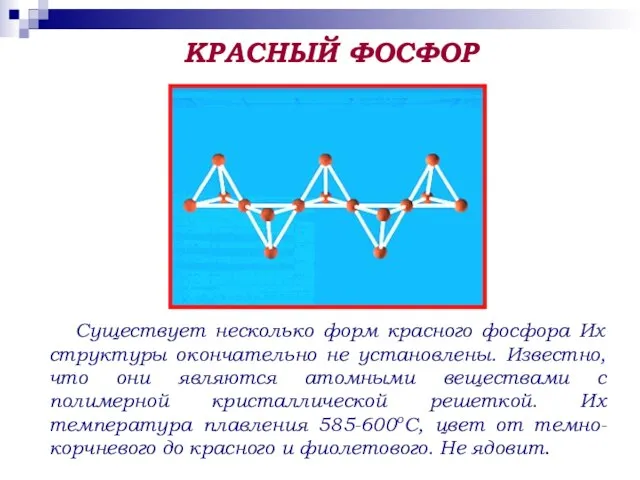
- 15. Существует несколько форм красного фосфора Их структуры окончательно не установлены. Известно, что они являются атомными веществами
- 17. Скачать презентацию










 Распутин Валентин Григорьевич
Распутин Валентин Григорьевич Спортивные игры. Баскетбол
Спортивные игры. Баскетбол Танковый пулемёт ДТ-29
Танковый пулемёт ДТ-29 финансовый контроль1
финансовый контроль1 Звезды на небе
Звезды на небе Занятие по обществознанию на тему: «Политические партии» Для студентов 1 курса СПО
Занятие по обществознанию на тему: «Политические партии» Для студентов 1 курса СПО Презентация на тему Ассирийская держава Древний мир
Презентация на тему Ассирийская держава Древний мир  Аэрация зданий
Аэрация зданий Город Бийск – город доброжелательный детям
Город Бийск – город доброжелательный детям Lilia Mikhailovna Shvetskaya
Lilia Mikhailovna Shvetskaya Работа с мышью
Работа с мышью Актуальные задачи развития дошкольного образования как самостоятельного элемента современной модели
Актуальные задачи развития дошкольного образования как самостоятельного элемента современной модели Программирование на языке с++
Программирование на языке с++ Насекомые (1 класс)
Насекомые (1 класс) 4 октября - день гражданской обороны Российской Федерации
4 октября - день гражданской обороны Российской Федерации Автомобилестроение США
Автомобилестроение США Кто хочет идти за Мною, отвергнись себя, и возьми крест свой, и следуй за Мною. (Мк.8.34)
Кто хочет идти за Мною, отвергнись себя, и возьми крест свой, и следуй за Мною. (Мк.8.34) Безопасность детей младшего дошкольного возраста
Безопасность детей младшего дошкольного возраста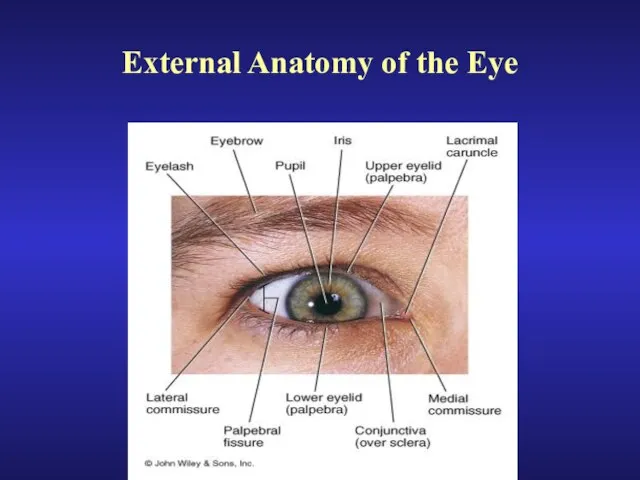 External Anatomy of the Eye
External Anatomy of the Eye Презентация на тему ИСТОРИЧЕСКИЙ ПОРТРЕТ НИКОЛАЯ МИХАЙЛОВИЧА КАРАМЗИНА (1766—1826)
Презентация на тему ИСТОРИЧЕСКИЙ ПОРТРЕТ НИКОЛАЯ МИХАЙЛОВИЧА КАРАМЗИНА (1766—1826)  Здоровыми в XXI век!
Здоровыми в XXI век! Family life in Great Britain
Family life in Great Britain Презентация на тему ФОРМИРОВАНИЕ ПОЗНАВАТЕЛЬНОГО ИНТЕРЕСА К МАТЕМАТИКЕ
Презентация на тему ФОРМИРОВАНИЕ ПОЗНАВАТЕЛЬНОГО ИНТЕРЕСА К МАТЕМАТИКЕ  Компонент 17.Ресурсное обеспечение
Компонент 17.Ресурсное обеспечение Электрические системы управления входными устройствами воздухозаборников реактивных двигателей
Электрические системы управления входными устройствами воздухозаборников реактивных двигателей OLAP ModelKit is a powerful and high-performance OLAP component specially designed to help you reduce your development time and costs while building effective decision support systems.
OLAP ModelKit is a powerful and high-performance OLAP component specially designed to help you reduce your development time and costs while building effective decision support systems. Родничок «Пискун»
Родничок «Пискун» Sotsiologia_Tema_1
Sotsiologia_Tema_1