Слайд 5Особенности элементов металлов
На внешнем уровне ….
…Са + О2 =…СаО
Металлы могут проявлять …..

свойства
3. Металлы проявляют общие физических свойства - …., которые обусловлены …..
4. Металл → …. оксид → ….. гидрокид ( ….)
Слайд 6Определите элемент, ион которого входит в состав поваренной соли:
А) 2е, 8е, 8е,

2е
Б) 2е, 8е, 1е
В) 2е, 8е, 5е
Охарактеризуйте элемент.
Запишите формулы высших оксида и гидроксида,
Запишите уравнения реакций, подтверждающих их характер.
Слайд 7Характеристика элемента-металла на основании его положения в ПС
Д.И. Менделеева
Положение элемента в

Периодической системе.
а) порядковый номер
б) период
в) группа, подгруппа
г) 2.Строение атома и его свойства
а) число протонов, электронов, нейтронов
б) заряд ядра
в) схема строения электронной оболочки
е) окислительно - восстановительные свойства
д) возможные степени окисления
3. Простое вещество
Слайд 8Характеристика высшего оксида и гидроксида
Формула высшего оксида и характер высшего оксида
Уравнения

реакций, подтверждающих характер оксида.
Формула и характер высшего гидроксида.
Уравнения реакций, подтверждающие свойства гидроксида.
Слайд 9Расположите элементы
1) в порядке возрастания металлических свойств: К, Аl, Са
2) в порядке

возрастания металлических свойств: Ca, Ba, Be, Mg
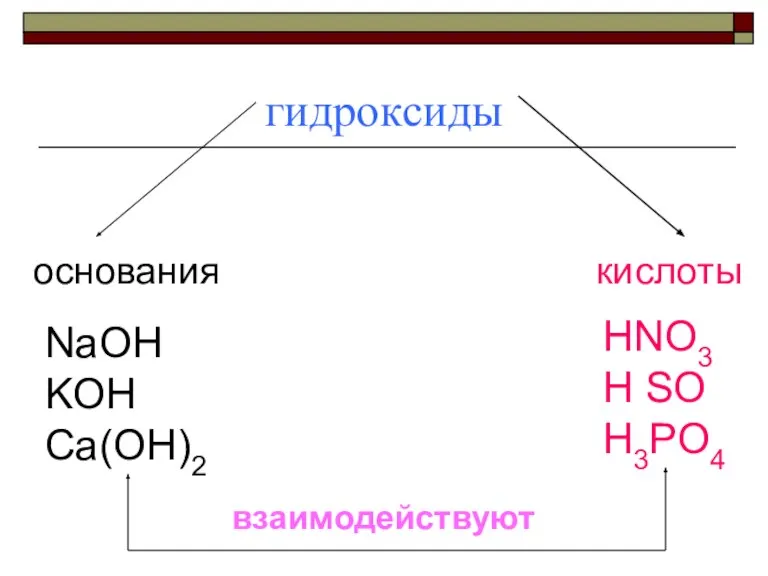
Слайд 10гидроксиды
основания
кислоты
NaOH
KOH
Ca(OH)2
HNO3
H SO
H3PO4
взаимодействуют
Слайд 11Закончите генетический ряд
Li → Li2O → ….. → Li2SO4 → BaSO4
Укажите класс

и название вещества.
Запишите уравнения реакций, подтверждающих характер веществ







 Мозаики Ломоносова М.В.
Мозаики Ломоносова М.В. THE KAZAKHSTAN’S ARCHITECTURE of the Ancientry and the Middle Ages / STYLES OF THE KAZAKHSTAN’S ARCHITECTURE (by K.I.Samoilov)
THE KAZAKHSTAN’S ARCHITECTURE of the Ancientry and the Middle Ages / STYLES OF THE KAZAKHSTAN’S ARCHITECTURE (by K.I.Samoilov) Области педагогики, исследования в которых приобрели особую актуальность в связи с задачами непрерывного образования
Области педагогики, исследования в которых приобрели особую актуальность в связи с задачами непрерывного образования Красота своими руками. Работы бисером
Красота своими руками. Работы бисером Обеспечение практической реализации закона об энергосбережении и о повышении энергетической эффективности
Обеспечение практической реализации закона об энергосбережении и о повышении энергетической эффективности Валютный курс. Факторы и режимы валютного курса
Валютный курс. Факторы и режимы валютного курса Лабораторная работа №4.Тема. Строение зрительного анализатора.Цель: изучить строение органа зрения. Оборудование: ПК, презента
Лабораторная работа №4.Тема. Строение зрительного анализатора.Цель: изучить строение органа зрения. Оборудование: ПК, презента Спорт в моей жизни
Спорт в моей жизни Презентация на тему Характеристика щелочных металлов 9 класс
Презентация на тему Характеристика щелочных металлов 9 класс Презентация на тему Нефтяная промышленность России 9 класс
Презентация на тему Нефтяная промышленность России 9 класс Что такое симметрия
Что такое симметрия Презентация на тему Работа социального педагогам с детьми девиантного поведения
Презентация на тему Работа социального педагогам с детьми девиантного поведения Семейное право. Правовая связь членов семьи
Семейное право. Правовая связь членов семьи Город Зарайск
Город Зарайск Портрет парадный и лирический
Портрет парадный и лирический Правовой статус гражданина РФ
Правовой статус гражданина РФ Презентация на тему Иммануил Кант
Презентация на тему Иммануил Кант PREZENTATsIYa_soglashenie_o_namerenia
PREZENTATsIYa_soglashenie_o_namerenia Глобальные прогнозы
Глобальные прогнозы Презентация на тему: Понятие квадратного корня из неотрицательного числа
Презентация на тему: Понятие квадратного корня из неотрицательного числа Самоконтроль при занятиях физическими упражнениями. Лекция 1
Самоконтроль при занятиях физическими упражнениями. Лекция 1 Б. М. Кустодиев. (1878-1927)
Б. М. Кустодиев. (1878-1927) Жуков Дмитрий - кандидат в председатели комиссии по спортивной работе
Жуков Дмитрий - кандидат в председатели комиссии по спортивной работе «НАШ НОВЫЙ ДЕТСКИЙ САД»
«НАШ НОВЫЙ ДЕТСКИЙ САД» Политика и власть. 10 класс
Политика и власть. 10 класс Русская тема в художественной культуре периода оттепели
Русская тема в художественной культуре периода оттепели Николай Хмеленок. Тренажёры по английскому языку. Расположите по порядку. Части тела
Николай Хмеленок. Тренажёры по английскому языку. Расположите по порядку. Части тела КРИМИНОЛОГИЯ
КРИМИНОЛОГИЯ