Содержание
- 2. ХИМИЯ
- 3. Рождение химии белка… Впервые белок был выделен (в виде клейковины) в 1728 г. итальянцем Якопо Бартоломео
- 4. Жерар Мульдер "Во всех растениях и животных присутствует некое вещество, которое без сомнения является наиболее важным
- 5. Белки, или протеины что происходит от греч. protos — первый, первичный. Одновременно с Мульдером французский химик
- 6. Проблемный вопрос: Можно ли утверждать что: «Нет белка – нет органической жизни на Земле»? Обоснуйте ответ,
- 7. Содержание учебного материала: Аминокислоты: строение молекулы, номенклатура и изомерия, кислотно-основные свойства, значение. Белки: строение молекулы, свойства,
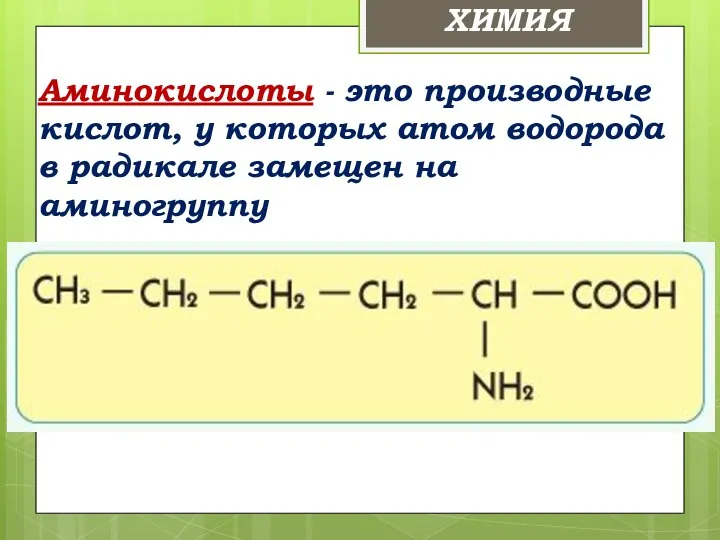
- 8. Аминокислоты - это производные кислот, у которых атом водорода в радикале замещен на аминогруппу ХИМИЯ
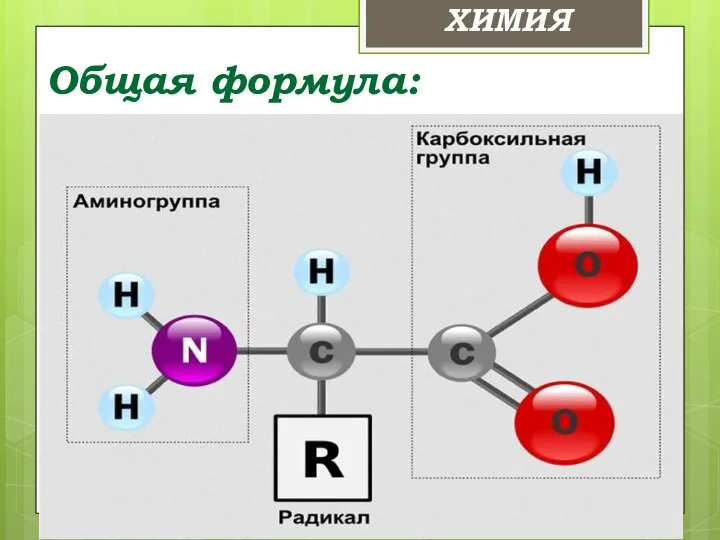
- 9. Общая формула: ХИМИЯ
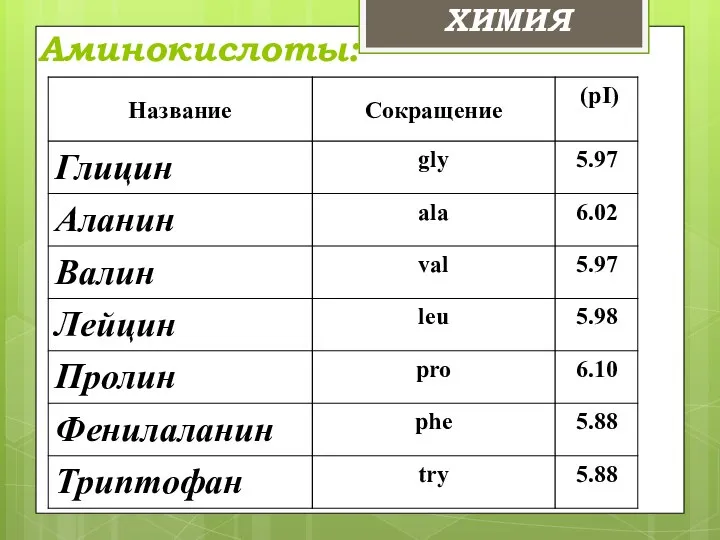
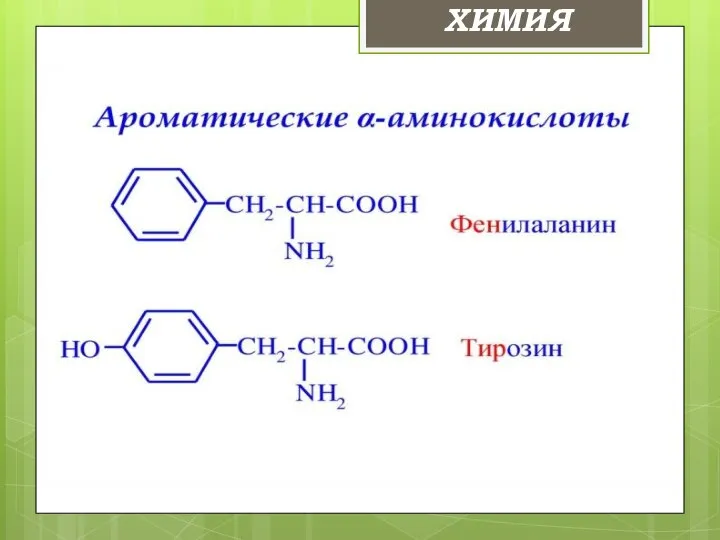
- 11. Аминокислоты: ХИМИЯ
- 12. Классификация аминокислот: 1.По природе радикала : ХИМИЯ
- 13. ХИМИЯ
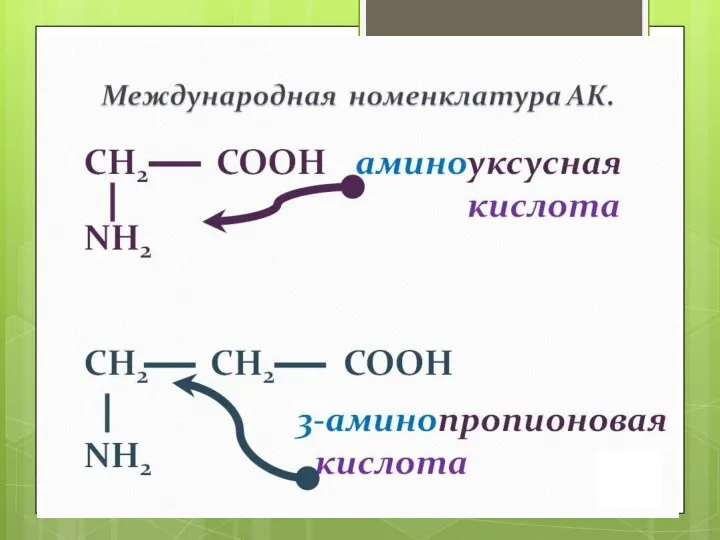
- 14. 2. По взаимному расположению функциональных групп выделяют α-, ß-, γ- и т.д. аминокислоты. ХИМИЯ
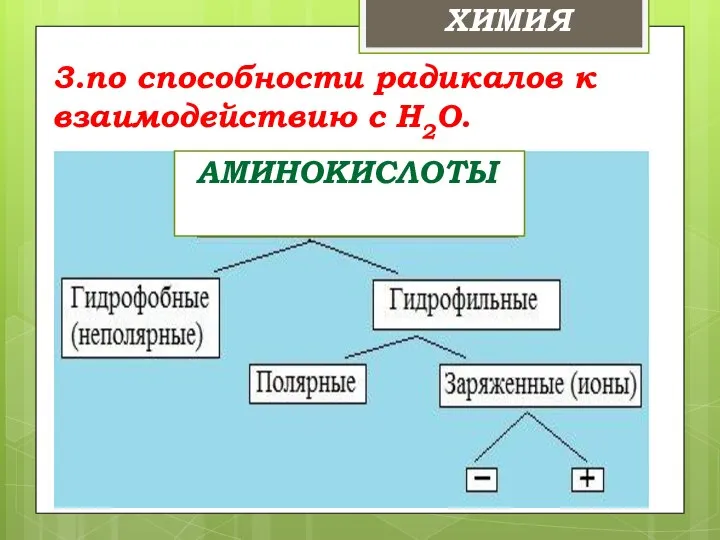
- 15. 3.по способности радикалов к взаимодействию с Н2О. ХИМИЯ АМИНОКИСЛОТЫ АМИНОКИСЛОТЫ
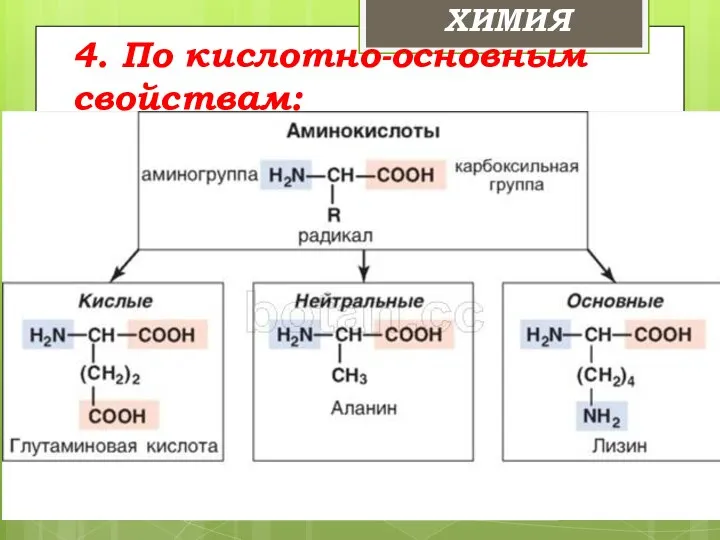
- 16. 4. По кислотно-основным свойствам: ХИМИЯ
- 17. Незаменимые (8) не синте-зируются организмом из других соединений, поэтому должны поступать с пищей. Полузамени-мые – (2)
- 18. ХИМИЯ Изомерия аминокислот Структурная изомерия:
- 19. Оптическая изомерия ХИМИЯ «Зеркало Венеры», 1898
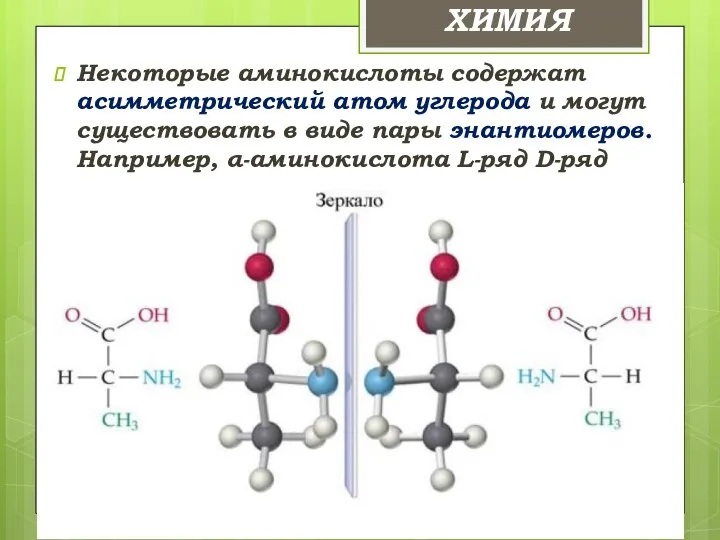
- 20. Некоторые аминокислоты содержат асимметрический атом углерода и могут существовать в виде пары энантиомеров. Например, α-аминокислота L-ряд
- 21. ХИМИЯ
- 22. нелетучие кристаллические вещества высокие температуры плавления нерастворимы в неполярных органических растворителях и растворимы в воде молекулы
- 23. В кристаллическом состоянии существуют в виде внутренних солей, т.е. биполярных ионов: Значение рН, при котором молекула
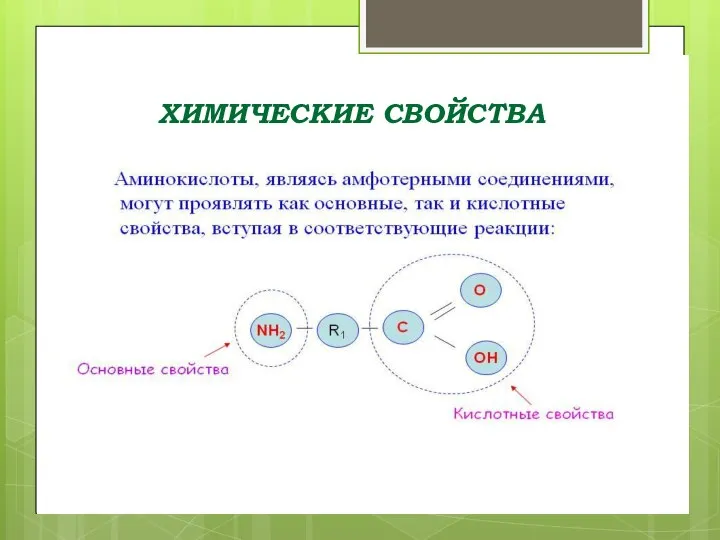
- 24. ХИМИЧЕСКИЕ СВОЙСТВА
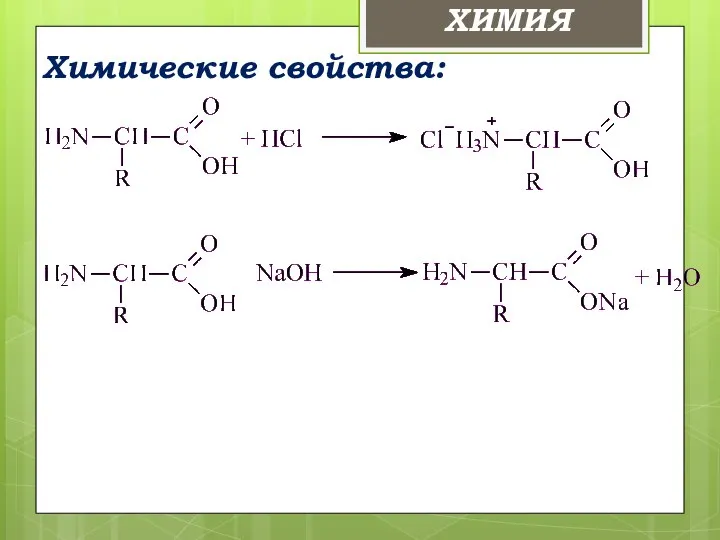
- 25. Химические свойства: ХИМИЯ
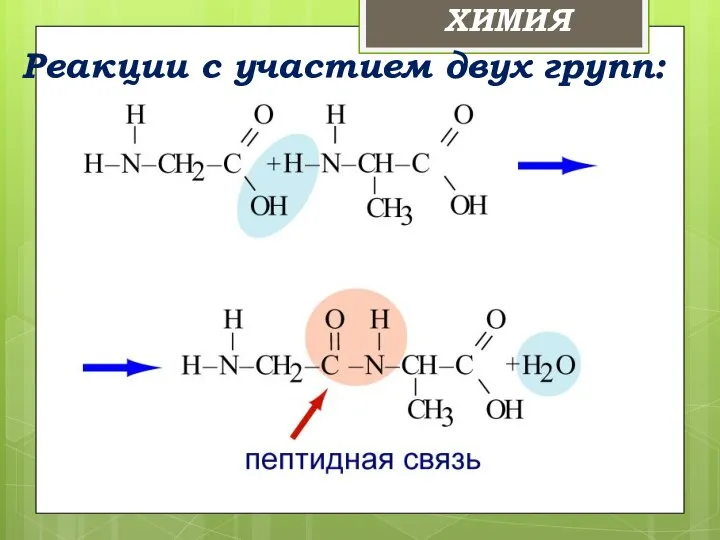
- 26. Реакции с участием двух групп: ХИМИЯ
- 27. Пептиды : - продукты поликонденсации, построенные из α-аминокислот. По числу аминокислотных остатков в молекуле пептида различают
- 29. Белки - сложные высокомолекулярные природные соединения, построенные из остатков α-аминокислот. Аминокислоты в белках связаны пептидными связями.
- 30. Свойства живого, связанные с белками: Способность к воспроизведению себе подобных. Сократимость и движение. Обмен веществ. ХИМИЯ
- 31. Задание к видеофрагменту: Сколько белков должен употреблять ежедневно человек? Какая пища является источником белка? Почему белки
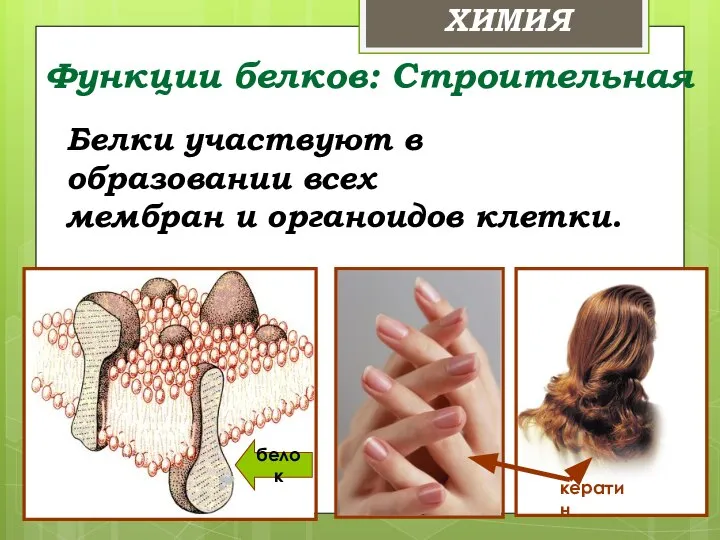
- 32. Функции белков: Строительная Белки участвуют в образовании всех мембран и органоидов клетки. белок кератин ХИМИЯ
- 33. Каталитическая В каждой клетке имеются сотни ферментов. Они помогают осуществлять биохимические реакции, действуя как катализаторы. Ускоряют
- 34. Транспортная Белки связывают и переносят различные вещества и внутри клетки, и по всему организму. Например, г
- 35. Регуляторная Белки - гормоны регулируют различные физиологические процессы. Например, инсулин регулирует уровень углеводов в крови. ХИМИЯ
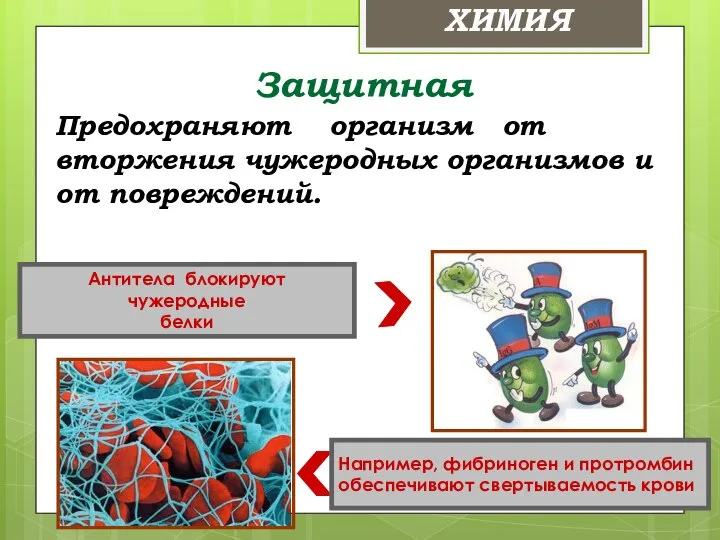
- 36. Защитная Например, фибриноген и протромбин обеспечивают свертываемость крови Антитела блокируют чужеродные белки Предохраняют организм от вторжения
- 37. Сократительная Белки - участвуют в сокращении мышечных волокон Актин и миозин – белки мышц ХИМИЯ
- 38. Энергетическая 1г белка - 17.6 кДж При недостатке углеводов или жиров окисляются молекулы аминокислот. При полном
- 39. Физико-химические свойства белков Белки имеют высокий молекулярный вес 16 000-1 000 000. Заряд белковой молекулы. Белковые
- 40. Химические свойства : Поддаются гидролизу с образованием аминокислот. Денатурируются: разрушается структура Горят - появляется запах жженого
- 41. Для обнаружения белков в растворе применяются цветные реакции: Видеоопыт: «Цветные реакции на белки» Задание: Записать название
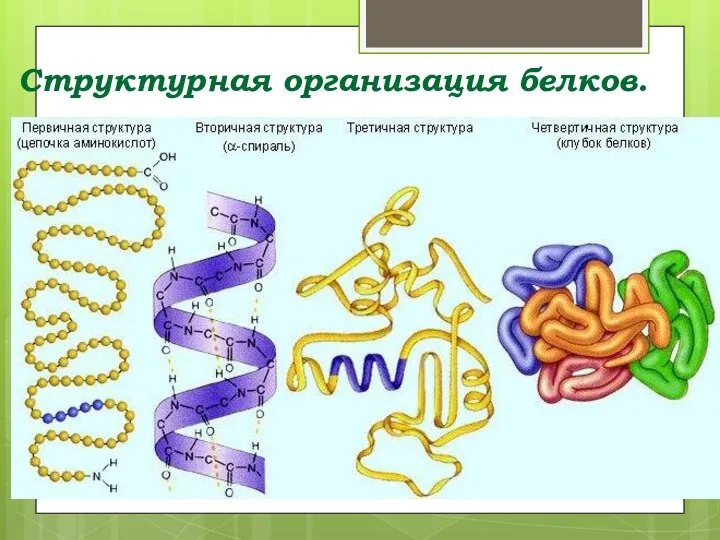
- 42. Структурная организация белков.
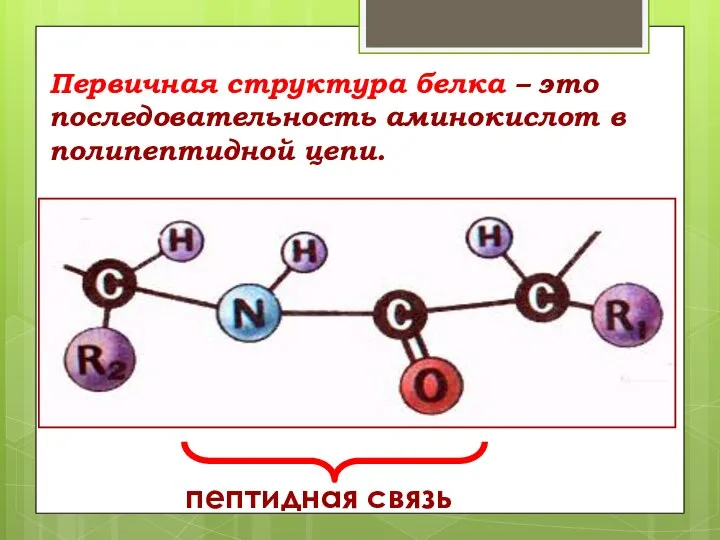
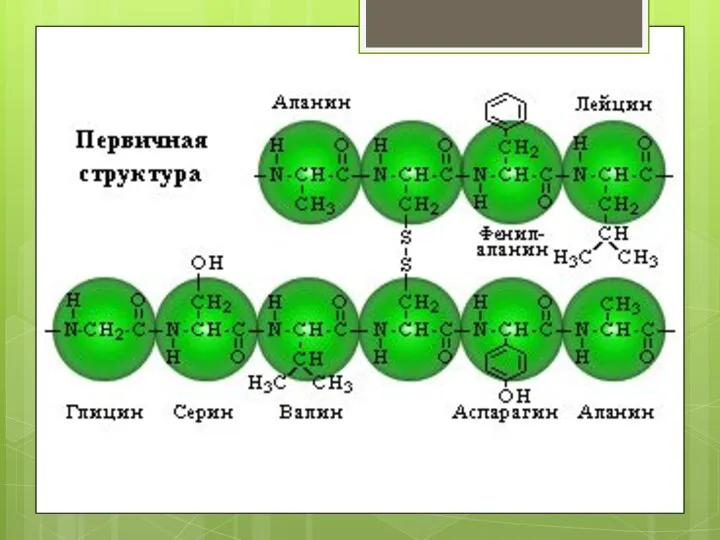
- 43. Первичная структура белка – это последовательность аминокислот в полипептидной цепи. пептидная связь
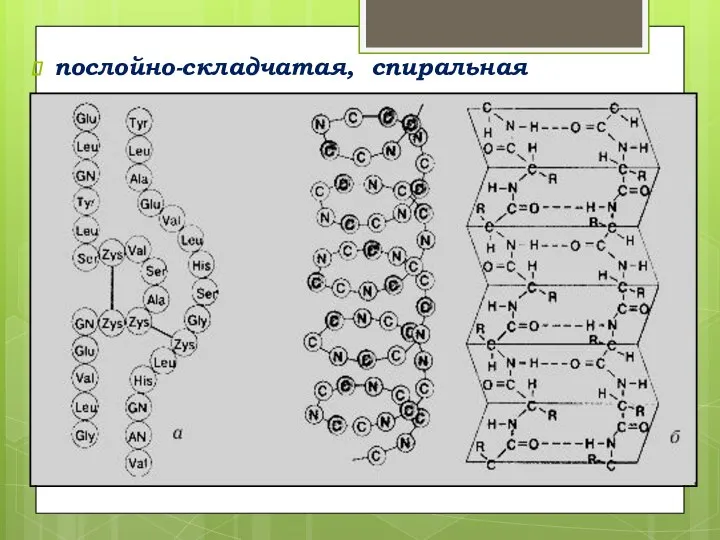
- 45. Вторичная структура - спираль, удерживаемая водородными связями.
- 46. послойно-складчатая, спиральная
- 47. Третичная структура – имеет вид клубка, удерживаемого взаимодействием различных остатков аминокислот. (дисульфидные связи)
- 48. Четвертичная структура агрегаты нескольких белковых макромолекул (белковые комплексы), образованные за счет взаимодействия разных полипептидных цепей
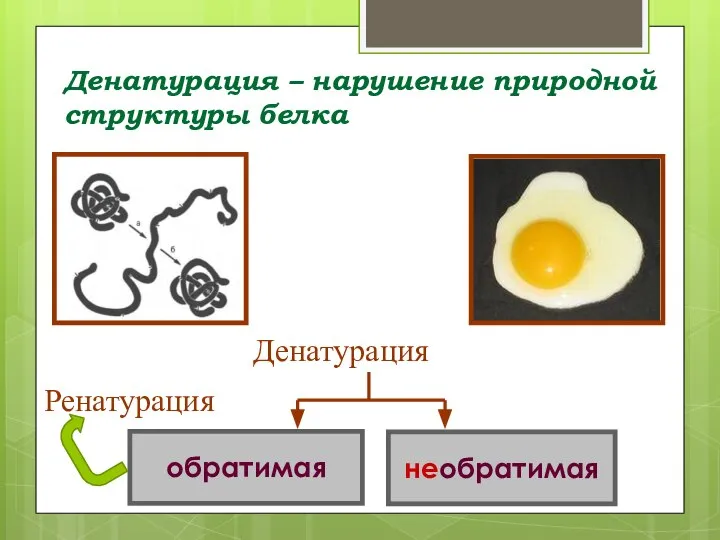
- 49. Денатурация – нарушение природной структуры белка. Денатурация необратимая обратимая Ренатурация
- 51. Проблемный вопрос: Можно ли утверждать что: «Нет белка – нет органической жизни на Земле»? Обоснуйте ответ,
- 52. Ситуационные задачи Почему яйца или молоко применяют в качестве противоядия при отравлении солями тяжелых металлов?
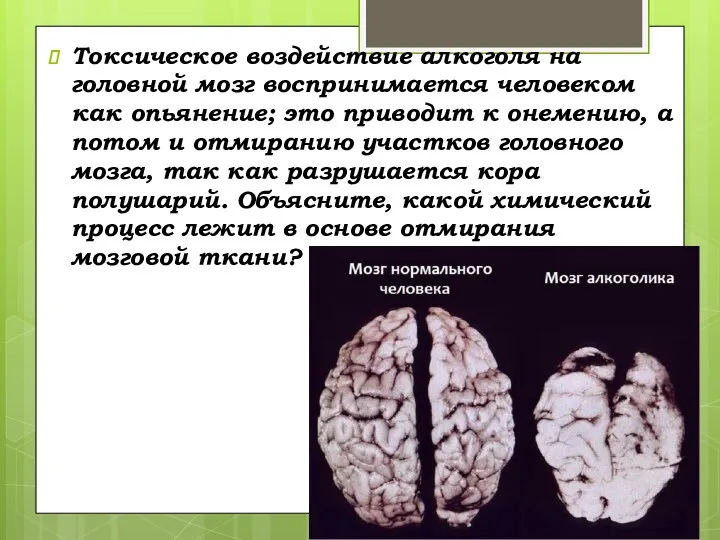
- 53. Токсическое воздействие алкоголя на головной мозг воспринимается человеком как опьянение; это приводит к онемению, а потом
- 54. Ситуационные задачи Почему ученые называют белки биологическими «бусами»?
- 55. Домашнее задание: 1. Изучить тему: «Аминокислоты, пептиды, белки» 2. Выполнить задания 17.13 – 17.18, с 326.
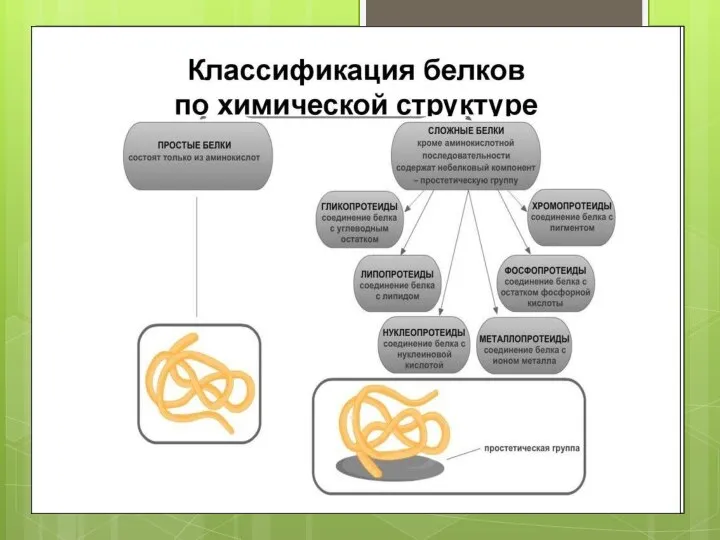
- 57. Сложные белки: 1. Гликопротеины (содержат углеводы). 2. Липопротеины (содержат липиды). 3. Фосфопротеины (содержат фосфорную кислоту). 4.
- 59. Скачать презентацию




































 Генетика соматических клеток. Методы генетики соматических клеток
Генетика соматических клеток. Методы генетики соматических клеток Презентация на тему Методы селекции растений (11 класс)
Презентация на тему Методы селекции растений (11 класс)  Презентация на тему Биология – наука о живой природе (5 класс)
Презентация на тему Биология – наука о живой природе (5 класс)  Кровеносная система
Кровеносная система 787229
787229 Основные методы селекции
Основные методы селекции Закономерности происхождения и развития жизни на Земле. 9 класс
Закономерности происхождения и развития жизни на Земле. 9 класс Самые – самые – самые… Пальма Рафия
Самые – самые – самые… Пальма Рафия Биология в естествознании
Биология в естествознании Викторина По страницам школьных учебников. Биология – чудеса привычного мира
Викторина По страницам школьных учебников. Биология – чудеса привычного мира Микроорганизмы - экстремофилы
Микроорганизмы - экстремофилы Место человека в системе органического мира
Место человека в системе органического мира Луговые цветы
Луговые цветы Красная книга. Проект
Красная книга. Проект Сон и сновидения
Сон и сновидения Микробиологическое исследование молочных продуктов продовольственных магазинов г. Барнаула
Микробиологическое исследование молочных продуктов продовольственных магазинов г. Барнаула Анатомия и физиология человека. Пищеварительная система. (Лекция 6)
Анатомия и физиология человека. Пищеварительная система. (Лекция 6) Типы и варианты наследования признаков
Типы и варианты наследования признаков Естественные и искусственные биоценозы
Естественные и искусственные биоценозы Бионеорганическая химия. Особенности биохимический процессов. (Лекция 1)
Бионеорганическая химия. Особенности биохимический процессов. (Лекция 1) Дыхание животных
Дыхание животных Генетический код
Генетический код Основные отряды Насекомых (7 класс)
Основные отряды Насекомых (7 класс) Углеводы. Химический состав клетки
Углеводы. Химический состав клетки Презентация на тему РАНЫ. ВИДЫ РАН
Презентация на тему РАНЫ. ВИДЫ РАН  Водоросли. Среда обитания
Водоросли. Среда обитания Презентация на тему Жабы и лягушки
Презентация на тему Жабы и лягушки  Голонасінні рослини
Голонасінні рослини