Содержание
- 2. П Л А Н 15.1 Аминокислоты, входящие в состав белков. Классификация. Стереоизомерия 15.2. Биосинтетические пути образования
- 3. 15.1 Аминокислоты, входящие в состав белков. Классификация. Стереоизомерия Аминокислоты - это производные карбоновых кислот, содержащие одновременно
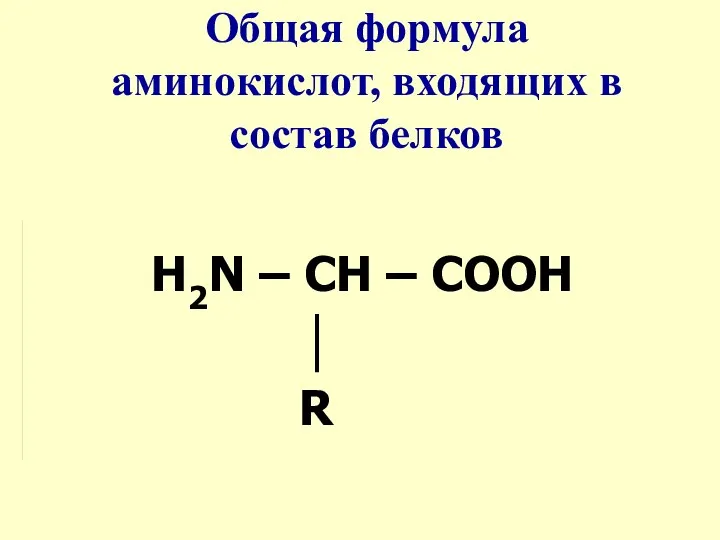
- 4. Общая формула аминокислот, входящих в состав белков Н2N – СН – СООН │ R
- 5. Аминокислоты, входящие в состав белков проявляют особые свойства Все относятся к α-аминокислотам Являются L-стереоизомерами Относятся к
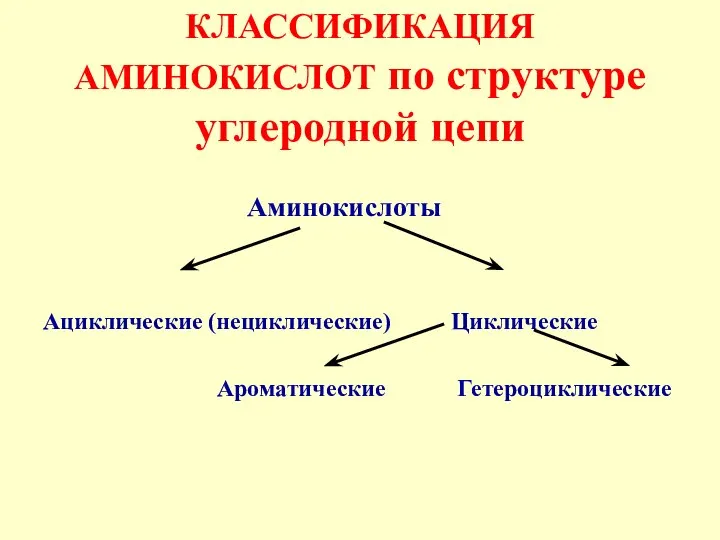
- 6. КЛАССИФИКАЦИЯ АМИНОКИСЛОТ по структуре углеродной цепи Аминокислоты Ациклические (нециклические) Циклические Ароматические Гетероциклические
- 7. Классификация по кислотно-основным группам, наличию других функциональных групп и радикалов Моноаминокарбоновые (нейтральные) аминокислоты: Аминоуксусная кислота, 2-аминоэтановаякислота,
- 8. α-аминопропионовая кислота, 2-аминопропановая кислота, аланин ( АЛА) Источник энергии для головного мозга и ЦНС, укрепляет иммунную
- 9. α-амино-β-гидроксипропионовая кислота, 2-амино-3-гидроксипропановая кислота, серин ( СЕР) Входит в состав белков растительного и животного происхождения, очень
- 10. α-амино-β-тиопропионовая кислота, 2- амино-3-меркаптопропановая кислота, цистеин (ЦИС) Участвует в обмене серы в организме, обладает радиопротекторным действием,
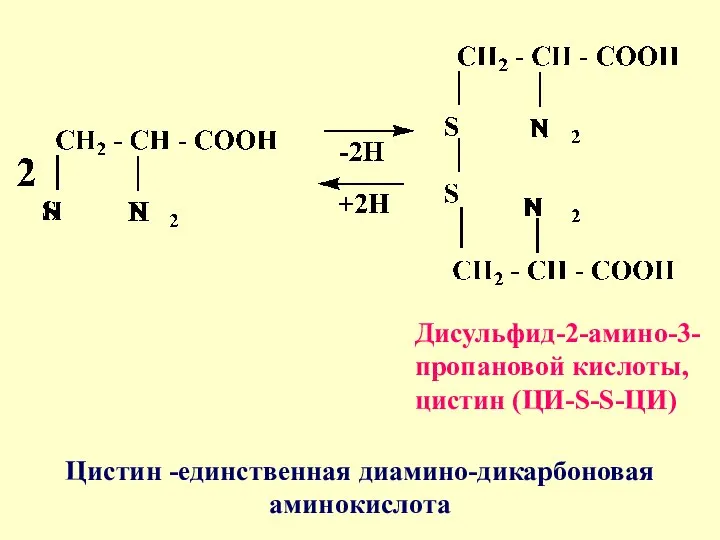
- 11. Дисульфид-2-амино-3-пропановой кислоты, цистин (ЦИ-S-S-ЦИ) Цистин -единственная диамино-дикарбоновая аминокислота
- 12. α-амино-γ-метилтиомасляная кислота, 2-амино-4-метилтиобутановая кислота, метионин (МЕТ) Метионин имеет метильную группу, благодаря которой способствует предупреждению ожирения печени,
- 13. Метионин, цистеин и цистин относят к серусодержащим аминокислотам, их особенно много в белках, которые входят в
- 14. α-аминоизовалериановая кислота, 2-амино-3-метилбутановая кислота, валин (ВАЛ) Один из главных компонентов роста тканей, применяется как антидепресант
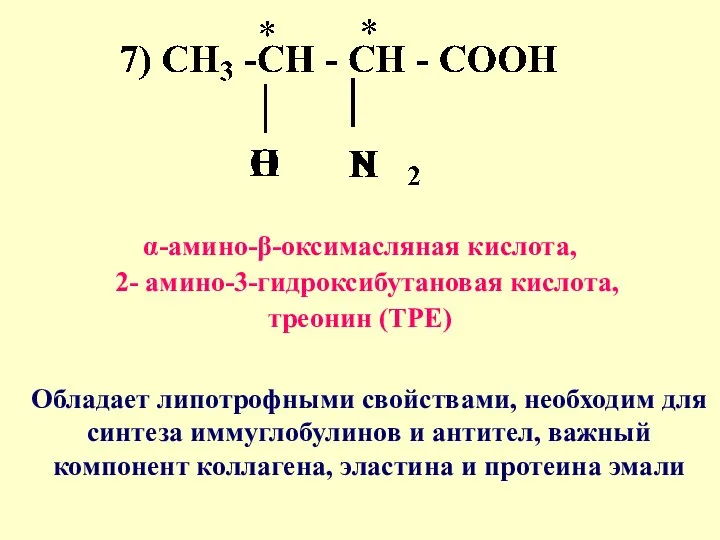
- 15. α-амино-β-оксимасляная кислота, 2- амино-3-гидроксибутановая кислота, треонин (ТРЕ) Обладает липотрофными свойствами, необходим для синтеза иммуглобулинов и антител,
- 16. α-аминоизокапроновая кислота, 2-амино-4-метилпентановая кислота, лейцин (ЛЕЙ) Лейцин в большом количестве содержится в гемоглобине, казеине, яичном альбумине,
- 17. α-амино-β-метилвалериановая кислота, 2- амино-3-метилпентановая кислота, изолейцин (ИЛЕ)
- 18. Моноаминодикарбоновые (кислые) аминокислоты: α-аминоянтарная кислота, 2-аминобутадиовая кислота, аспарагиновая кислота (АСП) Принимает участие в реакциях переаминирования, в
- 19. Моноаминодикарбоновые (кислые) аминокислоты: α-аминоглутаровая кислота, 2-аминопентандиовая кислота, глутаминовая кислота (ГЛУ) Источник аминогруппы в метаболических процессах
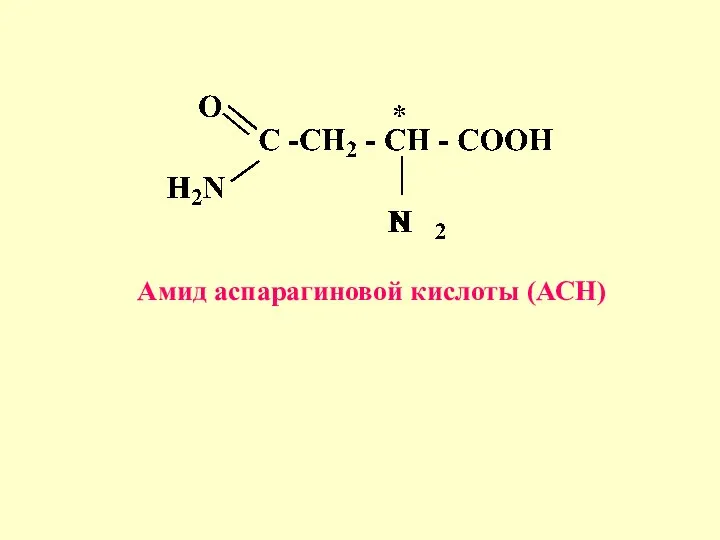
- 20. Амид аспарагиновой кислоты (АСН)
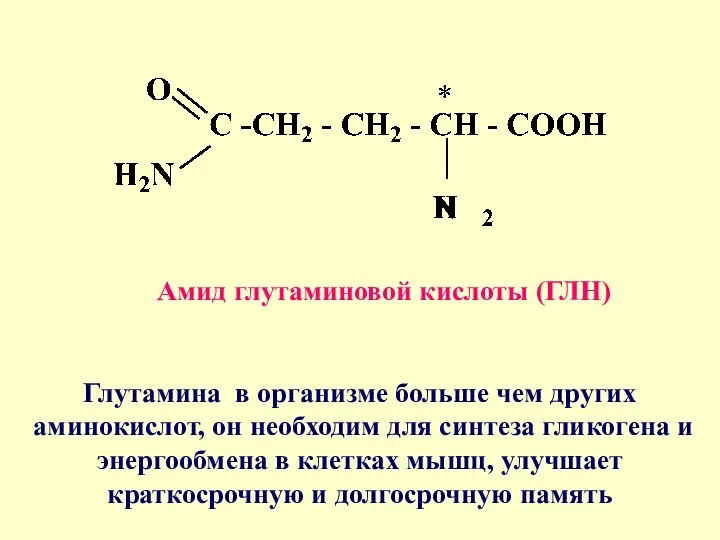
- 21. Глутамина в организме больше чем других аминокислот, он необходим для синтеза гликогена и энергообмена в клетках
- 22. Диаминомонокарбоновые (основные) аминокислоты: α,ε-диаминокапроновая кислота, 2,6-диаминогексановая кислота, лизин (ЛИЗ) Обеспечивает усвоение кальция, участвует в образовании коллагена,
- 23. Диаминомонокарбоновые (основные) аминокислоты: α-амино-Δ-гуанидилвалериановая кислота, 2-амино-5-гуанидилпентановая кислота, аргинин (АРГ) Вызывает замедление развития опухолей, укрепляет иммунную систему,
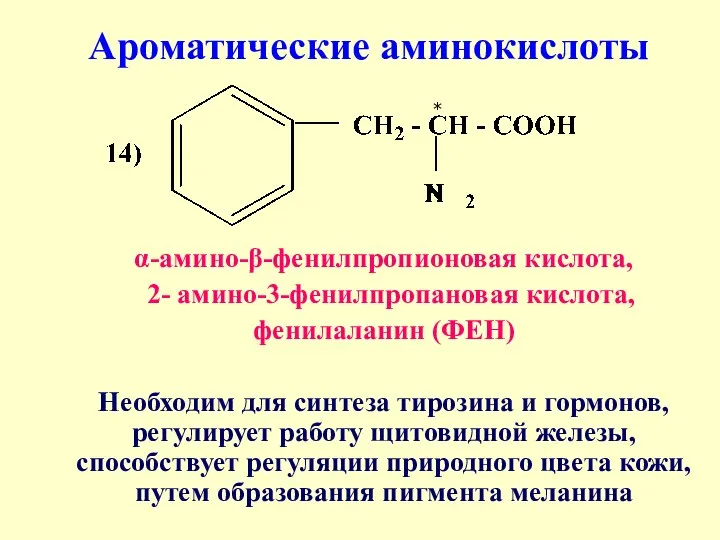
- 24. α-амино-β-фенилпропионовая кислота, 2- амино-3-фенилпропановая кислота, фенилаланин (ФЕН) Необходим для синтеза тирозина и гормонов, регулирует работу щитовидной
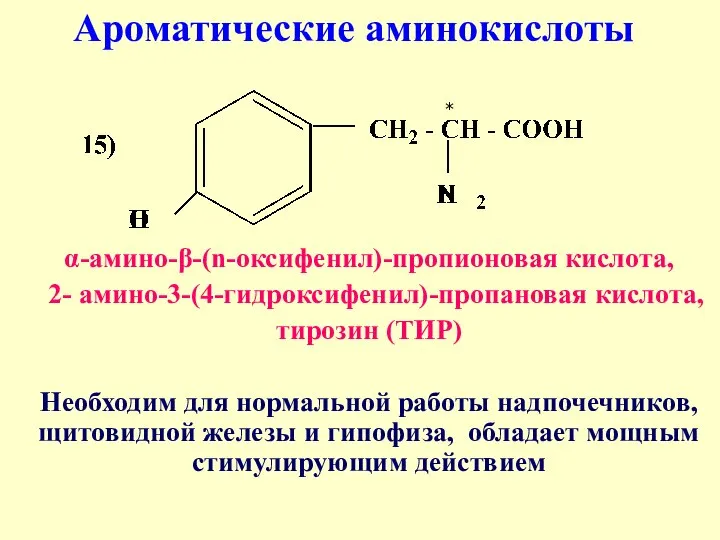
- 25. α-амино-β-(n-оксифенил)-пропионовая кислота, 2- амино-3-(4-гидроксифенил)-пропановая кислота, тирозин (ТИР) Необходим для нормальной работы надпочечников, щитовидной железы и гипофиза,
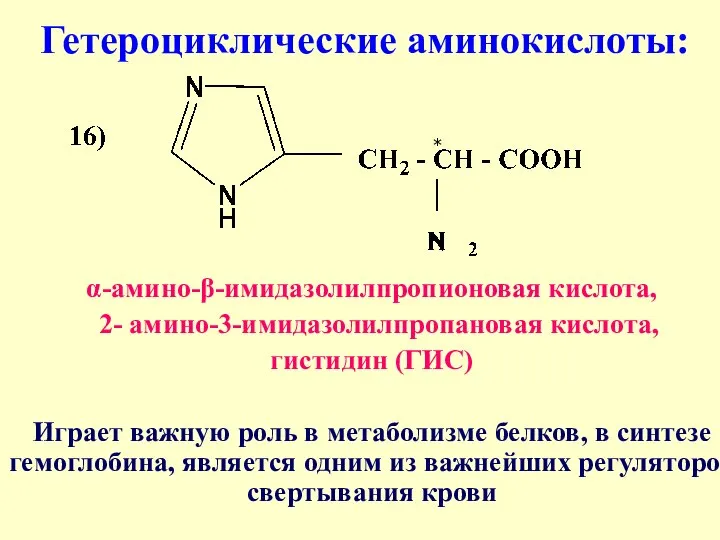
- 26. Гетероциклические аминокислоты: α-амино-β-имидазолилпропионовая кислота, 2- амино-3-имидазолилпропановая кислота, гистидин (ГИС) Играет важную роль в метаболизме белков, в
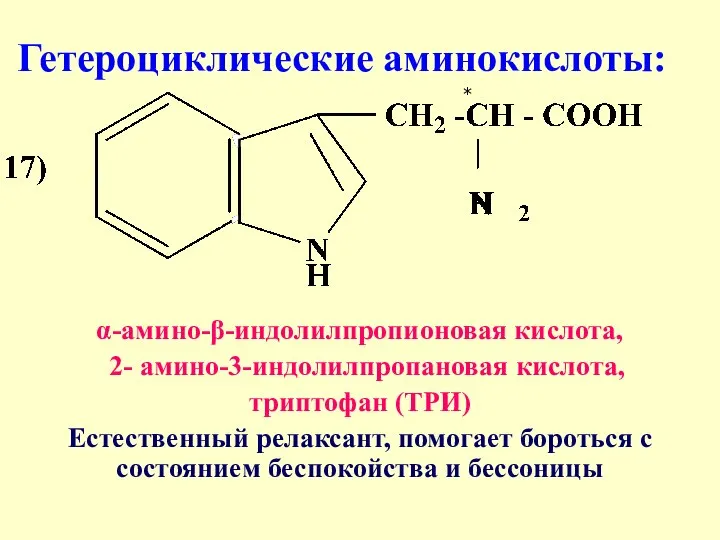
- 27. Гетероциклические аминокислоты: α-амино-β-индолилпропионовая кислота, 2- амино-3-индолилпропановая кислота, триптофан (ТРИ) Естественный релаксант, помогает бороться с состоянием беспокойства
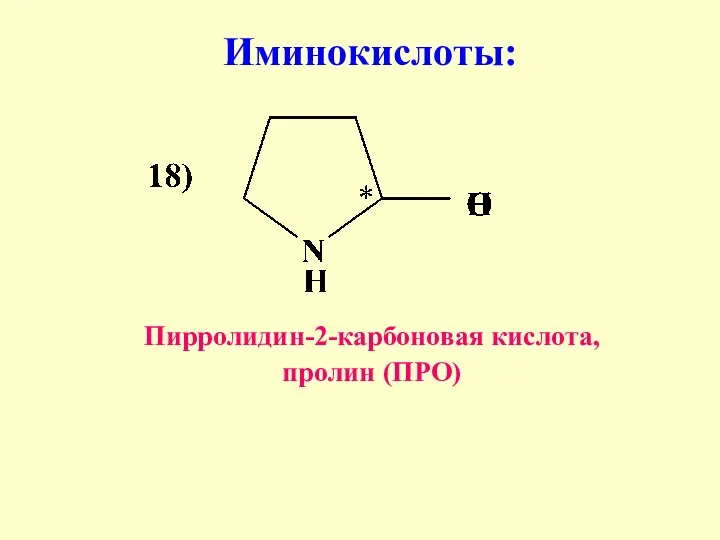
- 28. Иминокислоты: Пирролидин-2-карбоновая кислота, пролин (ПРО)
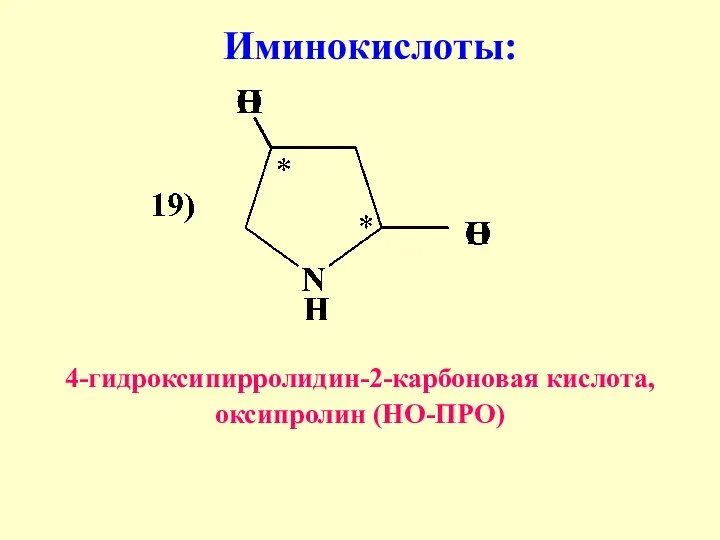
- 29. Иминокислоты: 4-гидроксипирролидин-2-карбоновая кислота, оксипролин (НО-ПРО)
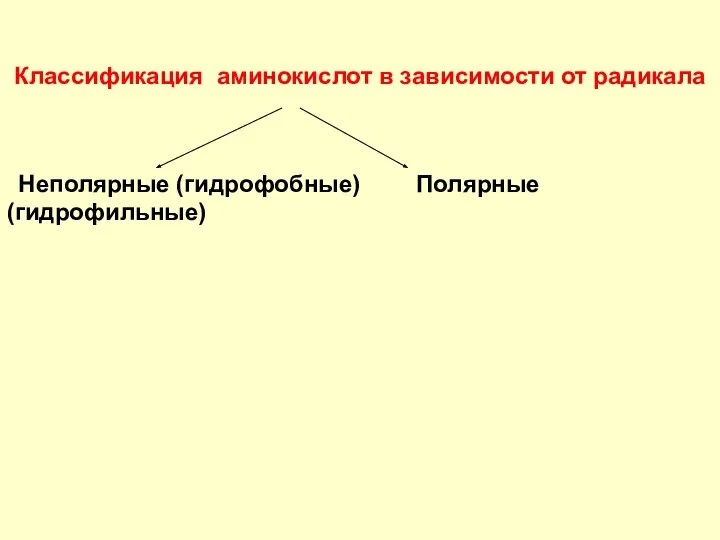
- 30. Неполярные (гидрофобные) Полярные(гидрофильные) Классификация аминокислот в зависимости от радикала
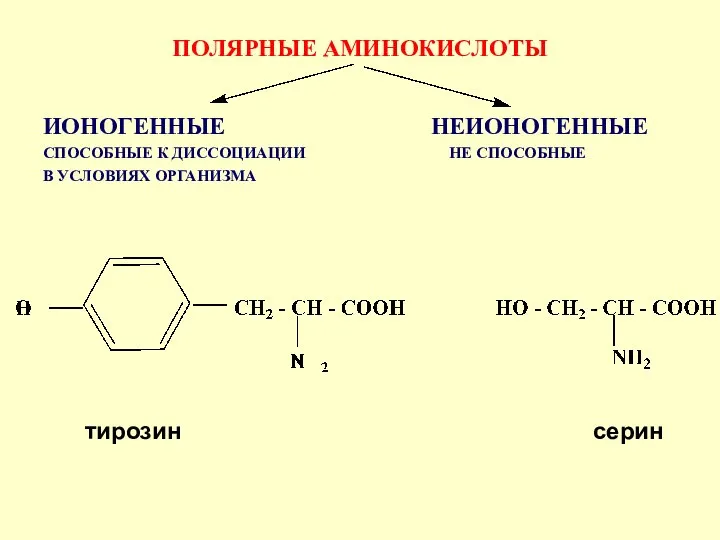
- 31. тирозин серин ПОЛЯРНЫЕ АМИНОКИСЛОТЫ ИОНОГЕННЫЕ НЕИОНОГЕННЫЕ СПОСОБНЫЕ К ДИССОЦИАЦИИ НЕ СПОСОБНЫЕ В УСЛОВИЯХ ОРГАНИЗМА
- 32. Полярные аминокислоты с ионогенными группами в условиях организма могут находиться в виде анионов и катионов В
- 33. Полярные ионогенные радикалы располагаются как на поверхности, так и внутри белковых молекул. Они участвуют в образовании
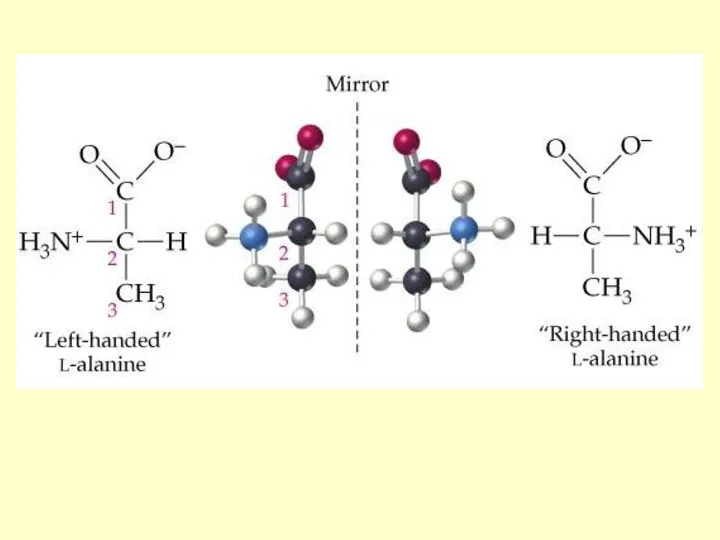
- 34. Все α-аминокислоты, за исключением глицина, имеют асимметрический атом углерода и существуют в виде энантиомеров, относящихся к
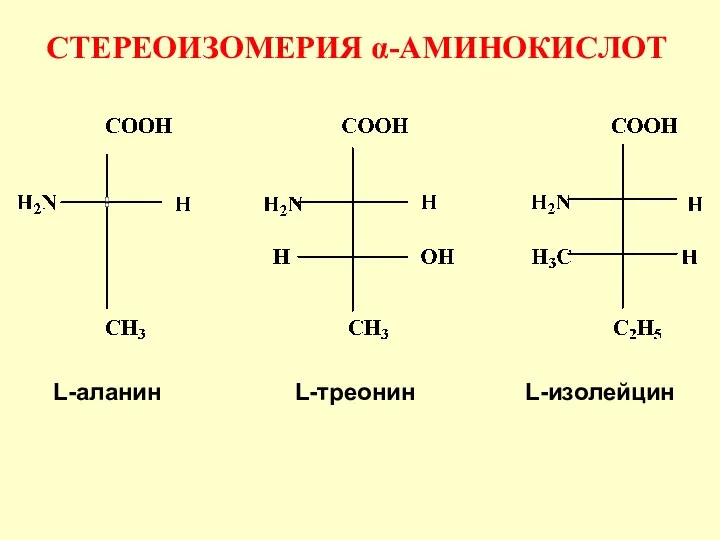
- 35. L-аланин L-треонин L-изолейцин СТЕРЕОИЗОМЕРИЯ α-АМИНОКИСЛОТ
- 37. Три аминокислоты имеют два центра хиральности треонин изолейцин, 4-гидроксипролин
- 38. 15.2. БИОСИНТЕТИЧЕСКИЕ ПУТИ ОБРАЗОВАНИЯ АМИНОКИСЛОТ Биосинтез α-аминокислот осуществляется из α-кетокислот - продуктов метаболизма углеводов. Возможны два
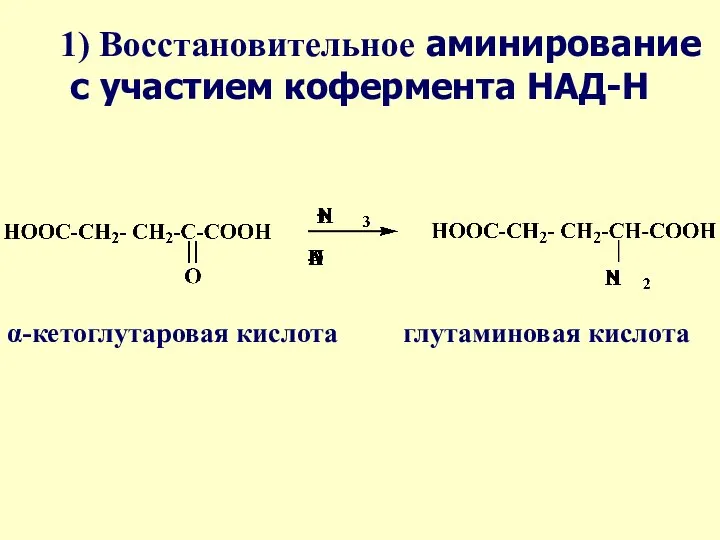
- 39. 1) 1) Восстановительное аминирование с участием кофермента НАД-Н α-кетоглутаровая кислота глутаминовая кислота
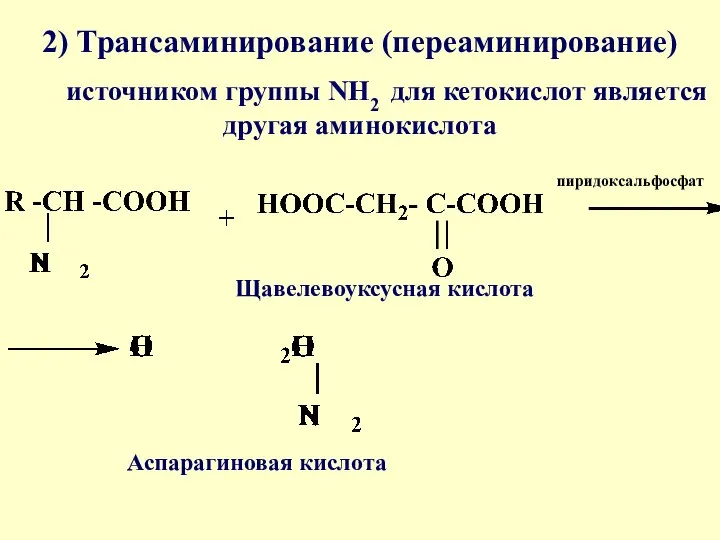
- 40. 2) Трансаминирование (переаминирование) источником группы NH2 для кетокислот является другая аминокислота пиридоксальфосфат Щавелевоуксусная кислота Аспарагиновая кислота
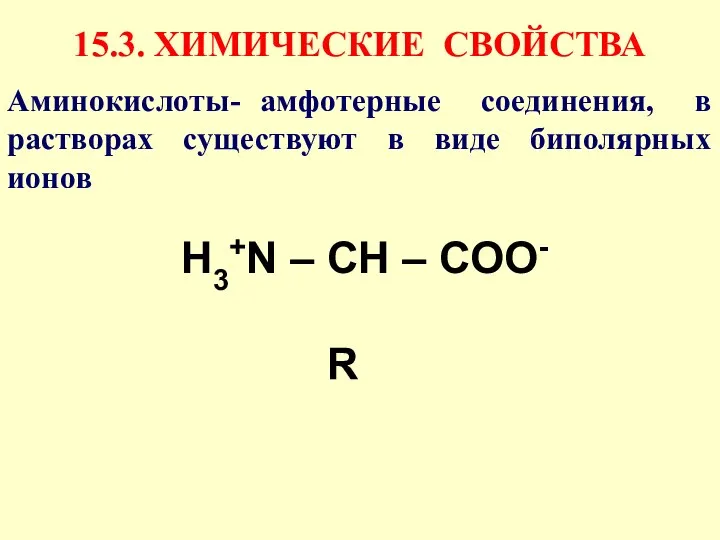
- 41. Н3+N – СН – СОО- R 15.3. ХИМИЧЕСКИЕ СВОЙСТВА Аминокислоты- амфотерные соединения, в растворах существуют
- 42. Аминокислотам присущи все свойства как карбоновых кислот, так и аминов Реакции карбоксильной группы - образование функциональных
- 43. Для аминокислот характерен целый ряд специфических реакций, обусловленных наличием в их структуре COOH- и NH2- групп
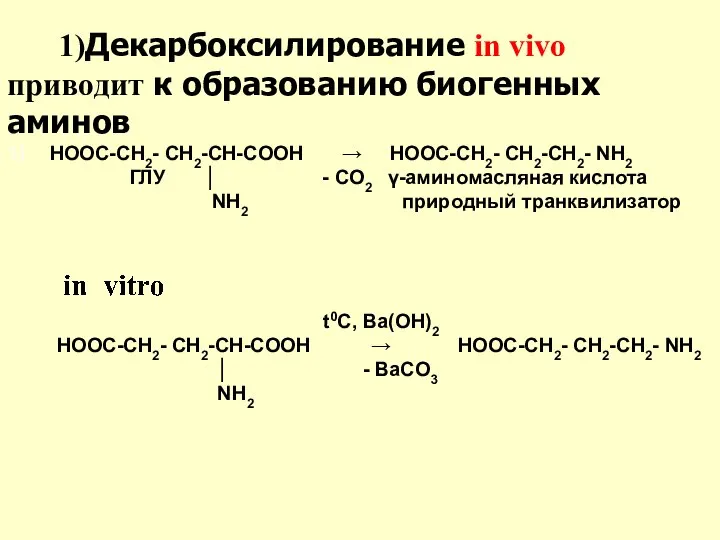
- 44. 1) HOOC-CH2- CH2-CH-COOH → HOOC-CH2- CH2-CH2- NH2 ГЛУ │ - CO2 γ-аминомасляная кислота NH2 природный транквилизатор
- 45. В результате реакции декарбоксилирования образуются биогенные амины (триптамин, гистамин, коламин, дофамин, серотонин)
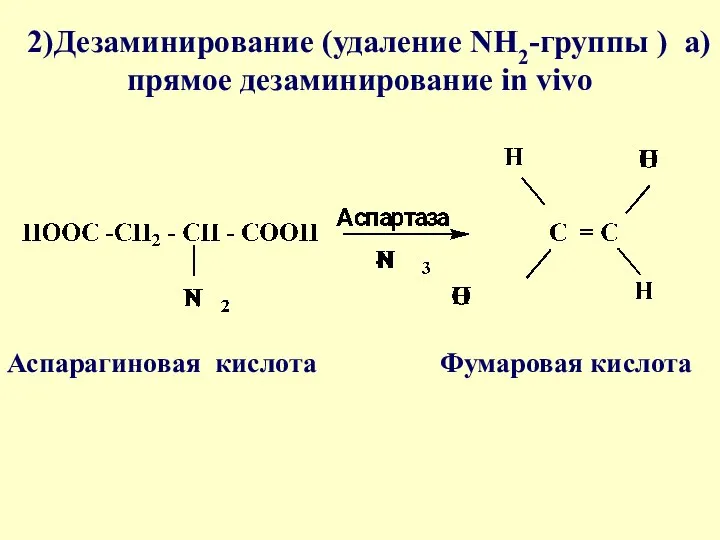
- 46. 2)Дезаминирование (удаление NH2-группы ) а)прямое дезаминирование in vivo Фумаровая кислота Аспарагиновая кислота
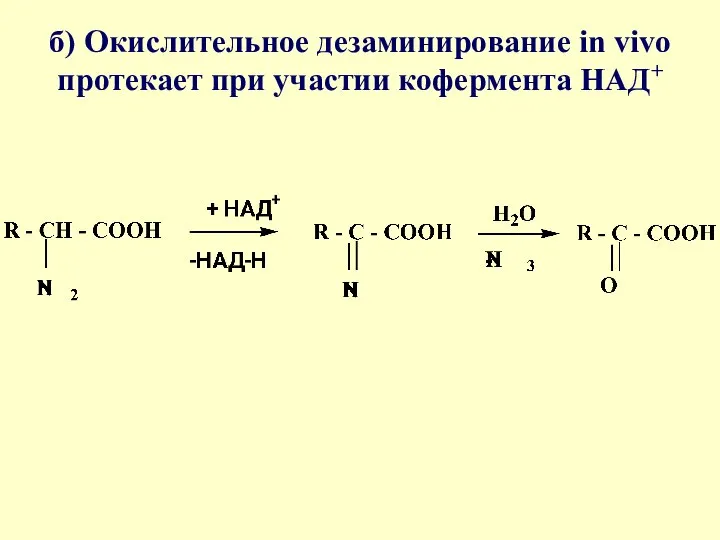
- 47. б) Окислительное дезаминирование in vivo протекает при участии кофермента НАД+
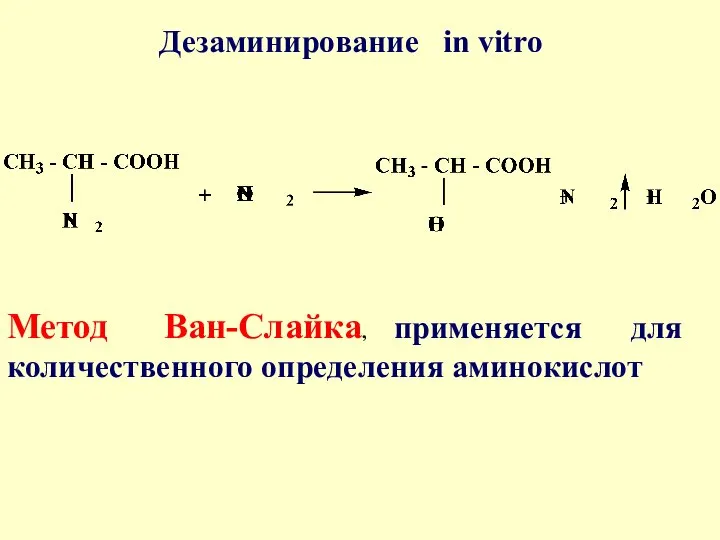
- 48. Дезаминирование in vitro Метод Ван-Слайка, применяется для количественного определения аминокислот
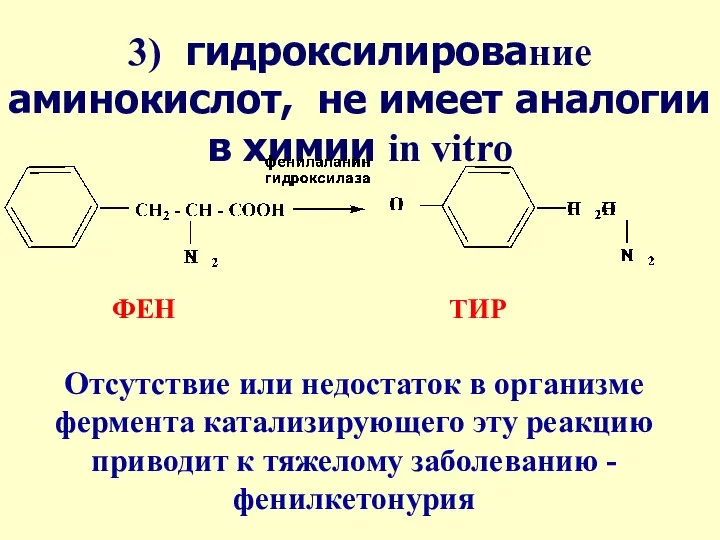
- 49. ФЕН ТИР 3) гидроксилирование аминокислот, не имеет аналогии в химии in vitro Отсутствие или недостаток в
- 51. Скачать презентацию
























 Удивительные и загадочные Ахатины (Achatina fulica)
Удивительные и загадочные Ахатины (Achatina fulica) День добра. Животные
День добра. Животные Методы селекции и исходный материал
Методы селекции и исходный материал Презентация на тему Животные Австралии
Презентация на тему Животные Австралии  Астра однолетняя
Астра однолетняя Патология ультраструктур клетки
Патология ультраструктур клетки Уход за культурными растениями
Уход за культурными растениями Пифарнин (ribavirin)
Пифарнин (ribavirin) Животные, имеющие суперспособности
Животные, имеющие суперспособности Презентация на тему Строение растений
Презентация на тему Строение растений  Цианобактерии. Крупные грамотрицательные бактерии, способные к фотосинтезу, сопровождающемуся выделением кислорода
Цианобактерии. Крупные грамотрицательные бактерии, способные к фотосинтезу, сопровождающемуся выделением кислорода Выращивание цветочной рассады
Выращивание цветочной рассады Брендбук. Хаски - центр У каменных ворот
Брендбук. Хаски - центр У каменных ворот Презентация на тему Горох Менделя
Презентация на тему Горох Менделя  Разноцветный мир растений. 5 класс
Разноцветный мир растений. 5 класс Лилейные и злаковые растения
Лилейные и злаковые растения Кровеносная система и её заболевания
Кровеносная система и её заболевания Стадии эволюции человека
Стадии эволюции человека О рыбах
О рыбах Дифференциация клеток тканей растений. Механизм регуляции функций у растений
Дифференциация клеток тканей растений. Механизм регуляции функций у растений Соцветия. 6 класс
Соцветия. 6 класс Побег. Виды почек
Побег. Виды почек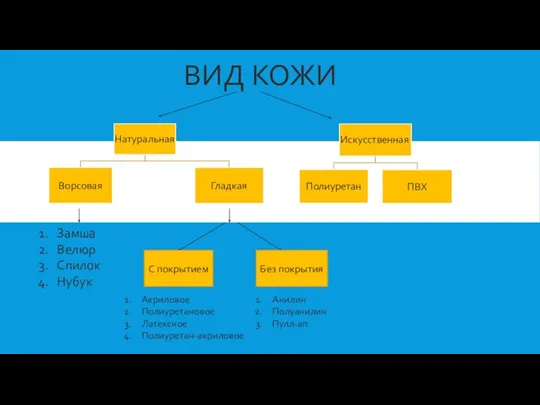 Вид кожи
Вид кожи Значение и мероприятия селекционно-племенной работы в животноводстве. Структура организаций
Значение и мероприятия селекционно-племенной работы в животноводстве. Структура организаций Строение и свойства клетки
Строение и свойства клетки Влияние соотношения фракций семян с различными морфотипами зародыша на урожайность озимой твердой пшеницы
Влияние соотношения фракций семян с различными морфотипами зародыша на урожайность озимой твердой пшеницы Корни.Корневые системы
Корни.Корневые системы Происхождение трансляционных процессов и генетического кода
Происхождение трансляционных процессов и генетического кода