Содержание
- 2. Процессинг иРНК – процесс созревания зрелой иРНК 5’ 3’ Кэпирование Присоединение полиаденилового «хвоста» Вырезание интронов Сплайсинг
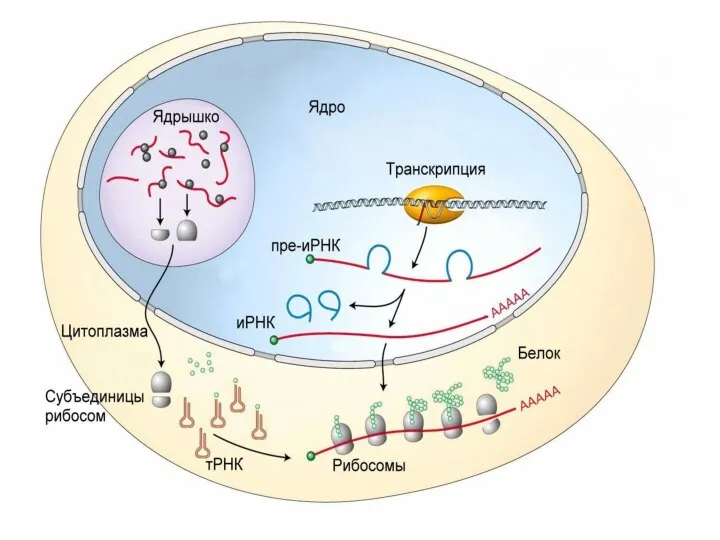
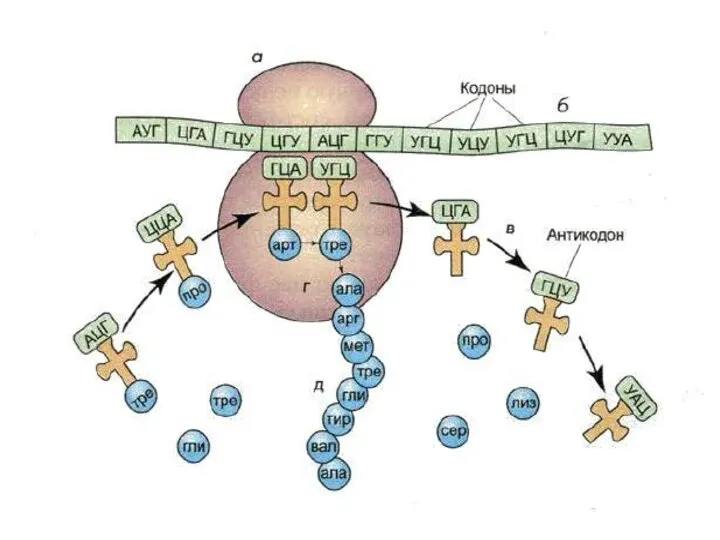
- 3. Трансляция – это синтез белковой молекулы (полипептида) на матрице и-РНК. Проходит в цитоплазме клетки или на
- 5. Для трансляции необходимы: 1. иРНК, кодирующая последовательность аминокислот в полипептиде; 2. рибосомы, образующие полипептид; 3. тРНК,
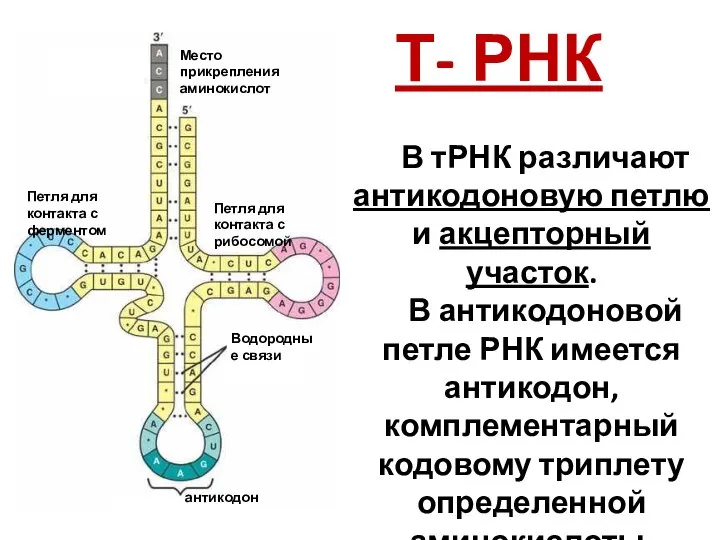
- 6. Т- РНК В тРНК различают антикодоновую петлю и акцепторный участок. В антикодоновой петле РНК имеется антикодон,
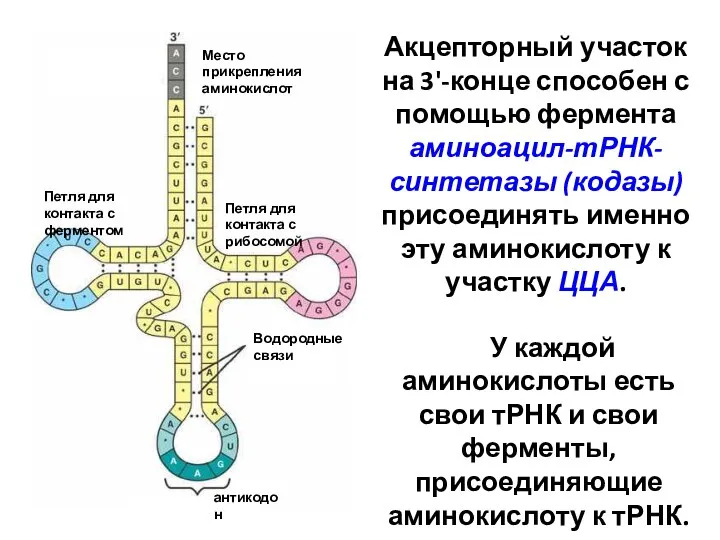
- 7. Акцепторный участок на 3'-конце способен с помощью фермента аминоацил-тРНК-синтетазы (кодазы) присоединять именно эту аминокислоту к участку
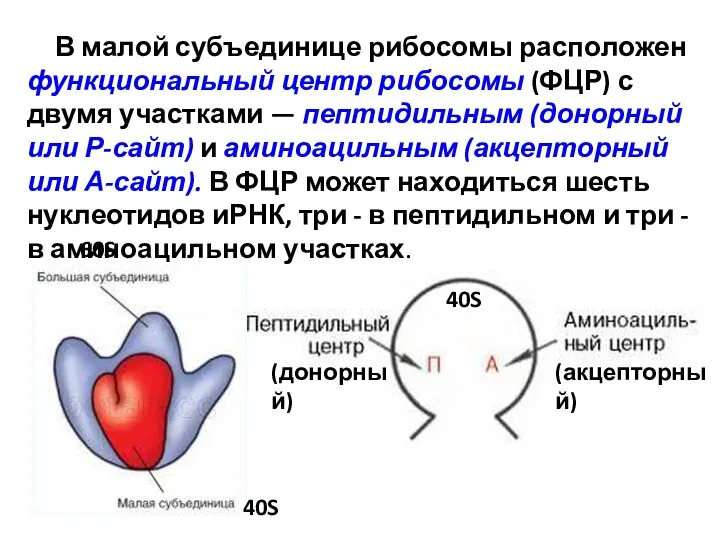
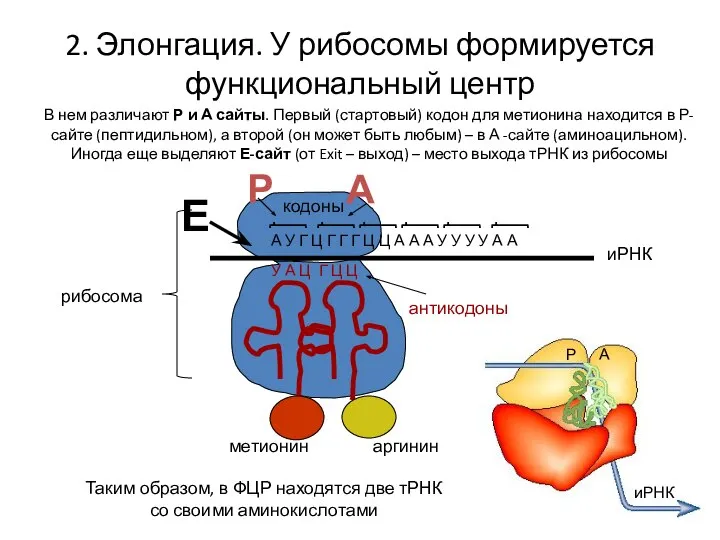
- 8. В малой субъединице рибосомы расположен функциональный центр рибосомы (ФЦР) с двумя участками — пептидильным (донорный или
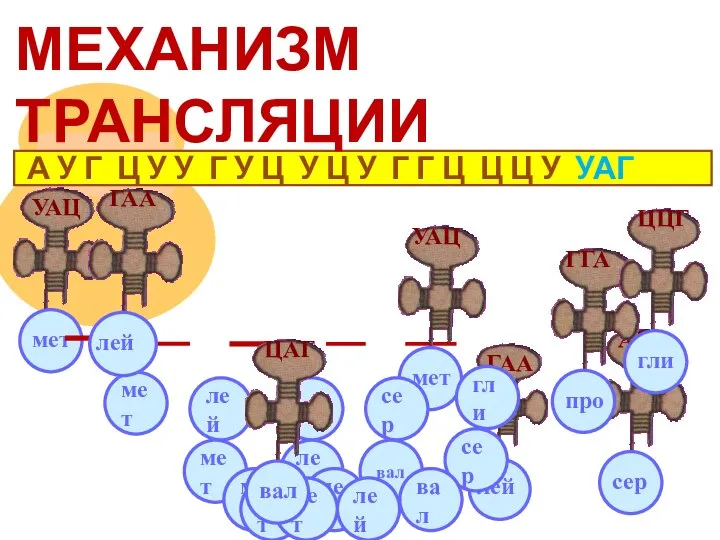
- 10. Различают три этапа в трансляции: Инициация. Синтез белка начинается с того момента, когда к 5'-концу иРНК
- 11. А У Г Ц У У Г У Ц У Ц У Г Г Ц Ц
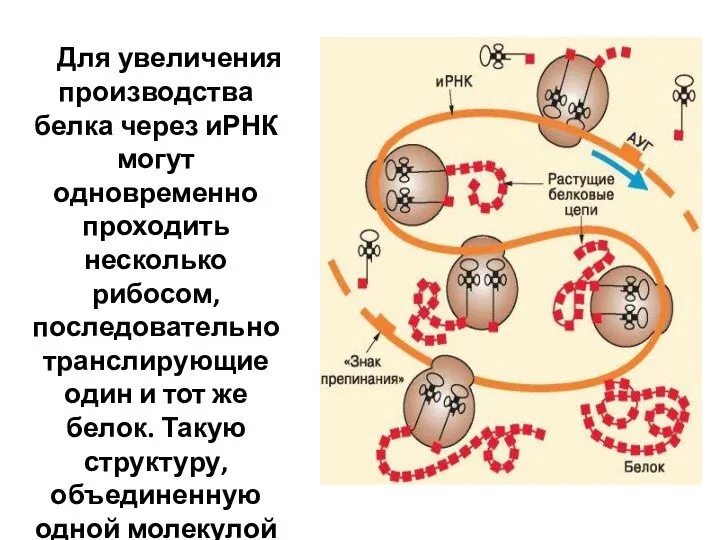
- 12. Для увеличения производства белка через иРНК могут одновременно проходить несколько рибосом, последовательно транслирующие один и тот
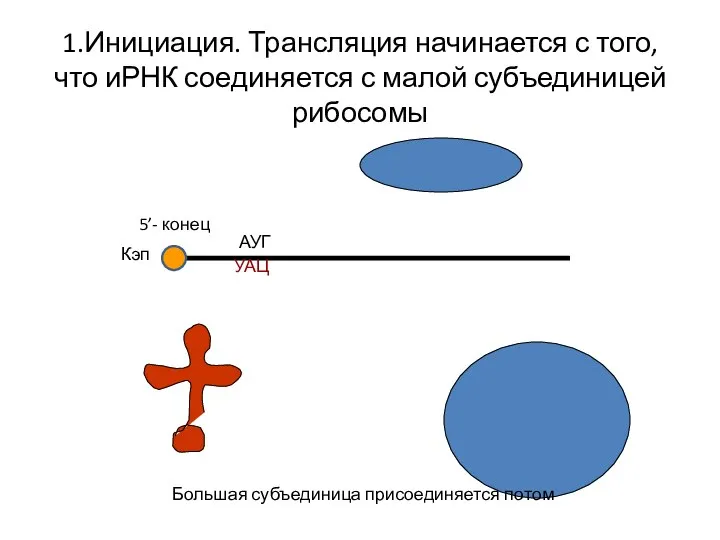
- 14. 1.Инициация. Трансляция начинается с того, что иРНК соединяется с малой субъединицей рибосомы АУГ УАЦ Большая субъединица
- 15. 2. Элонгация. У рибосомы формируется функциональный центр А У Г Ц Г Г Г Ц Ц
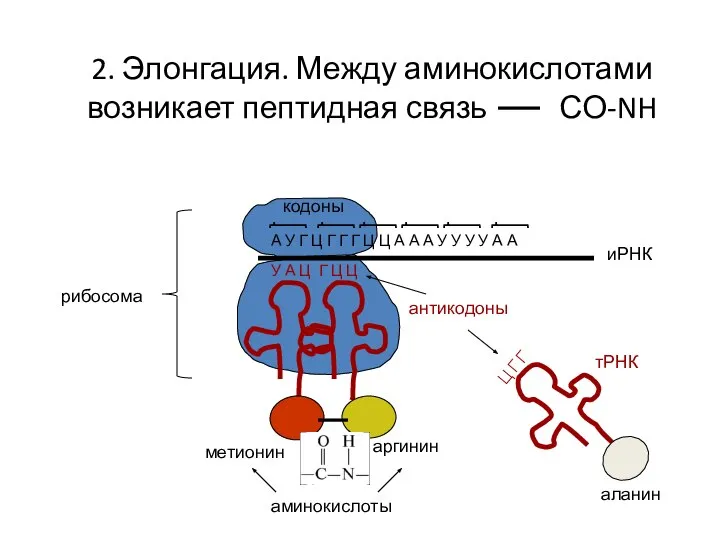
- 16. 2. Элонгация. Между аминокислотами возникает пептидная связь СО-NH А У Г Ц Г Г Г Ц
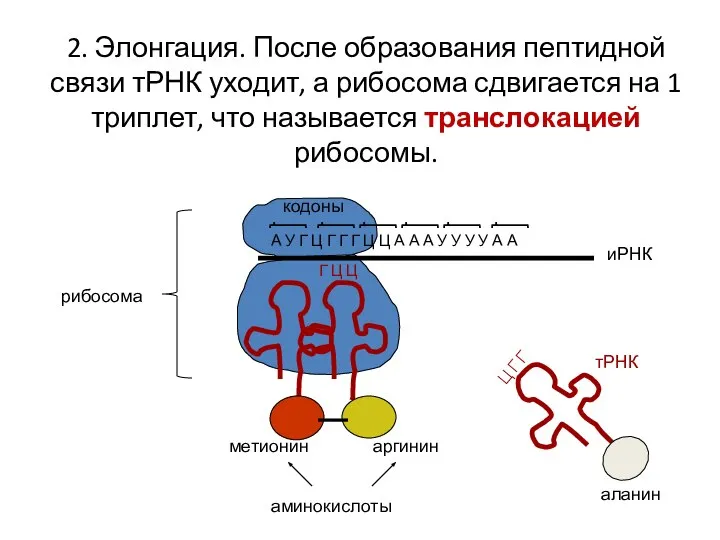
- 17. 2. Элонгация. После образования пептидной связи тРНК уходит, а рибосома сдвигается на 1 триплет, что называется
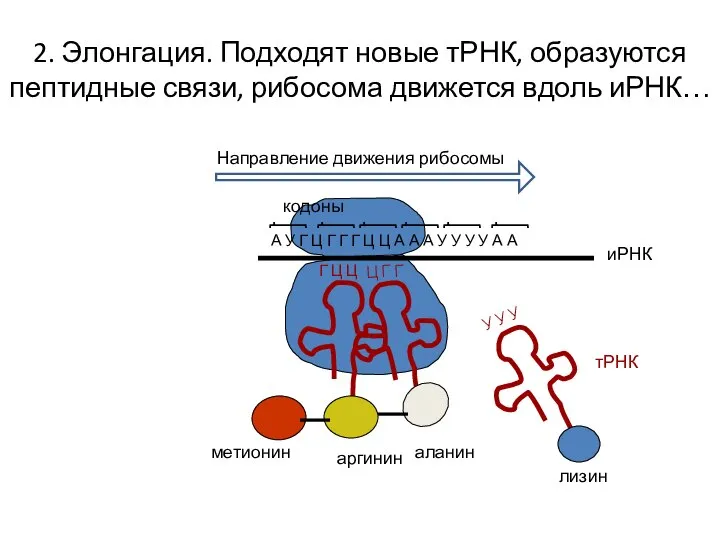
- 18. 2. Элонгация. Подходят новые тРНК, образуются пептидные связи, рибосома движется вдоль иРНК… А У Г Ц
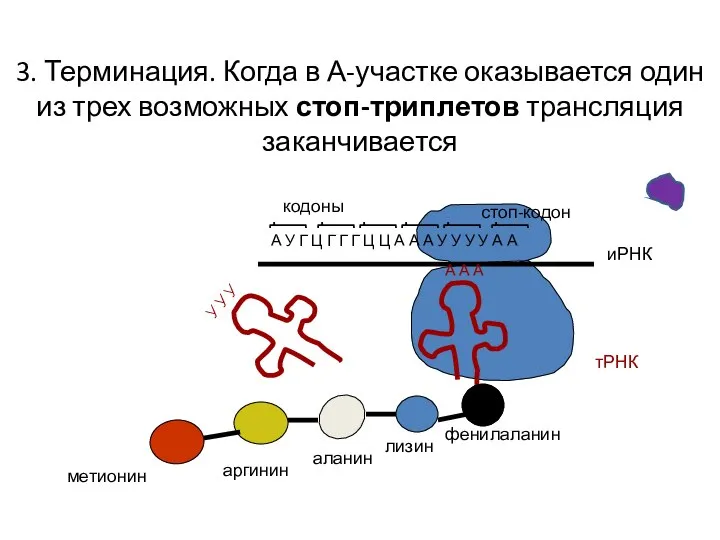
- 19. 3. Терминация. Когда в А-участке оказывается один из трех возможных стоп-триплетов трансляция заканчивается А У Г
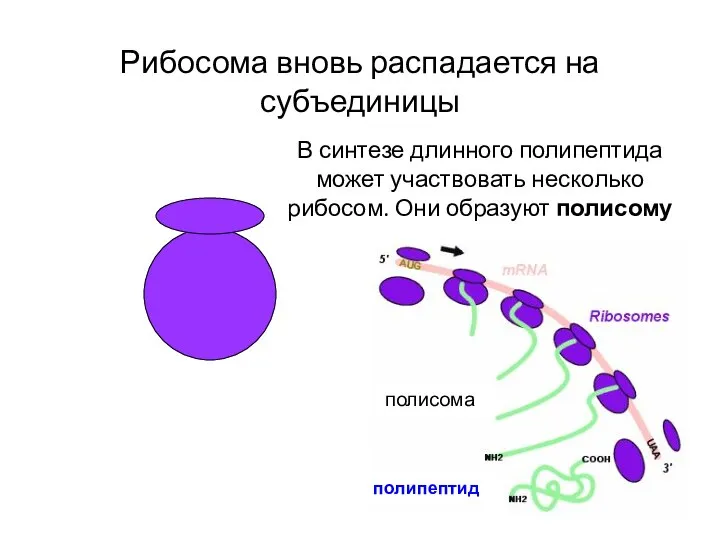
- 20. Рибосома вновь распадается на субъединицы В синтезе длинного полипептида может участвовать несколько рибосом. Они образуют полисому
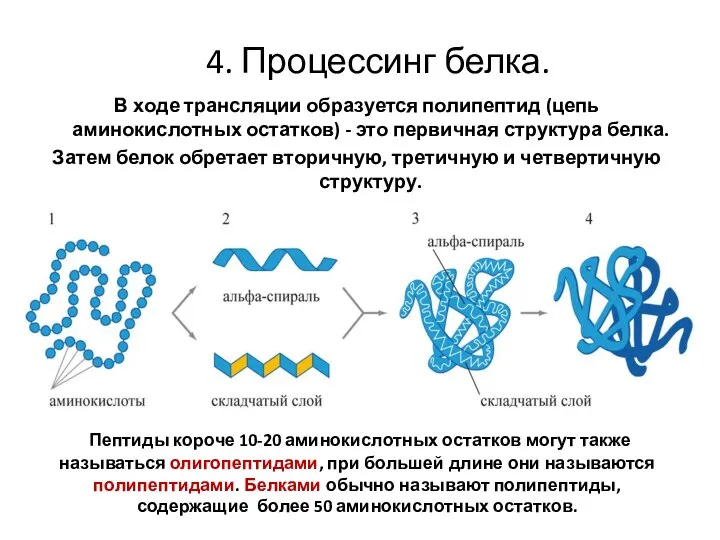
- 21. 4. Процессинг белка. В ходе трансляции образуется полипептид (цепь аминокислотных остатков) - это первичная структура белка.
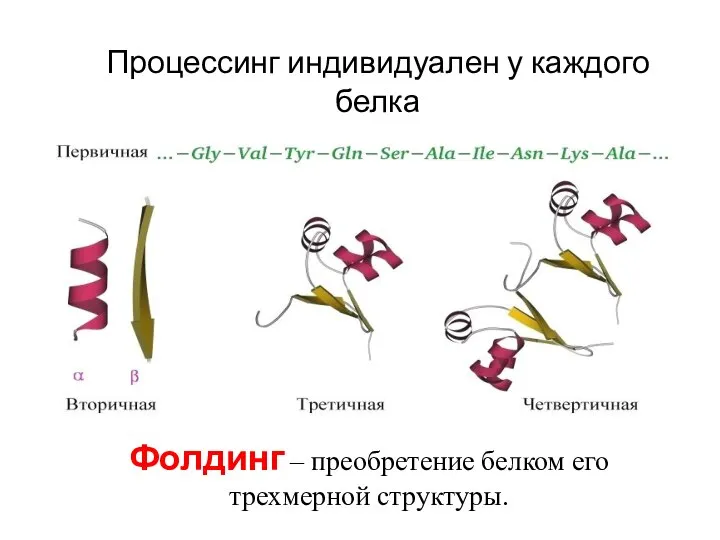
- 22. Процессинг индивидуален у каждого белка Фолдинг – преобретение белком его трехмерной структуры.
- 23. К основным реакциям процессинга белков относятся: 1. Удаление с N-конца метионина или даже нескольких аминокислот. 2.
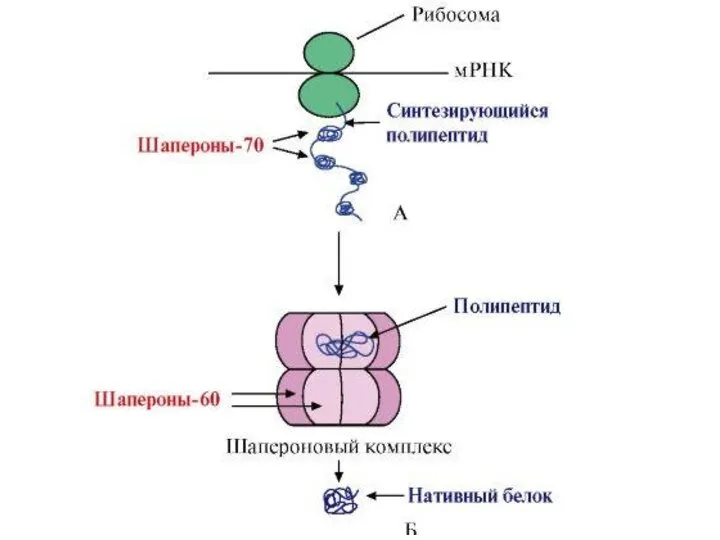
- 24. Фолдинг белков Фолдинг – это процесс укладки вытянутой полипептидной цепи в правильную трехмерную структуру. Для обеспечения
- 28. Скачать презентацию






 Обмен веществ. Питание. Пищеварение
Обмен веществ. Питание. Пищеварение Эпителиальные ткани: особенности, функции, классификация
Эпителиальные ткани: особенности, функции, классификация Птицы нашего города
Птицы нашего города Онтогенез
Онтогенез Клеточное строение организмов как доказательство их родства, единства живой природы
Клеточное строение организмов как доказательство их родства, единства живой природы Построение вариационной кривой
Построение вариационной кривой С каким цветом глаз видят лучше в темноте люди
С каким цветом глаз видят лучше в темноте люди Биогеоценоз бөлік
Биогеоценоз бөлік b58bfe068ffb4227bbe0ddb9fa139058
b58bfe068ffb4227bbe0ddb9fa139058 Осень
Осень Мочевыделительная система
Мочевыделительная система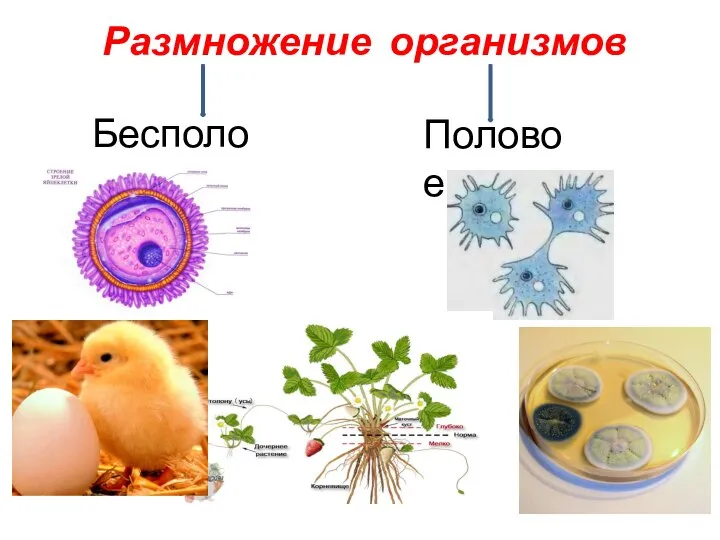 Бесполое и половое размножение организмов
Бесполое и половое размножение организмов Психофизиология. Психофизиологическая проблема
Психофизиология. Психофизиологическая проблема Неполное доминирование
Неполное доминирование геохронология 7 кл (1)
геохронология 7 кл (1) Plexus lumbosacralis
Plexus lumbosacralis Transport of gases. Regulation of respiration
Transport of gases. Regulation of respiration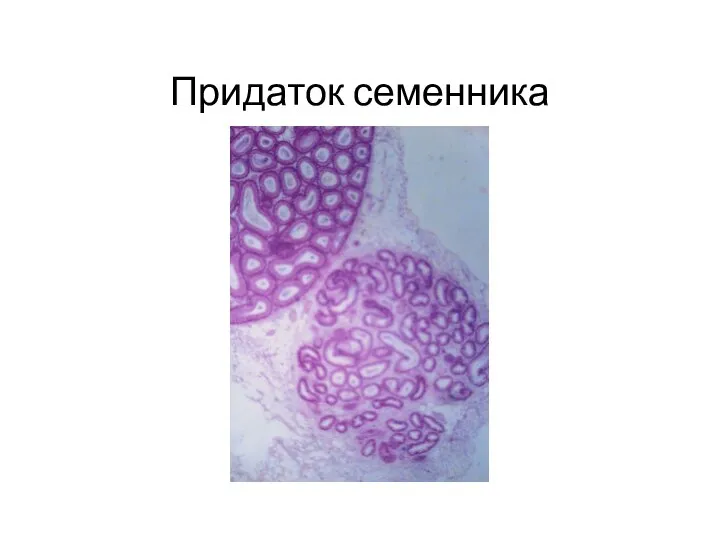 Придаток семенника
Придаток семенника Різноманітність життя
Різноманітність життя Особенности прокариотических и неклеточных организмов
Особенности прокариотических и неклеточных организмов Пища. Органы пищеварительной системы
Пища. Органы пищеварительной системы D-элементы в жизни растений
D-элементы в жизни растений Зачем человеку кожа
Зачем человеку кожа Прокариоты, грибы, растения
Прокариоты, грибы, растения Дикие животные и их детёныши
Дикие животные и их детёныши Учение И.И. Мечникова о защитных свойствах крови. Иммунитет. Виды иммунитета
Учение И.И. Мечникова о защитных свойствах крови. Иммунитет. Виды иммунитета Эндокринная система. Лекция №15
Эндокринная система. Лекция №15 11. Покрытосеменные растения
11. Покрытосеменные растения