Содержание
- 2. Открыты ферменты были в 1814 году Кирхгофом. В 1833 году это вещество было выделено из солода
- 3. В 1897 году Бухнер установил, что дрожжевой экстракт, не содержащий клеток, способен катализировать процесс спиртового брожения.
- 4. Сущность действия ферментов заключается в том, что они снижают энергию активации различных реакций. Так, для разложения
- 5. Все ферменты делятся на 2 класса: 1. Однокомпонентные - состоящие только из белка. 2. Двухкомпонентные -
- 6. Теория двухкомпонентной природы ферментов была основана Вильштеттером. Активная простетическая группа названа агон, а белковый носитель- ферон
- 7. Свойства ферментов Ферменты обладают специфичностью и обратимостью действия. Специфичность действия ферментов заключается в том, что действие
- 8. По обратному выражению Эмиля Фишера, фермент подходит к своему субстрату, так, как ключ подходит к замку.
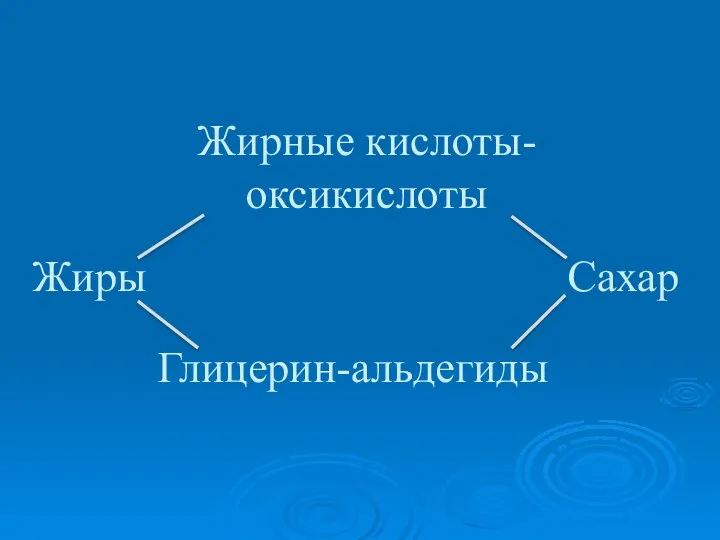
- 9. Липаза может одновременно синтезировать жир из сахара через промежуточные продукты (жирные кислоты и глицерин) и наоборот,
- 10. Жиры Глицерин-альдегиды Сахар Жирные кислоты- оксикислоты
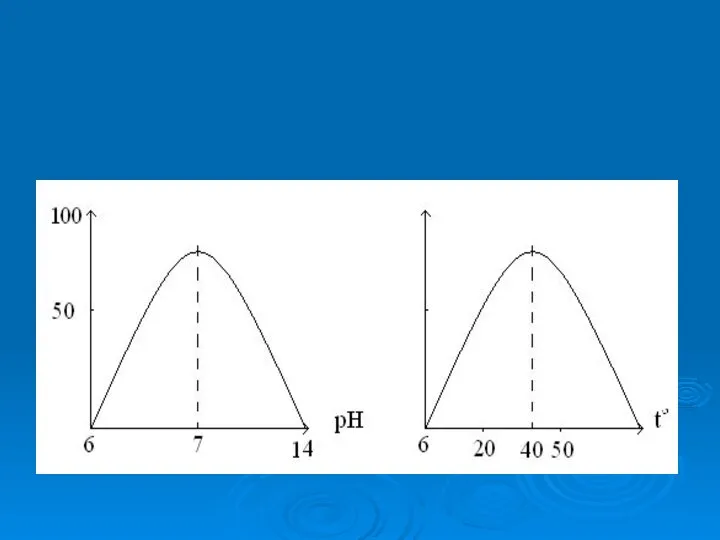
- 11. Наибольшая активность большинства растительных ферментов отмечается при слабокислой или нейтральной реакции, которая характерна для растительных клеток
- 13. Активаторы и ингибиторы. Действие ферментов очень сильно зависит от специфических активаторов и парализаторов (ингибиторов). Вещества, которые
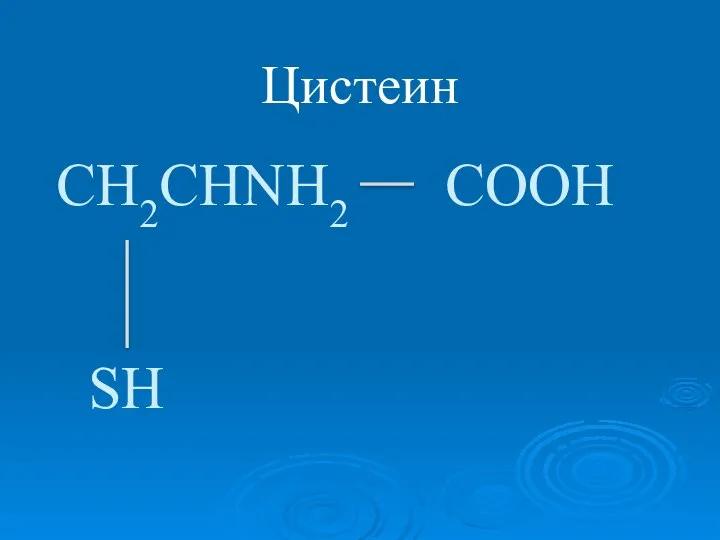
- 14. Действие многих ферментов активируется в присутствии незначительных количеств сульфгидрильных соединений содержащих группу SH.
- 15. Цистеин CН2CHNН2 COOH SH
- 16. Такими веществами являются соли тяжелых металлов (свинца, ртути, вольфрама), трихлоруксусная кислота и др.
- 17. Классификация ферментов Ферменты разделены на 6 классов. I. Оксидоредуктазы По выполняемой функции окислительно-восстановительные ферменты делятся на
- 18. 1. Дегидрогеназы - ферменты отнимающие водород от органического соединения и передающие его на другие, принимая на
- 19. Отщепление H2 от окислительных субстратов катализируется ферментами, называются дегидрогеназами АН2+В дегидр ВН2+А
- 20. Дегидрогеназы: - аэробные (оксиды) - анаэробные
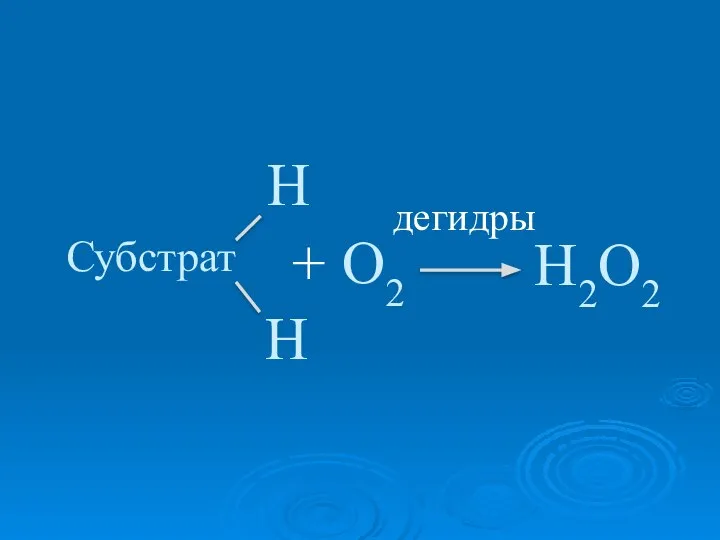
- 21. Аэробные дегидрогеназы отщепляют Н2, передают на другие акцепторы (ферменты)
- 22. Н Н O2 Н2O2 Субстрат + дегидры
- 23. 2Н2О2 каталаза 2Н2О+О2
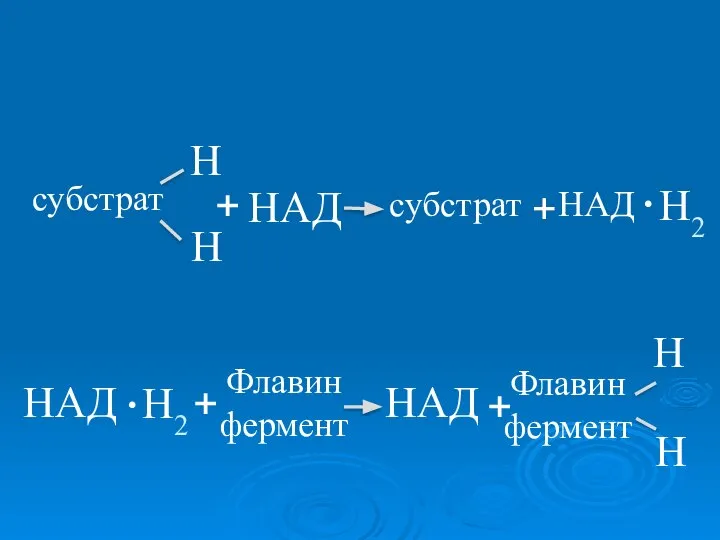
- 24. Анаэробные дегидрогеназы 2-х компонентные ферменты, у которых активная группа представлена НАД или НАДФ
- 25. субстрат Н НАД субстрат НАД Н2 Н + . НАД Н2 Флавин фермент НАД Флавин фермент
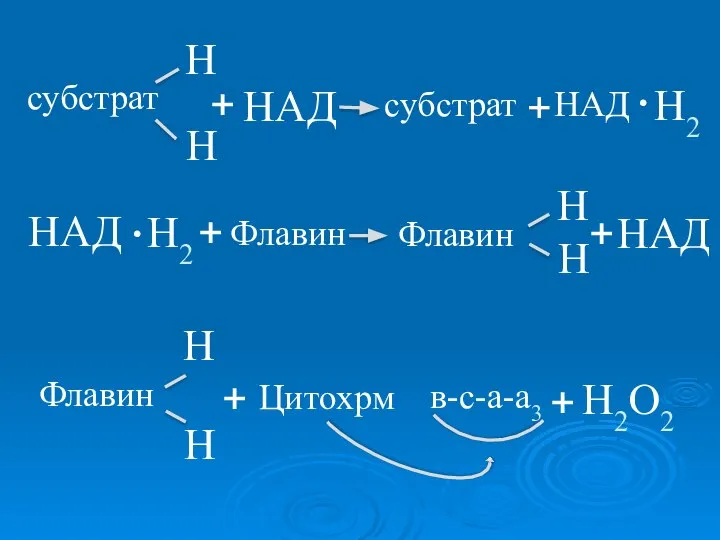
- 26. Между флавиновыми ферментами и кислородом воздуха есть еще одно промежуточное звено - цитохромная система, активная группа
- 27. субстрат Н НАД субстрат НАД Н + . Н2 НАД Н2 Флавин НАД Флавин Н Н
- 28. - осуществляют перенос радикалов, и отдельных группировок. В зависимости от того , что они транспортируют их
- 29. - ферменты, катализирующие гидролитический распад органических веществ. В зависимости от того на какие органические вещества они
- 30. Карбогидразы- довольно обширная группа участвует при распаде различных углеводов. (С6Н10О5)n амилазы nC6 Н12O6 глюкоза
- 31. Протеазы - расщепляют белки до аминокислот с накоплением небольшого количества NН3 RCO-NHR1+HOH RCOOH+R1NH2
- 32. Среди эстераз прежде всего следует отметить липазы- ферменты катализирующие гидролитическое расщепление и синтез жиров: CH2OOC-R1 CHOOCR2
- 33. Амидазы- ферменты превращающие аминокислоты (аспарагиновую и глутаминовую) в их амиды (аспарагин и глутамин) аспарагиназа COOHCH2*CHNH2COOH+NH3 аспарагиновая
- 34. глутаминаза COOHCH2 СН2CHNH2COOH+NH3 глутаминовая к-та CONH2CH2 CH2 CHNH2COOH+H2O глутамин
- 35. - ферменты катализирующие негидролитический распад органических веществ, при этом отщепляется определенная группа (молекулы углерода, воды, NH2
- 36. Фермент декорбоксилаза в результате отщепления СО2 , щавелевоуксусную кислоту переводит в пировиноградную декорбоксилаза СООНСН2СОСООН СН3СОСООН+СО2 Щ
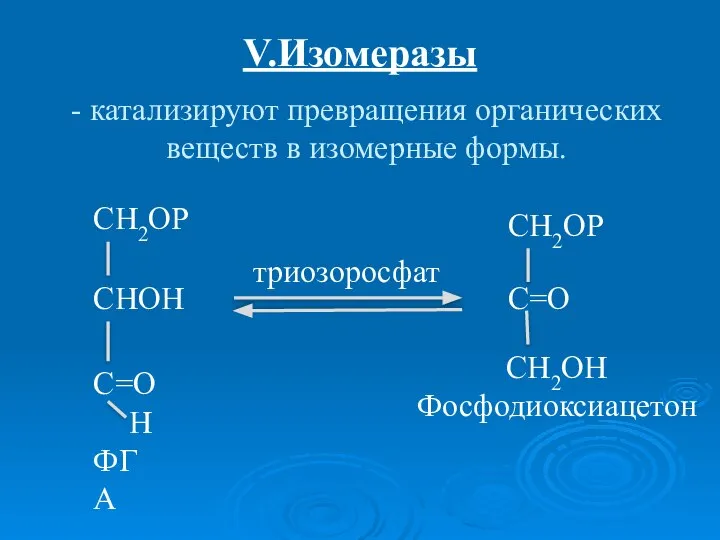
- 37. - катализируют превращения органических веществ в изомерные формы. СН2ОP СН2ОP СНOH С=O С=O H ФГА СН2ОH
- 39. Скачать презентацию





























 Свиньи. Характеристика
Свиньи. Характеристика Дыхание растений
Дыхание растений Происхождение человека. 6 класс
Происхождение человека. 6 класс 4. 1. Характеристика и систематика растений
4. 1. Характеристика и систематика растений Презентация на тему Биосфера - живая оболочка планеты
Презентация на тему Биосфера - живая оболочка планеты  Ботаника. Микология. Лишайники. Бактерии
Ботаника. Микология. Лишайники. Бактерии Подцарство одноклеточные. Тип саркодовые. Класс саркодовые
Подцарство одноклеточные. Тип саркодовые. Класс саркодовые Как прекрасен этот мир!
Как прекрасен этот мир! Анализаторы
Анализаторы Экологическое сортоиспытание гибридов арбузов в условиях Мозыркого Полесья
Экологическое сортоиспытание гибридов арбузов в условиях Мозыркого Полесья Дыхание растений. Тест
Дыхание растений. Тест Биология - наука о живой природе
Биология - наука о живой природе Клуб любителей кошек
Клуб любителей кошек Body clock
Body clock Египетская гладкошерстная кошка
Египетская гладкошерстная кошка Жизненный цикл клетки. 10 класс
Жизненный цикл клетки. 10 класс Сухопутные черепахи
Сухопутные черепахи Анатомия, физиология и патология зрительного анализатора
Анатомия, физиология и патология зрительного анализатора Презентация на тему Внешнее и внутреннее строение корня
Презентация на тему Внешнее и внутреннее строение корня  Изучение антимикробной активности слизи улитки achatina fulica
Изучение антимикробной активности слизи улитки achatina fulica Высшая нервная деятельность. Рефлексы
Высшая нервная деятельность. Рефлексы Подборка заданий линии 24 (задания 2 части ЕГЭ с ошибками в тексте) из сборников Рохлова
Подборка заданий линии 24 (задания 2 части ЕГЭ с ошибками в тексте) из сборников Рохлова Росянка (лат. Drósera)
Росянка (лат. Drósera) Презентация на тему Самые ядовитые и опасные пауки в мире
Презентация на тему Самые ядовитые и опасные пауки в мире  Презентация на тему Бактериологическое оружие и его воздействие на организм человека
Презентация на тему Бактериологическое оружие и его воздействие на организм человека  Зодіакальна система та здоров'я. Планування робочого часу. Біологічні ритми в живих системах
Зодіакальна система та здоров'я. Планування робочого часу. Біологічні ритми в живих системах Анатомия сердца
Анатомия сердца Грибы. Тест
Грибы. Тест