Содержание
- 2. Цели и задачи урока: Цель: с помощью видео-эксперимента исследовать состав, а так же некоторые физические и
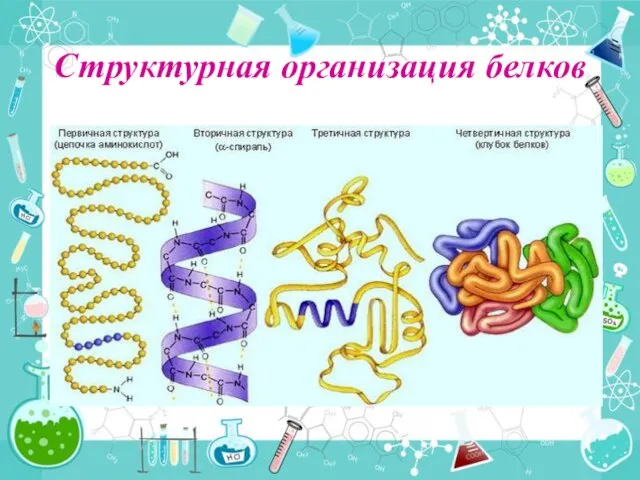
- 3. Структурная организация белков
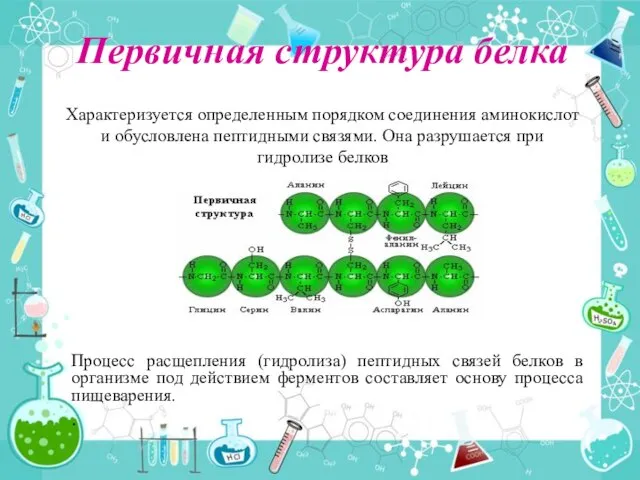
- 4. Первичная структура белка Процесс расщепления (гидролиза) пептидных связей белков в организме под действием ферментов составляет основу
- 5. Вторичная структура белка Полипептидная цепь закручивается в виде α-спирали Витки скреплены между собой водородными связями Водородные
- 6. Третичная структура белка Это трехмерная пространственная структура, образующаяся за счет взаимодействия радикалов аминокислот. Радикалы по своей
- 7. Четвертичная структура белка Состоит из нескольких полипептидных цепей. Есть не у всех белков, только самых сложных.
- 8. Состав молекул белков Предположите, какие химические элементы должны обязательно присутствовать в молекулах белков, состоящих из аминокислотных
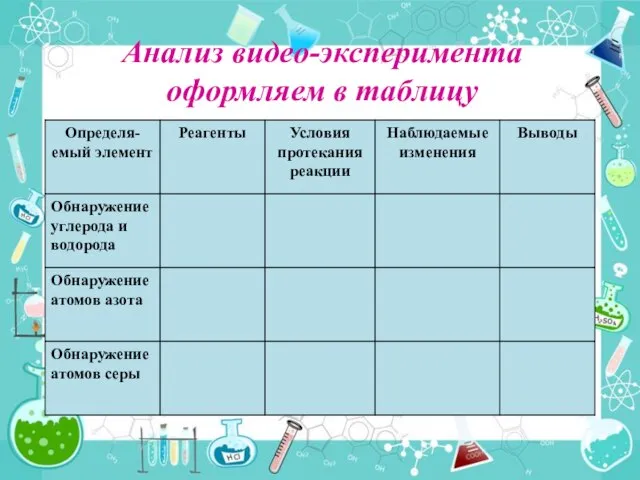
- 9. Анализ видео-эксперимента оформляем в таблицу
- 10. Внимание! Эксперимент!
- 11. Обнаружение углерода и водорода
- 12. Обнаружение атомов азота
- 13. Обнаружение атомов серы
- 14. Сверим результаты с научными данными В составе белков содержится: Углерод (51 - 53%) Кислород (21,5 –
- 15. Исследование физических свойств белков Вспомните известные вам белки (белок яйца, молочный белок, желатин и другие) Опишите
- 16. Внимание! Эксперимент!
- 17. Отношение белков к воде
- 18. Особое свойство белков Белки, содержащиеся в пищевых продуктах (зерновых, мясе, яйцах и др.), мы подвергаем тепловой
- 19. Внимание! Эксперимент!
- 20. Реакция денатурации
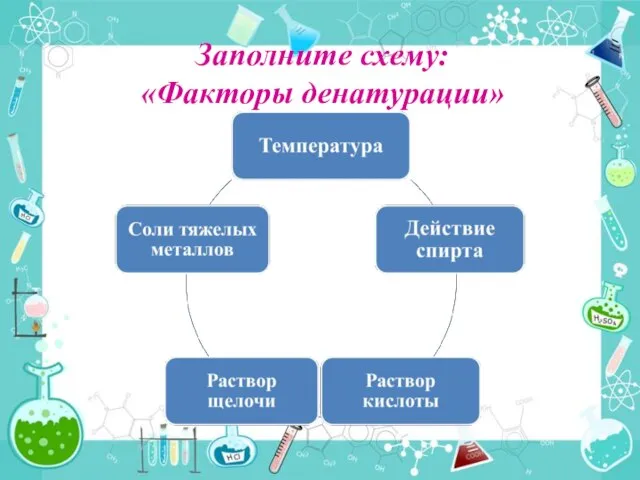
- 21. Заполните схему: «Факторы денатурации»
- 22. Качественные реакции на белки Вспомните понятие «качественной реакции»; Для каких целей используют качественные реакции? Представителям каких
- 23. Внимание! Эксперимент!
- 24. Биуретовая реакция
- 25. Ксантопротеиновая реакция
- 26. Качественные реакции Биуретовая реакция Реагенты: Видимые признаки: Ксантопротеиновая реакция Реагенты: Видимые признаки: Оформите результаты наблюдения следующим
- 27. Подведение итогов исследования С помощью эксперимента мы подтвердили качественный состав молекул белков, обнаружив в них атомы
- 28. Подведение итогов исследования В ходе эксперимента выявили факторы, вызывающие денатурацию белковых молекул. Познакомились с качественным реакциями,
- 29. Домашнее задание § 27 изучить Подготовить ответы на вопросы 3 – 8, стр. 234
- 31. Скачать презентацию























 Биологические ресурсы Земли
Биологические ресурсы Земли призентация по биологии500832462pptx (1)
призентация по биологии500832462pptx (1) Подготовка к ЕГЭ по темам Человек
Подготовка к ЕГЭ по темам Человек Витамин B1
Витамин B1 Карачаевский медведь
Карачаевский медведь Принципы разработки схем севооборотов:
Принципы разработки схем севооборотов: Презентация на тему Жизненный цикл клетки. Митоз. Амитоз (10 класс)
Презентация на тему Жизненный цикл клетки. Митоз. Амитоз (10 класс) 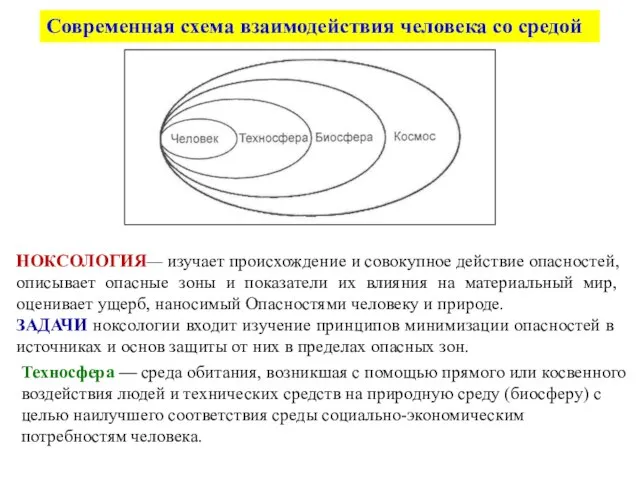 Современная схема взаимодействия человека со средой
Современная схема взаимодействия человека со средой Тыныс алу жүйесі
Тыныс алу жүйесі Подборка заданий линии 24 (задания 2 части ЕГЭ с ошибками в тексте) из сборников Рохлова
Подборка заданий линии 24 (задания 2 части ЕГЭ с ошибками в тексте) из сборников Рохлова Дополнительная литература по биологии за 6-8 классы
Дополнительная литература по биологии за 6-8 классы Характеристика царства Растения
Характеристика царства Растения Репродуктивная система человека
Репродуктивная система человека Дикие животные весной
Дикие животные весной Обучение речи антропоидов
Обучение речи антропоидов Викторина Моллюски
Викторина Моллюски Внимание (8 класс биология)
Внимание (8 класс биология) Domenii de viață pe pământ
Domenii de viață pe pământ Цитология. Клетка - универсальная единица живой материи
Цитология. Клетка - универсальная единица живой материи Образование. Фотосинтез. Симметрия. Хиральность
Образование. Фотосинтез. Симметрия. Хиральность Головной мозг (cerebrum)
Головной мозг (cerebrum)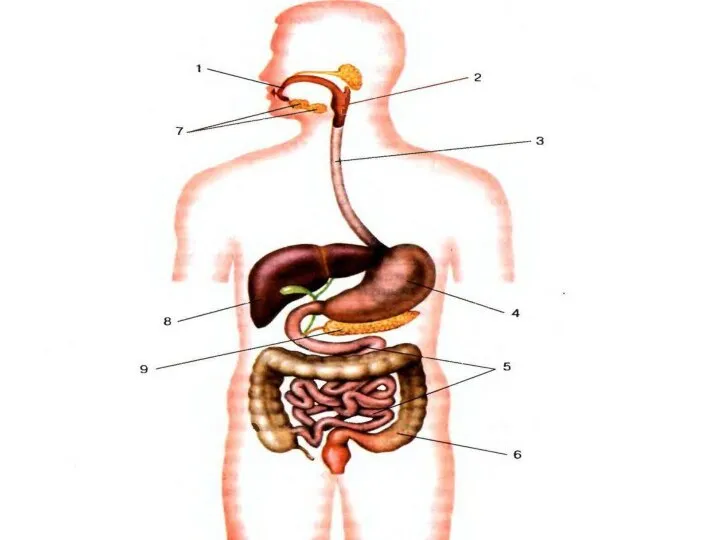 Пищеварительная система
Пищеварительная система Эти удивительные черепахи
Эти удивительные черепахи Как можно добыть энергию для жизни? Растения
Как можно добыть энергию для жизни? Растения Nocturnal animals. Day animals
Nocturnal animals. Day animals Гормональная регуляция обменных процессов: белков, воды, натрия, калия, кальция, фосфатов. Лекция № 22
Гормональная регуляция обменных процессов: белков, воды, натрия, калия, кальция, фосфатов. Лекция № 22 Skład ciala u osób trenujących i nietrenujących
Skład ciala u osób trenujących i nietrenujących Презентация на тему РАЗНООБРАЗИЕ РАСТЕНИЙ
Презентация на тему РАЗНООБРАЗИЕ РАСТЕНИЙ