Содержание
- 2. Любое исследование, проводимое с участием человека в качестве субъекта для выявления или подтверждения клинических и/или фармакологических
- 4. Немного из истории клинических исследований
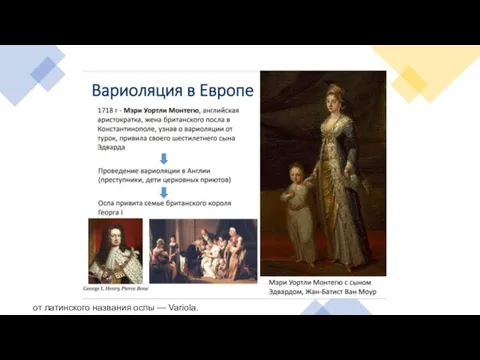
- 6. от латинского названия оспы — Variola.
- 12. Первое рандомизированное исследование Клиническое исследование с рандомизированными группами. Джеймс Линд. 1747 год 31 мая 1747 г.
- 13. 11 января 1922 года начались, в некотором смысле, первые клинически исследования . Умирающий от сахарного диабета
- 14. Первый в мире пациент, получивший инсулинотерапию, Леонард Томпсон (1908-1935 гг.). В терминальной стадии диабета на руках
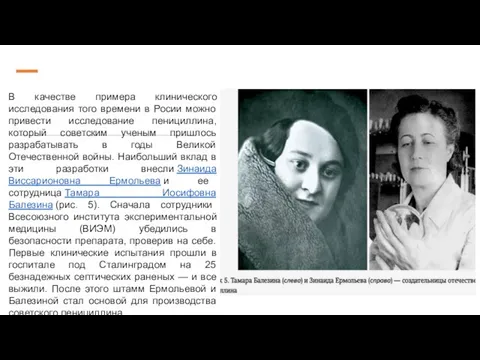
- 15. В качестве примера клинического исследования того времени в Росии можно привести исследование пенициллина, который советским ученым
- 16. Негуманный медицинский эксперимент С 1932 по 1972 год отслеживание всех стадий сифилиса на популяции Афроамериканцев. Их
- 17. Во время Второй мировой войны в концентрационных лагерях нацистской Германии проводились смертельные эксперименты. Так, в 1942–1944
- 18. Медицинские военные преступления нацистов (1939–1945) Нюрнбергский процесс по делу врачей проходил с 9 декабря 1946 по
- 19. Талидомид, 1958 В 1954 году в ходе разработки недорогого способа производства антибиотиков из пептидов немецкой фармацевтической
- 20. В 1961 году из Германии пришла страшная новость. Группа исследователей назвала талидомид причиной появления на свет
- 21. Осенью 2005 года на Трафальгарской площади в Лондоне появился очень необычная скульптура работы известного мастера Марка
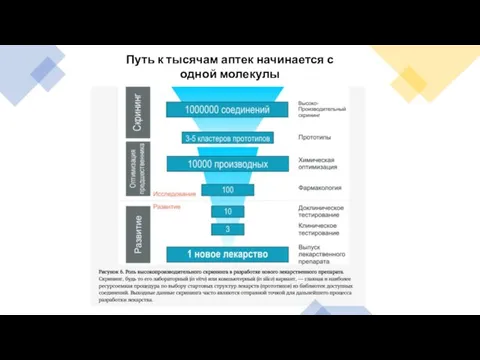
- 22. Путь к тысячам аптек начинается с одной молекулы
- 23. Итак, потребность в новом препарате налицо, найдены мишени и соединения, которые могут на них воздействовать. Что
- 39. Рандомизация (randomization, син. random allocation) Процесс распределения субъектов исследования по группам лечения или контроля случайным образом,
- 47. Сложности в применении препаратов на практике Доказательность бывает разных порядков. Классический пример неоднозначных методов — дилемма
- 48. Если данные о медицинском вмешательстве получены в небольшом числе рандомизированных исследований, в нерандомизированных исследованиях или в
- 49. В России сложилась специфическая ситуация с сертификацией медикаментов. Любому, даже самому эффективному фирменному препарату, который прошёл
- 50. Что касается российских лекарств, никакой международной сертификации они не проходят, поскольку нет задачи вывести их на
- 51. Ошибка выжившего, или Почему мы порой делаем неправильные выводы Ошибка выжившего — это когнитивная ошибка восприятия
- 52. «После» не значит «вследствие» «После этого — значит по причине этого» (лат. post hoc ergo propter
- 53. Сбор и обработка информации о побочных эффектах, осложнениях лечения, качестве жизни больных, выбывании пациентов из исследования
- 55. Пара слов о дженериках Дженерики, или генерики, — это препараты-аналоги, которые можно выпускать после того, как
- 56. Наконец-то в аптеки и больницы Патент защищает новое лекарство от копирования, но еще не дает права
- 57. И это еще не все Новый препарат поступил в аптеки, теперь врачи могут назначать его пациентам,
- 58. Силденафиловая эпопея В 1989 году в лабораториях компании Pfizer был создан новый потенциальный лекарственный препарат —
- 60. Скачать презентацию


















































 Класс млекопитающие
Класс млекопитающие Сравнительная характеристика внутренних систем организма животных различных классов, 7 класс
Сравнительная характеристика внутренних систем организма животных различных классов, 7 класс Комнатные растения в интерьере квартиры урок технологии в 6 классе
Комнатные растения в интерьере квартиры урок технологии в 6 классе ОГЭ 2020 год
ОГЭ 2020 год Витаминная азбука
Витаминная азбука Породы декоративных крыс
Породы декоративных крыс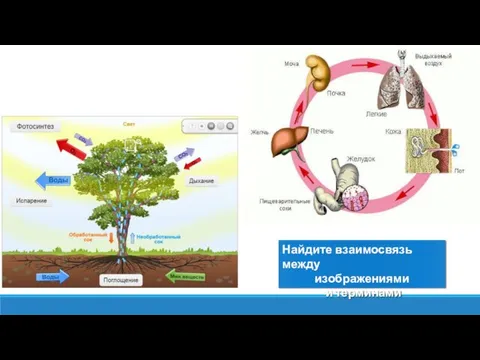 Значение выделения в жизни организмов. Продукты выделения
Значение выделения в жизни организмов. Продукты выделения Презентация на тему Семейство Сложноцветные
Презентация на тему Семейство Сложноцветные  Ботаника. Зоология. Экология. Человек
Ботаника. Зоология. Экология. Человек Основы генетики
Основы генетики Влияние природных условий на характер питания человека
Влияние природных условий на характер питания человека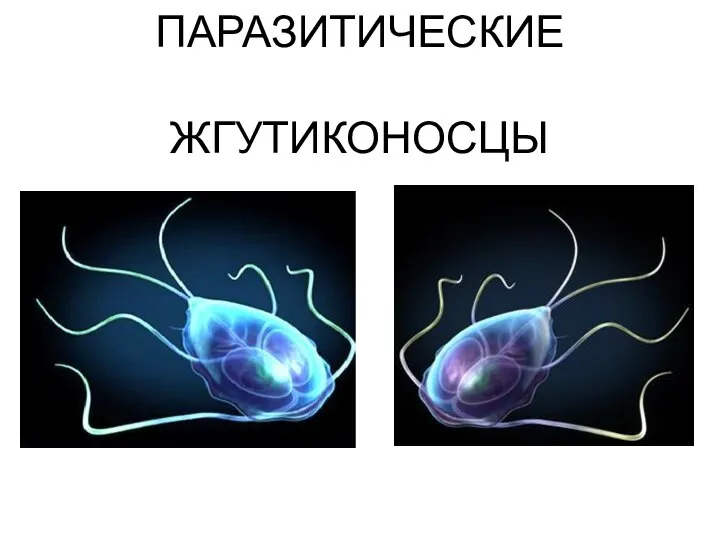 Паразитические жгутиконосцы
Паразитические жгутиконосцы Питание, увлажнение кожи. Защита кожи
Питание, увлажнение кожи. Защита кожи Органы растений. Строение побега
Органы растений. Строение побега Физиология автономной нервной системы
Физиология автономной нервной системы Электрические скаты
Электрические скаты Вычисление линейного увеличения клеток
Вычисление линейного увеличения клеток Лучевая болезнь. Патофизиология воздействия ионизирующего излучения
Лучевая болезнь. Патофизиология воздействия ионизирующего излучения Краски осени
Краски осени Животные в истории
Животные в истории Внешнее строение птиц. Опорно-двигательная система птиц
Внешнее строение птиц. Опорно-двигательная система птиц Презентация на тему Скорпионы
Презентация на тему Скорпионы  Тип Губки
Тип Губки Растения и животные Африки
Растения и животные Африки organoidy_kletki
organoidy_kletki Ах, картошка, объеденье
Ах, картошка, объеденье Транскрипция - биосинтез РНК на матрице ДНК
Транскрипция - биосинтез РНК на матрице ДНК Здравствуй, птичья страна!
Здравствуй, птичья страна!