Слайд 2Участие водородных связей в формировании вторичной структуры
Укладка белка в виде α-спирали
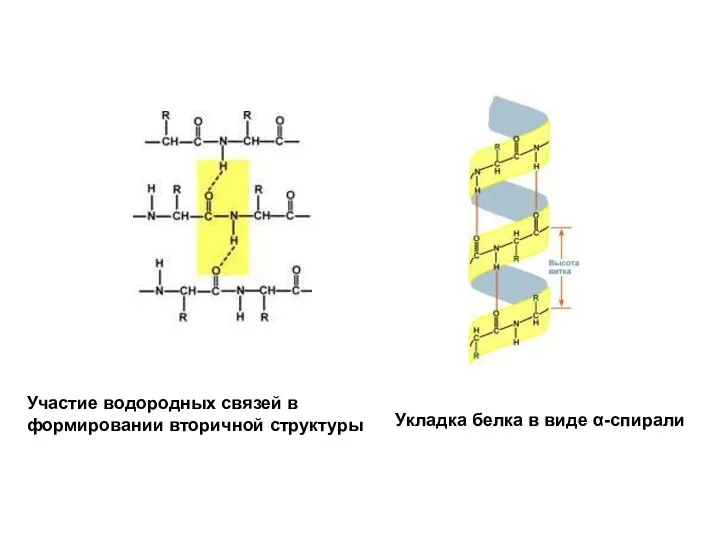
Слайд 3Укладка белка в виде β-складчатого слоя
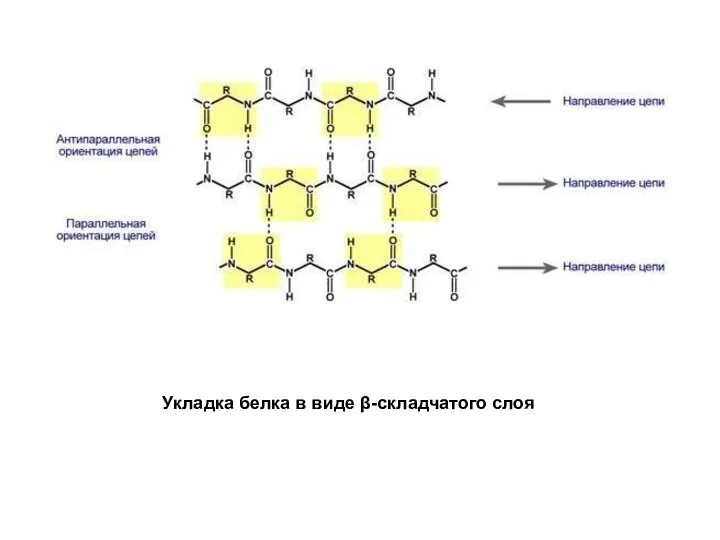
Слайд 4Супервторичная структура в виде α/β-бочонка. А - триозофосфатизомераза; Б - домен пируваткиназы.
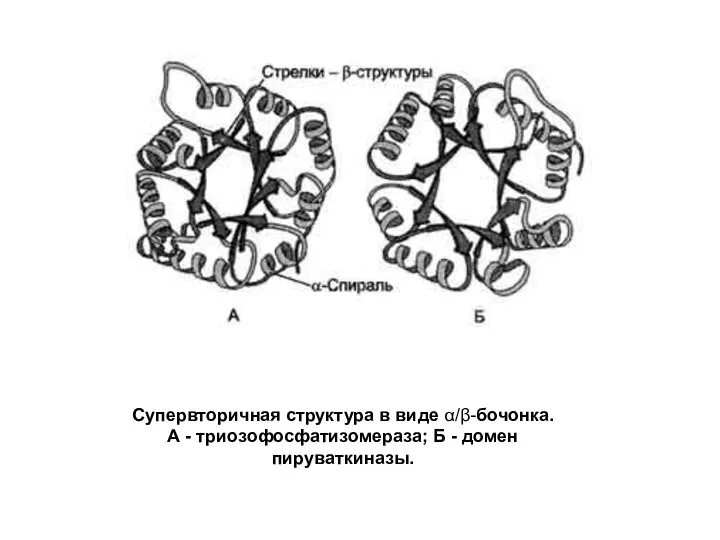
Слайд 5Связывание супервторичной структуры "α-спираль-поворот-α-спираль" ДНК-связывающего белка в большой бороздке ДНК.
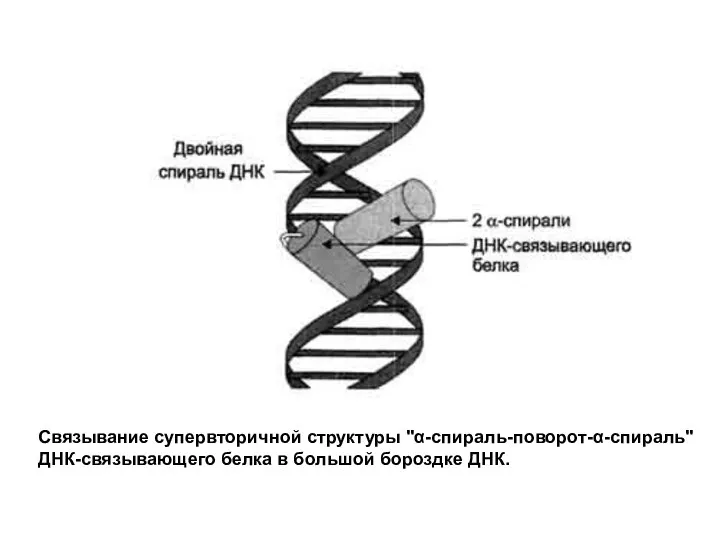
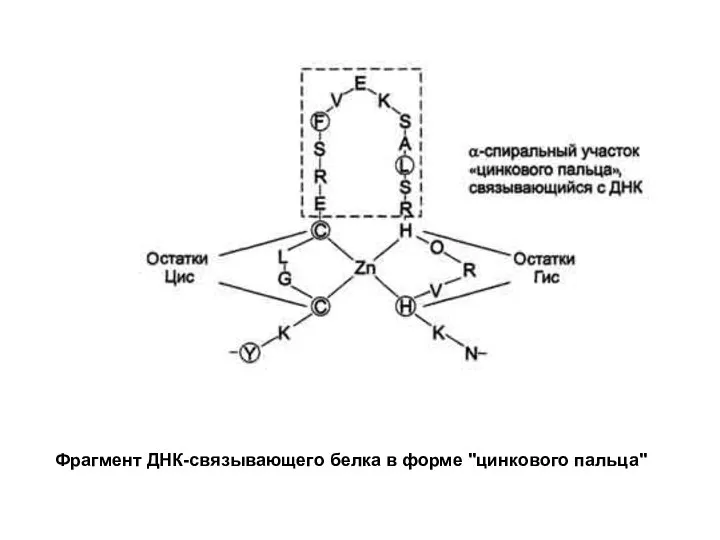
Слайд 6Фрагмент ДНК-связывающего белка в форме "цинкового пальца"
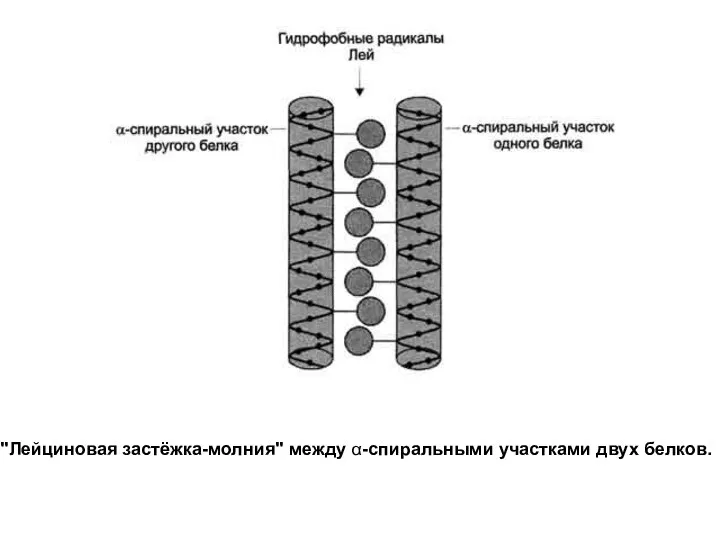
Слайд 7"Лейциновая застёжка-молния" между α-спиральными участками двух белков.
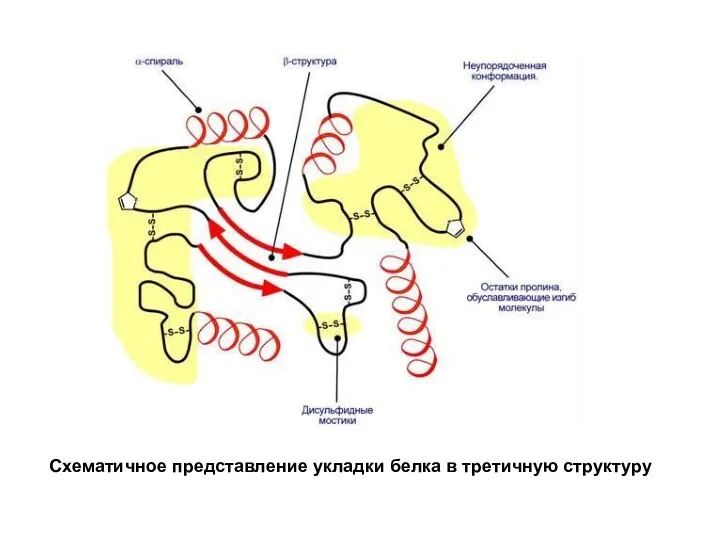
Слайд 8Схематичное представление укладки белка в третичную структуру
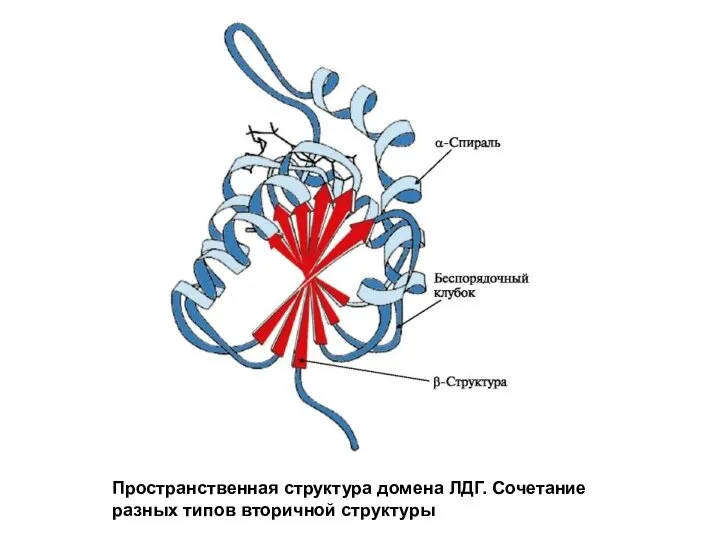
Слайд 9Пространственная структура домена ЛДГ. Сочетание разных типов вторичной структуры
Слайд 10Локализация гидрофобных и гидрофильных радикалов в молекуле белка
А - гидрофильный цитоплазматический белок;
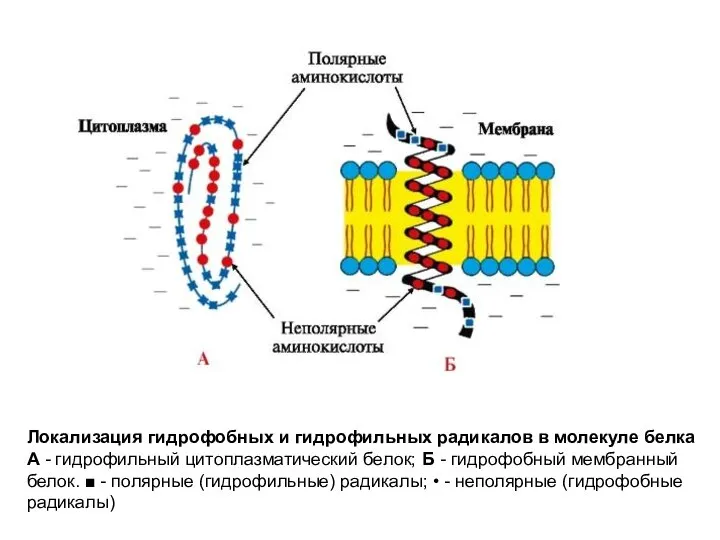
Б - гидрофобный мембранный белок. ■ - полярные (гидрофильные) радикалы; • - неполярные (гидрофобные радикалы)
Слайд 11Структурные уровни белковой молекулы
Четвертичная (IV) структура белка - пространственное взаиморасположение нескольких полипептидных
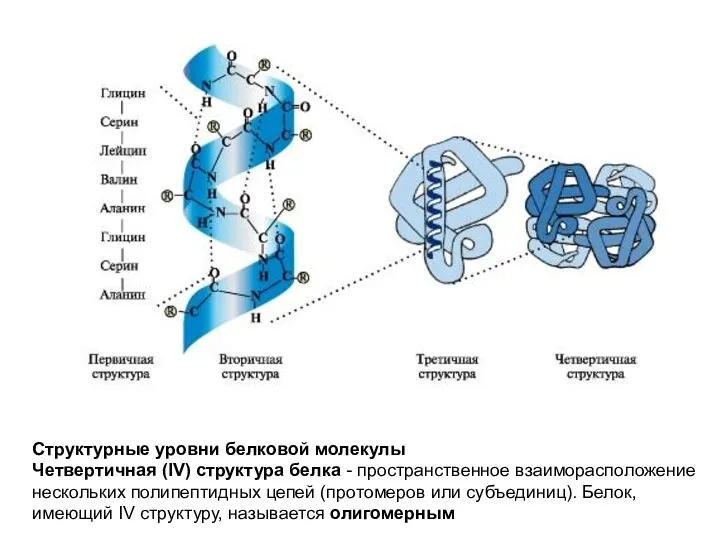
цепей (протомеров или субъединиц). Белок, имеющий IV структуру, называется олигомерным
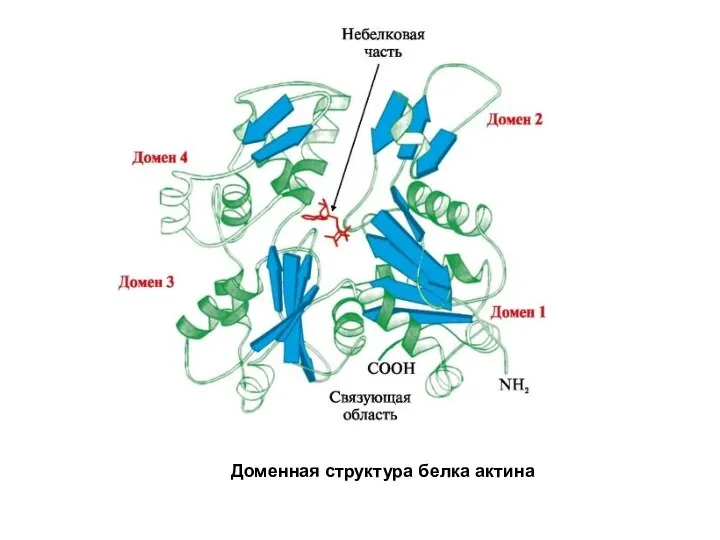
Слайд 12Доме́н белка́ – элемент третичной структуры белка, представляющий собой достаточно стабильную и

независимую подструктуру белка, чей фолдинг проходит независимо от остальных частей. В состав домена обычно входит несколько элементов вторичной структуры. В белке домены выполняют какую-либо его функцию (например, цитоплазматический домен, трансмембранный домен и т.п.).
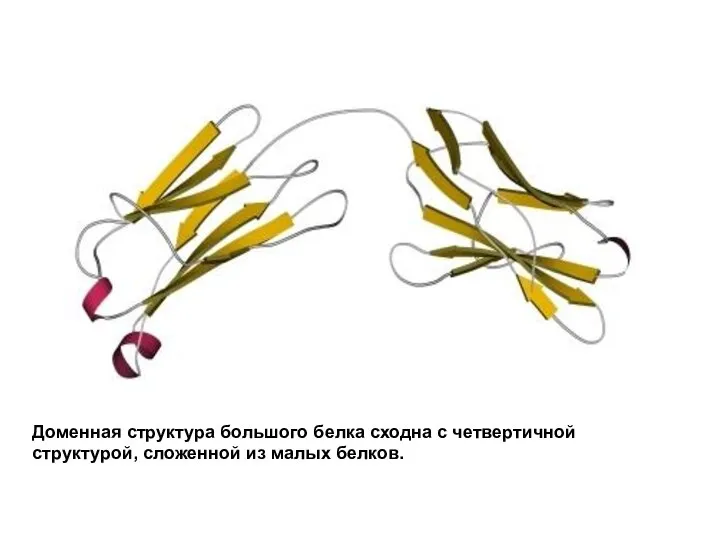
Слайд 13Доменная структура большого белка сходна с четвертичной структурой, сложенной из малых белков.
Слайд 18Заряд и растворимость альбумина (содержит много дикарбоновых аминокислот) при разных значениях рН
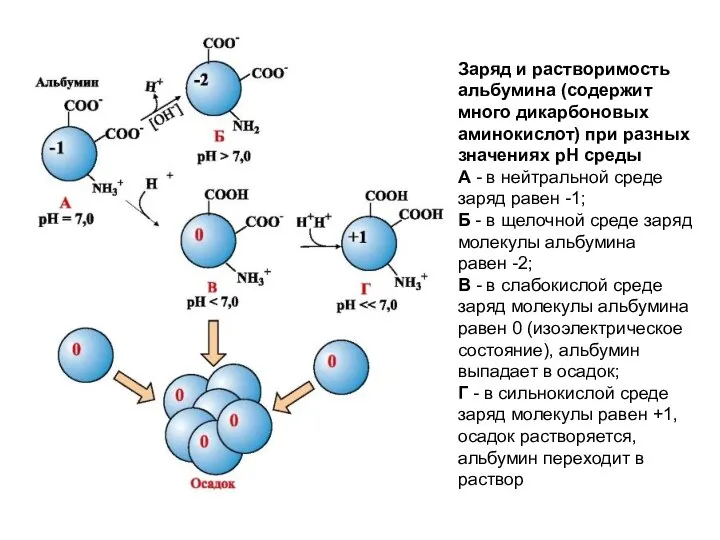
среды
А - в нейтральной среде заряд равен -1;
Б - в щелочной среде заряд молекулы альбумина
равен -2;
В - в слабокислой среде заряд молекулы альбумина равен 0 (изоэлектрическое состояние), альбумин выпадает в осадок;
Г - в сильнокислой среде заряд молекулы равен +1, осадок растворяется, альбумин переходит в раствор
Слайд 19Денатурация белковой молекулы (схема).
а - исходное состояние; б - начинающееся обратимое нарушение
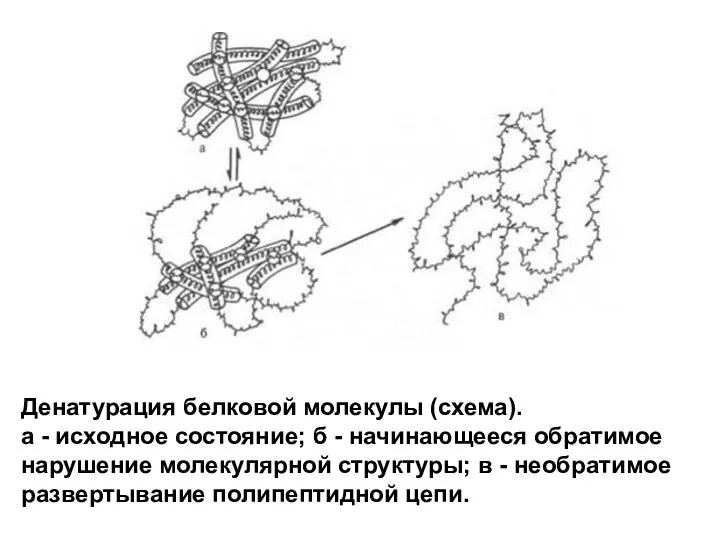
молекулярной структуры; в - необратимое развертывание полипептидной цепи.
Слайд 20Денатурация и ренативация рибонуклеазы
А - нативная молекула рибонуклеазы, в третичной структуре которой
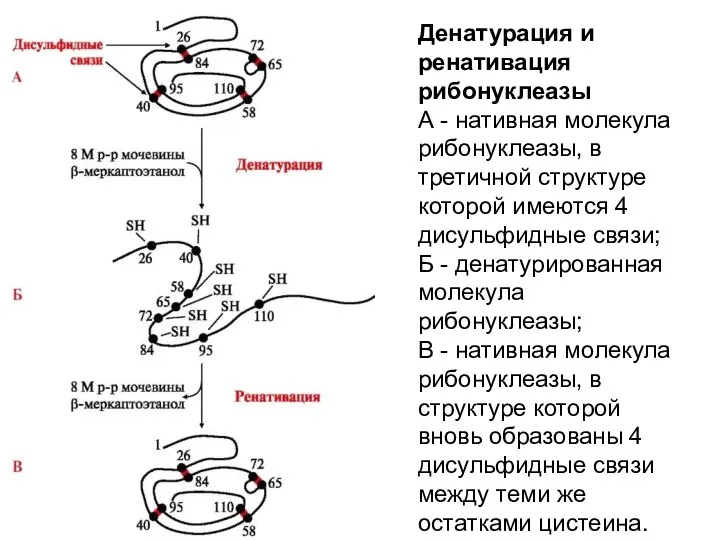
имеются 4 дисульфидные связи;
Б - денатурированная молекула рибонуклеазы;
В - нативная молекула рибонуклеазы, в структуре которой вновь образованы 4 дисульфидные связи между теми же остатками цистеина.


















 Анатомия и физиология. Общие характеристики
Анатомия и физиология. Общие характеристики Мхи и лишайники
Мхи и лишайники 3_pischevarenie
3_pischevarenie Роль запахов в мире животных
Роль запахов в мире животных Физиология автономной нервной системы
Физиология автономной нервной системы Всё о кошках и моей Муси…
Всё о кошках и моей Муси… Они такие разные, бывают и опасные
Они такие разные, бывают и опасные Отдел мхи. Кукушкин лен
Отдел мхи. Кукушкин лен Половое размножение покрытосеменных растений
Половое размножение покрытосеменных растений Биосфера-оболочка земли, состав, структура и свойства
Биосфера-оболочка земли, состав, структура и свойства Сцепленное наследование генов и кроссинговер
Сцепленное наследование генов и кроссинговер Тест: растения луга
Тест: растения луга Лилейные и злаковые растения
Лилейные и злаковые растения Размножение и развитие растений. Опыление
Размножение и развитие растений. Опыление История развития науки о клетке. Клеточная теория
История развития науки о клетке. Клеточная теория Социально-экономические факторы разнообразия растений в городе
Социально-экономические факторы разнообразия растений в городе Солнце, растения и мы с вами
Солнце, растения и мы с вами Партеногенез. Гиногенез. Андрогенез
Партеногенез. Гиногенез. Андрогенез Деление клетки. Митоз
Деление клетки. Митоз Метод, позволяющий амплифицировать ДНК в ходе многократных последовательных удвоений исходной молекулы ДНК
Метод, позволяющий амплифицировать ДНК в ходе многократных последовательных удвоений исходной молекулы ДНК Мужская половая система (МПС)
Мужская половая система (МПС) Представители животного сообщества абиссали
Представители животного сообщества абиссали Общая характеристика одноклеточных
Общая характеристика одноклеточных Отдел Голосеменные растения. Общая характеристика и значение
Отдел Голосеменные растения. Общая характеристика и значение Экспрессия генов
Экспрессия генов Борьба за существование
Борьба за существование Витамины и их значение для организма
Витамины и их значение для организма Генная и клеточная инженерия
Генная и клеточная инженерия