Содержание
- 2. ДАВЛЕНИЕ ГАЗА — сила, с которой давит газ, стремясь к расширению под действием теплового движения его
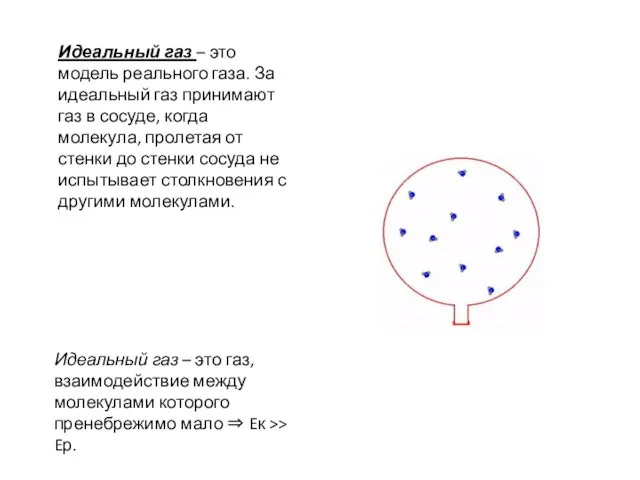
- 3. Идеальный газ – это модель реального газа. За идеальный газ принимают газ в сосуде, когда молекула,
- 4. Основное уравнение МКТ связывает макроскопические параметры (давление p, объём V, температура T, масса m) газовой системы
- 5. Уравнение состояния идеального газа — формула, устанавливающая зависимость между давлением, объёмом и абсолютной температурой идеального газа,
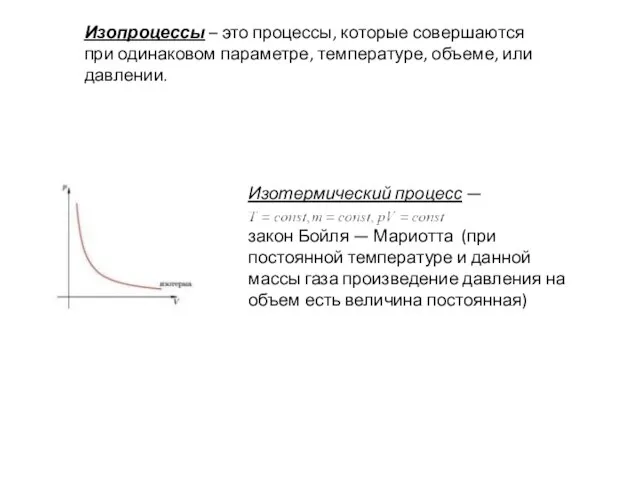
- 6. Изопроцессы – это процессы, которые совершаются при одинаковом параметре, температуре, объеме, или давлении. Изотермический процесс —
- 7. Изобарный процесс — — закон Гей-Люссака (при постоянном давлении для данной массы газа отношение объема к
- 8. Вывели газовые законы из уравнения Менделеева — Клапейрона. Но исторически всё было наоборот: газовые законы были
- 9. Источники: http://kaplio.ru/davlenie-gaza-uravnenie-mendeleeva-klapejrona-izoprotsessy/ https://studopedia.ru/9_73036_davlenie-gaza-uravnenie-sostoyaniya-idealnogo-gaza-uravnenie-mendeleeva-klapeyrona-izoprotsessi.html
- 11. Скачать презентацию






 Презентация на тему Однофазный мостовой выпрямитель
Презентация на тему Однофазный мостовой выпрямитель  Изменение агрегатных состояний вещества. Решение задач
Изменение агрегатных состояний вещества. Решение задач Сущность и применение метода импеданса с помощью прибора БакТрак для определения различных групп микроорганизмов
Сущность и применение метода импеданса с помощью прибора БакТрак для определения различных групп микроорганизмов Задания
Задания Многофункциональная система обслуживания придомовых территорий
Многофункциональная система обслуживания придомовых территорий Свободные и вынужденные электромагнитные колебания
Свободные и вынужденные электромагнитные колебания Электризация тел. Электрический заряд. Закон сохранения электрического заряда
Электризация тел. Электрический заряд. Закон сохранения электрического заряда Где живет электричество? 8 класс
Где живет электричество? 8 класс Механические колебания
Механические колебания Кинематика. Движение твердой среды
Кинематика. Движение твердой среды Теплоемкость. Модель Дебая. Закон Дебая. Экспериментальные методы исследований фононного спектра
Теплоемкость. Модель Дебая. Закон Дебая. Экспериментальные методы исследований фононного спектра Воздухораспределитель усл.№292-001
Воздухораспределитель усл.№292-001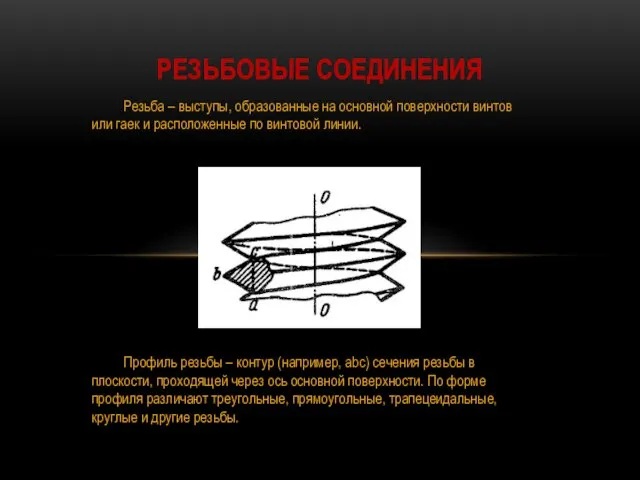 Порядок решения задач на резьбовые соединения
Порядок решения задач на резьбовые соединения Ядерное оружие
Ядерное оружие Применение частотного метода регулирования скорости вращения асинхронного двигателя
Применение частотного метода регулирования скорости вращения асинхронного двигателя Радіо. Історія виникнення радіозв'язку
Радіо. Історія виникнення радіозв'язку Случайности не случайны! А вас бьет током? 4 класс
Случайности не случайны! А вас бьет током? 4 класс Мобильный микроманипулятор для экстремальных климатических условий
Мобильный микроманипулятор для экстремальных климатических условий Механическая работа
Механическая работа Уравнения переменного тока. Задачи
Уравнения переменного тока. Задачи Электромагнитные волны
Электромагнитные волны Электромагнитные колебания
Электромагнитные колебания Проект Прорыв – создание Опытно-демонстрационного энергокомплекса
Проект Прорыв – создание Опытно-демонстрационного энергокомплекса Вес тела. Единицы силы. Связь между силой тяжести и массой тела
Вес тела. Единицы силы. Связь между силой тяжести и массой тела Законы Ньютона
Законы Ньютона Механические колебания
Механические колебания Обеспечение высокого уровня технического обслуживания и текущего ремонта грузового транспорта в условиях предприятия
Обеспечение высокого уровня технического обслуживания и текущего ремонта грузового транспорта в условиях предприятия Аэродинамика Т 5-1
Аэродинамика Т 5-1