Слайд 2МЕТОД РОЗДІЛЕННЯ І КОНЦЕНТРУВАННЯ
Потреба:
проба містить компоненти, які заважають визначенню;
концентрація досліджуваного

компонента нижче за межу виявлення методу;
досліджувані компоненти нерівномірно розподілені в пробі;
відсутні стандартні зразки для калібрування приладів;
проба високотоксична, радіоактивна або вартісна.
Слайд 3ВИЗНАЧЕННЯ:
Розділення – це операція (процес), у результаті якого компоненти, що входять до

вихідної суміші, віддаляються один від одного.
Концентрування – операція (процес), у результаті якого підвищується відношення концентрації або кількості мікрокомпонентів до концентрації або кількості макрокомпонентів.
Слайд 4СПОСОБИ КОНЦЕНТРУВАННЯ:
екстракція;
випаровування;
осадження;
кристалізація;
вибіркова адсорбція;
озолення;
перегонка.

Слайд 5СПОСОБИ РОЗДІЛЕННЯ:
осадження;
екстракція;
хроматографічні методи;
перегонка.

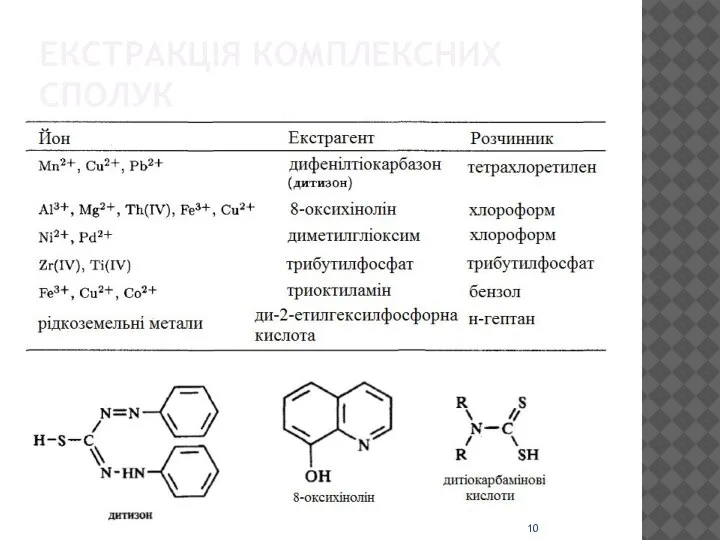
Слайд 6ЕКСТРАКЦІЯ
Екстракція – це фізико-хімічний процес розподілу речовин між двома рідкими фазами, які

не змішуються між собою.
Екстрагент – органічна фаза або розчин реагенту в органічній фазі, який утворює екстраговані сполуки.
Екстракт – органічна фаза, що відокремлена від водної фази після екстракції та містить екстраговані речовини.
Реекстракція – зворотній процес переходу речовини з органічної фази у водну.
Слайд 7УМОВ ЕКСТРАКЦІЇ РЕЧОВИН:
молекули речовини можуть переходити через межу розділу рідких фаз

в органічний розчинник тільки у незарядженому стані; для переходу через межу розділу фаз у молекули повинна зруйнуватися гідратна оболонка і утворитися сольватна;
екстракція можлива, якщо розчинність досліджуваної сполуки в органічному розчиннику є вищою, ніж у воді; чим більшою є енергія сольватації і меншою енергія гідратації, тим вищим є ступінь екстракції;
щоб йони металів та інші заряджені частинки перейшли в органічну фазу, необхідно нейтралізувати їх заряд; йони металів можна зв’язати у незаряджений комплекс; комплекси, які мають заряд, можна екстрагувати як йонні асоціати.
Слайд 8УМОВ ЕКСТРАКЦІЇ РЕЧОВИН:
для полегшення переходу речовини в органічний розчинник необхідно зменшити

гідрофільність цієї речовини; як правило, гідрофільність органічної сполуки визначається наявністю в її молекулі таких груп: -SO3H, -COOH, -OH та ін.;
зі збільшенням розміру органічних молекул екстрагованої сполуки ступінь її гідратації переважно зростає, оскільки великі молекули погано гідратуються; хелатні комплекси йонів металів є достатньо об’ємними, а їх ліганд може блокувати гідрофільну частину молекули;
при екстракції йонних асоціатів важливими є заряд і розмір їх йонів; ступінь екстракції йонних асоціатів зростає зі зменшенням заряду йонів і збільшенням їх розміру;
комплекси із низьким значенням константи нестійкості екстрагуються краще.
Слайд 9ЗАКОН НЕРНСТА
Речовина розподіляється між двома фазами, що не змішуються, таким чином, що
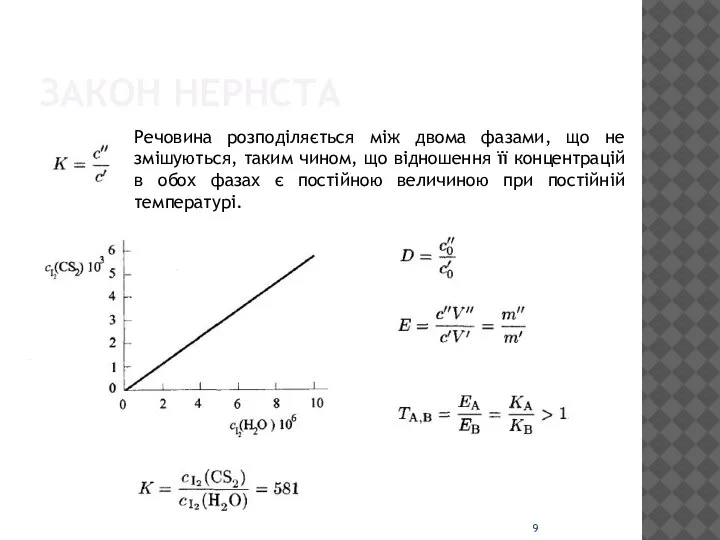
відношення її концентрацій в обох фазах є постійною величиною при постійній температурі.








 Кинематика. Движение твердой среды
Кинематика. Движение твердой среды Классическая теория излучения. Общая теория Максвелла — Лоренца
Классическая теория излучения. Общая теория Максвелла — Лоренца Статика. Условие равновесия
Статика. Условие равновесия Электромагнитная индукция
Электромагнитная индукция Электрические явления
Электрические явления Давление твердых тел. 7 класс
Давление твердых тел. 7 класс Выполнение подготовки центробежного нагнетателя к ремонту
Выполнение подготовки центробежного нагнетателя к ремонту Лестница знаний
Лестница знаний Сила Архимеда
Сила Архимеда Постоянный ток. Сила тока. Сопротивление. Закон Ома для участка цепи. Виды соединения проводников
Постоянный ток. Сила тока. Сопротивление. Закон Ома для участка цепи. Виды соединения проводников Проверочные вопросы по теме Этапы работы над исследовательским проектом
Проверочные вопросы по теме Этапы работы над исследовательским проектом Что изучает физика!
Что изучает физика! Презентация на тему Второй закон Ньютона
Презентация на тему Второй закон Ньютона  Моделирование аксиально-поршневой гидромашины с раздельными цилиндрами
Моделирование аксиально-поршневой гидромашины с раздельными цилиндрами Санитарно-гигиенический контроль за микроклиматом помещений аптек
Санитарно-гигиенический контроль за микроклиматом помещений аптек Расчёт коэффициента торможения (Лекция 2)
Расчёт коэффициента торможения (Лекция 2) Хроматическая аберрация. (Лекция 33)
Хроматическая аберрация. (Лекция 33) Принцип Гюйгенса-Френеля
Принцип Гюйгенса-Френеля Магнитное поле Земли
Магнитное поле Земли Биомехатронные системы. Лекция 1. Двойной маятник
Биомехатронные системы. Лекция 1. Двойной маятник Неразъемные соединения
Неразъемные соединения Презентация на тему Опытная проверка закона Гей - Люссака
Презентация на тему Опытная проверка закона Гей - Люссака  Пути увеличения скорости водоизмещающего судна
Пути увеличения скорости водоизмещающего судна Електричні двигуни
Електричні двигуни Механические передачи. Общие понятия о цилиндрических передачах. Лекция №2
Механические передачи. Общие понятия о цилиндрических передачах. Лекция №2 Магнитное поле
Магнитное поле Презентация на тему Применение фотоэффекта в солнечных батареях
Презентация на тему Применение фотоэффекта в солнечных батареях  Контроль – измерительные приборы и автоматика (для операторов ТХУ)
Контроль – измерительные приборы и автоматика (для операторов ТХУ)