Содержание
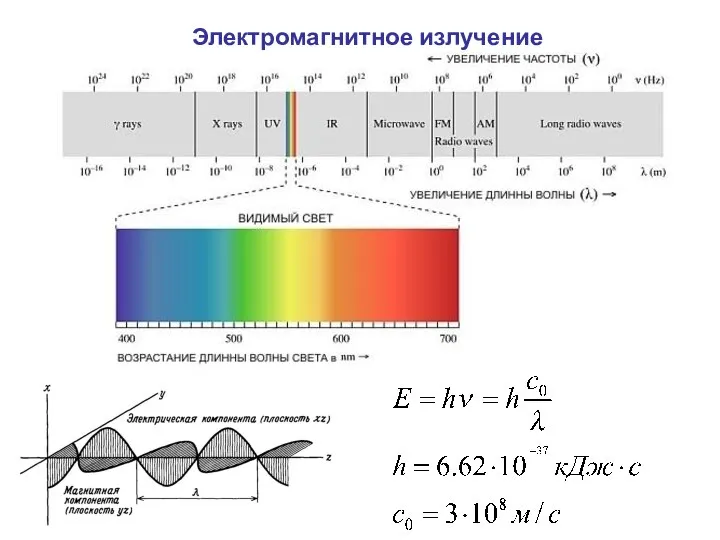
- 2. Электромагнитное излучение
- 3. Виды молекулярной спектроскопии
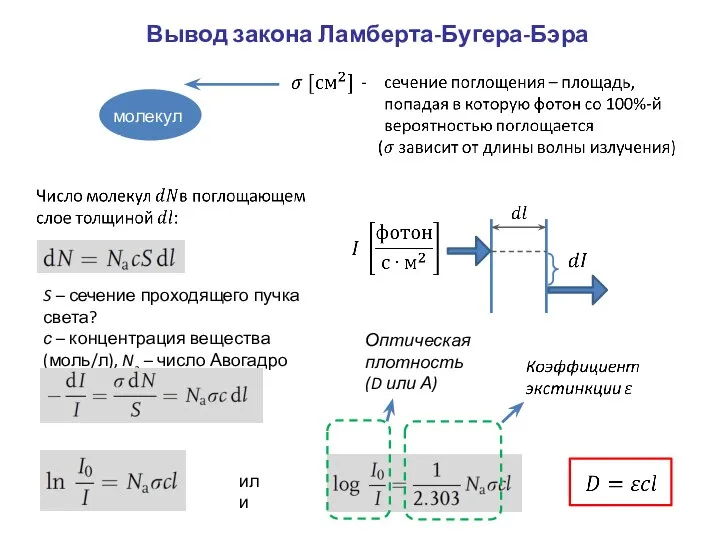
- 4. Вывод закона Ламберта-Бугера-Бэра молекула или Оптическая плотность (D или А)
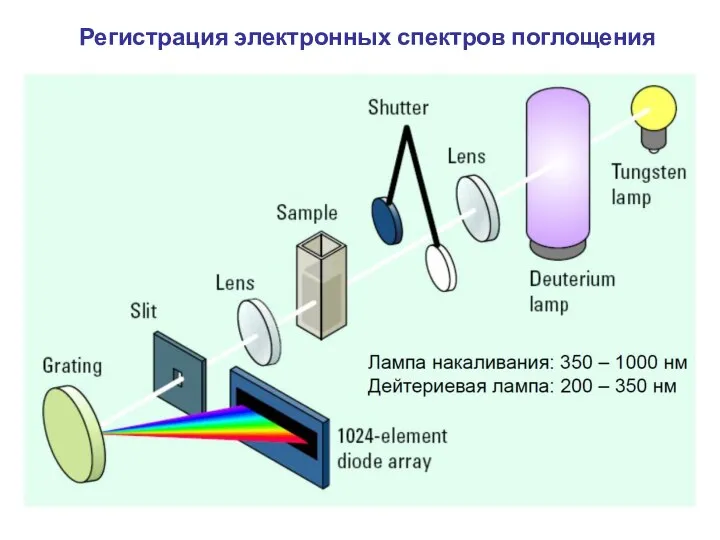
- 5. Регистрация электронных спектров поглощения
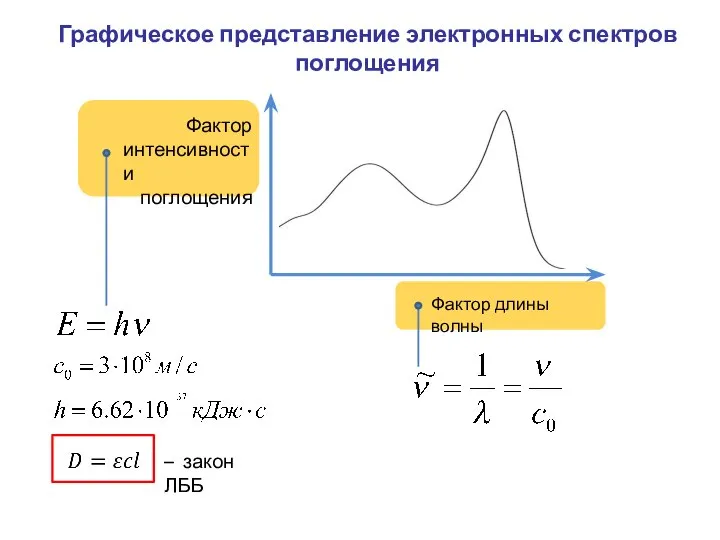
- 6. Фактор интенсивности поглощения Фактор длины волны Графическое представление электронных спектров поглощения
- 7. M ~100 г/моль ε ~ 10000 l = 1 см А = 0.3 – 0.9 Концентрация
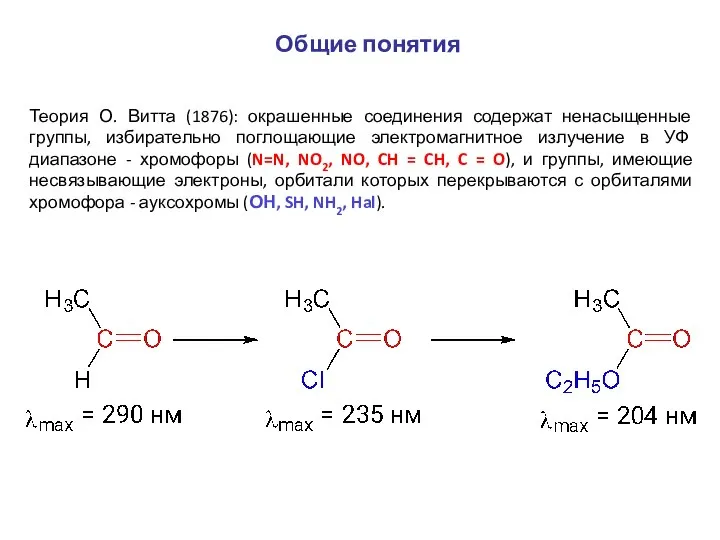
- 8. Общие понятия Теория О. Витта (1876): окрашенные соединения содержат ненасыщенные группы, избирательно поглощающие электромагнитное излучение в
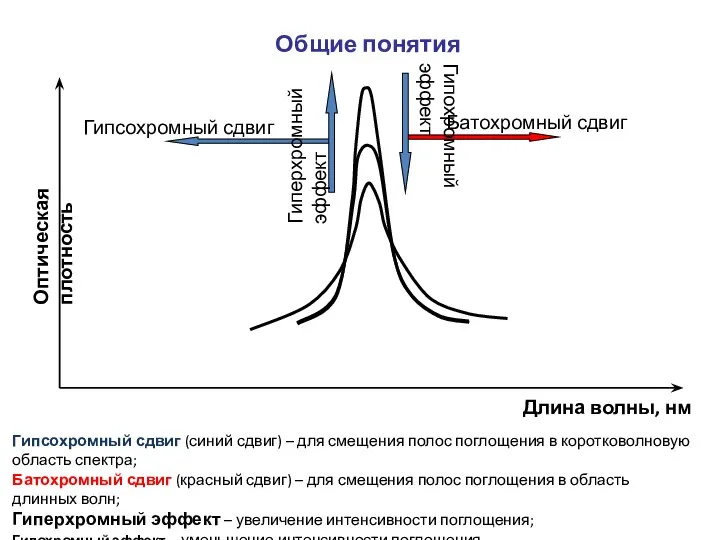
- 9. Гипсохромный сдвиг Батохромный сдвиг Гиперхромный эффект Гипохромный эффект Длина волны, нм Оптическая плотность Гипсохромный сдвиг (синий
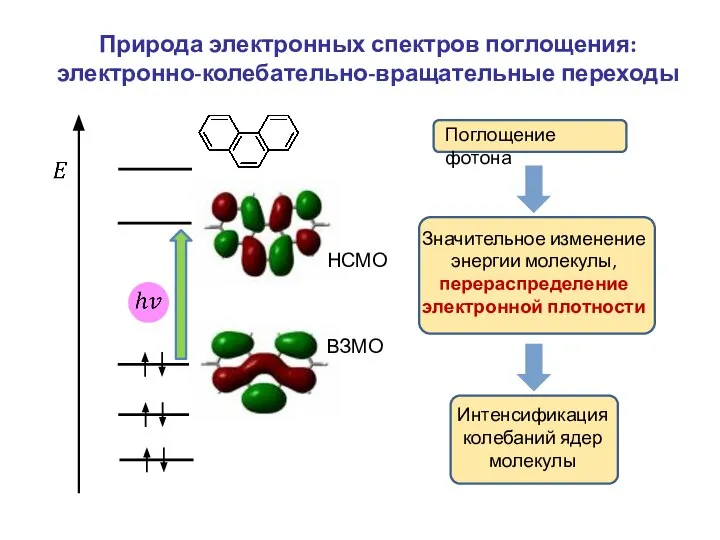
- 10. Природа электронных спектров поглощения: электронно-колебательно-вращательные переходы ВЗМО НСМО Поглощение фотона Значительное изменение энергии молекулы, перераспределение электронной
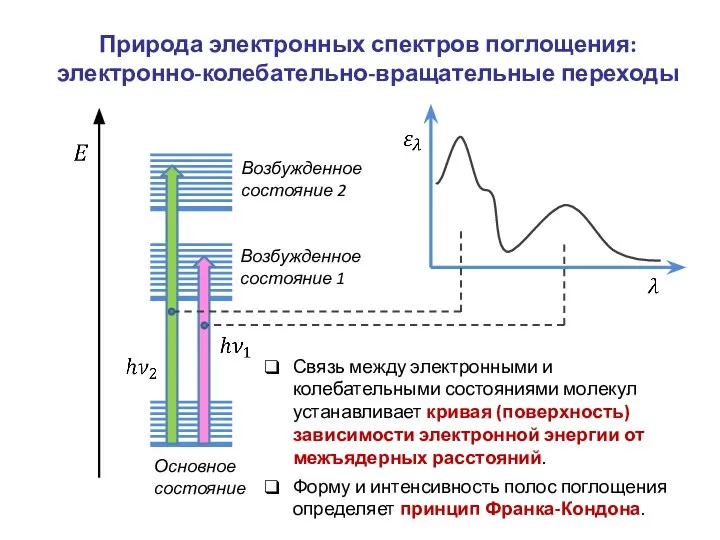
- 11. Природа электронных спектров поглощения: электронно-колебательно-вращательные переходы Основное состояние Возбужденное состояние 1 Возбужденное состояние 2 Связь между
- 12. Конфигурация электронно-колебательных уровней двухатомной молекулы
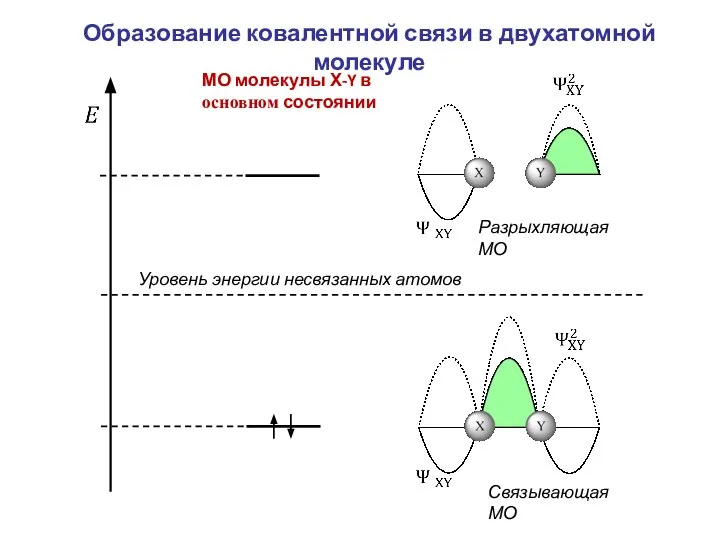
- 13. Связывающая МО Разрыхляющая МО Уровень энергии несвязанных атомов Образование ковалентной связи в двухатомной молекуле МО молекулы
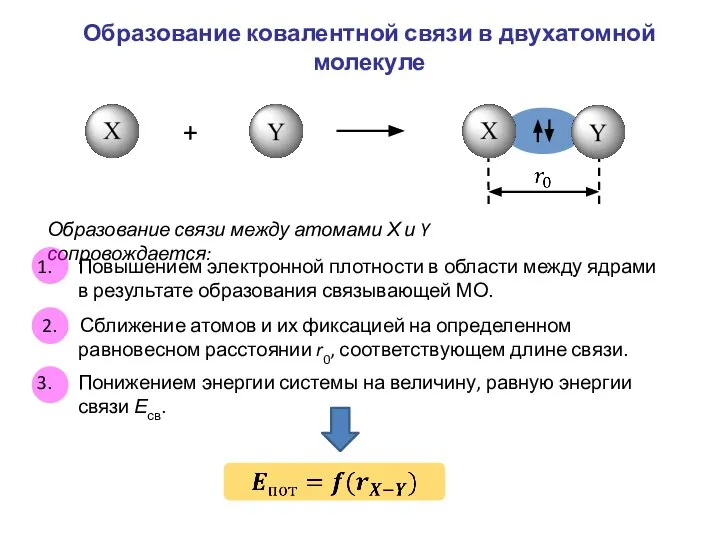
- 14. + Образование связи между атомами Х и Y сопровождается: Повышением электронной плотности в области между ядрами
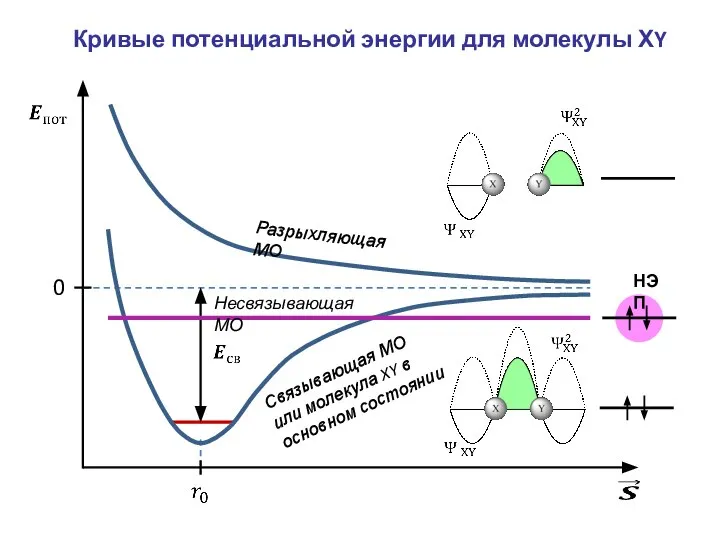
- 15. Кривые потенциальной энергии для молекулы ХY Связывающая МО или молекула XY в основном состоянии Разрыхляющая МО
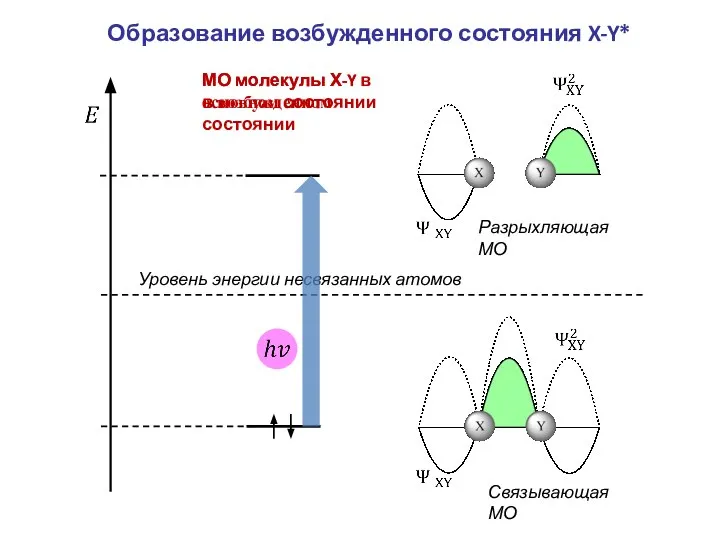
- 16. Связывающая МО Разрыхляющая МО Уровень энергии несвязанных атомов Образование возбужденного состояния X-Y* МО молекулы Х-Y в
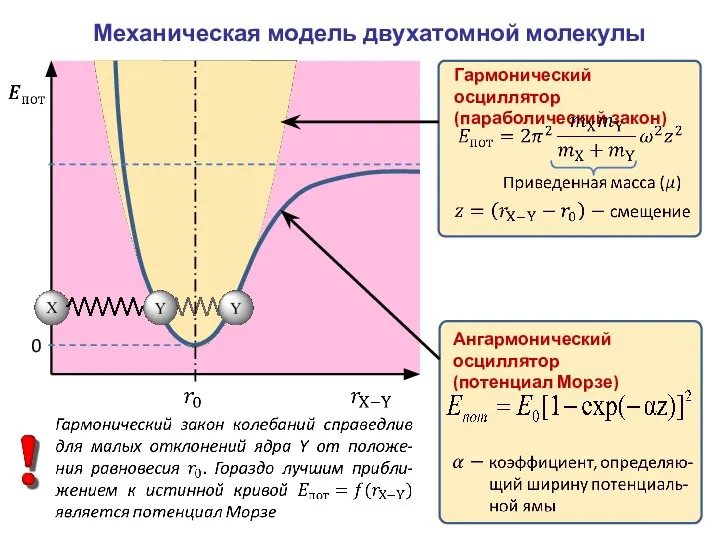
- 17. Механическая модель двухатомной молекулы 0 Гармонический осциллятор (параболический закон) Ангармонический осциллятор (потенциал Морзе)
- 18. Квантово-механическая модель двухатомной молекулы Потенциал Морзе Уравнение Шредингера для одномерного осциллятора: Результат решения (Уравнение Морзе):
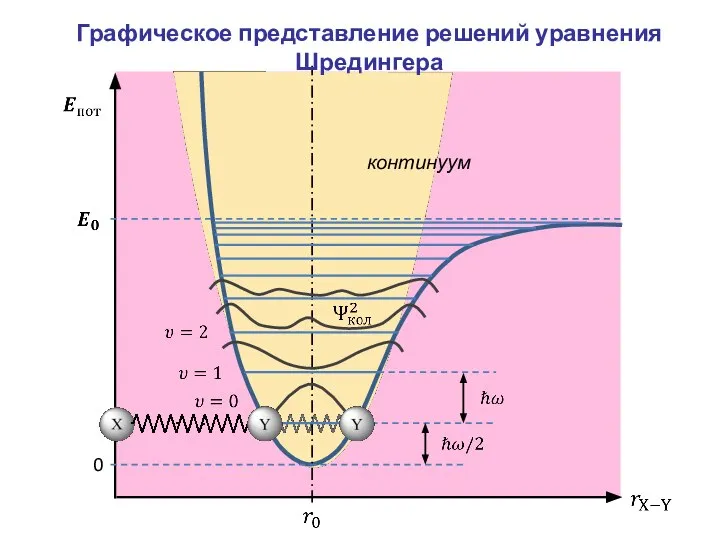
- 19. Графическое представление решений уравнения Шредингера
- 20. Принцип Франка-Кондона и форма полос поглощения в электронных спектрах
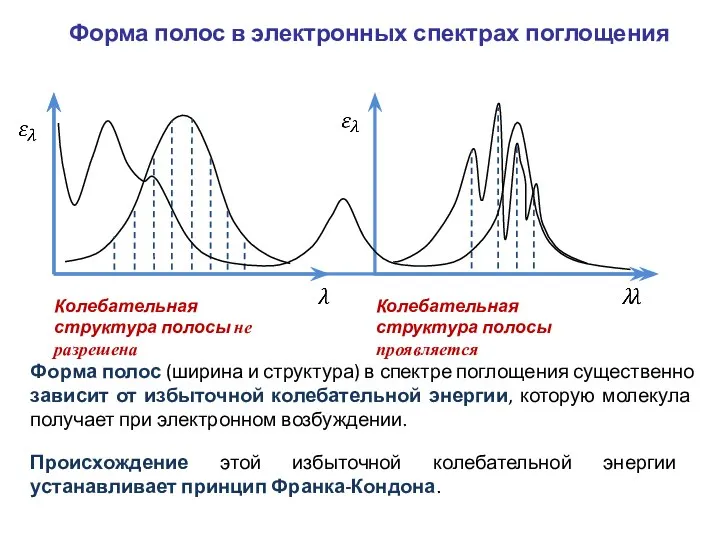
- 21. Форма полос в электронных спектрах поглощения Форма полос (ширина и структура) в спектре поглощения существенно зависит
- 22. Принцип Франка-Кондона Если процессы фотовозбуждения изображать как переход с одной потенциальной кривой на другую, то принцип
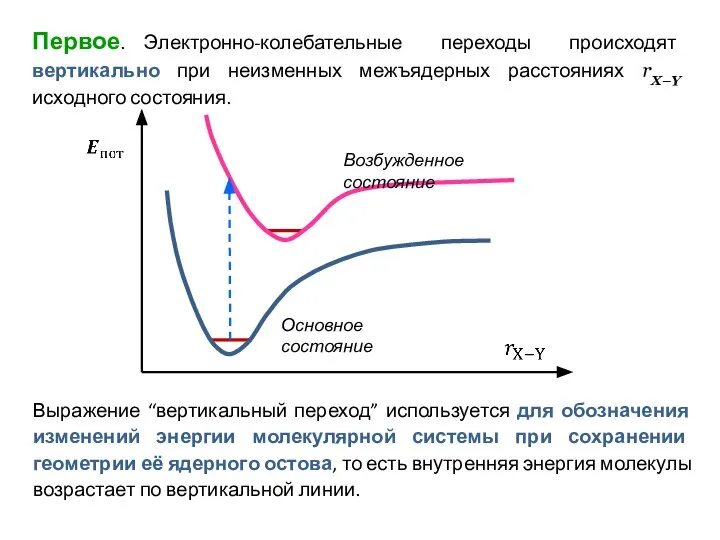
- 23. Первое. Электронно-колебательные переходы происходят вертикально при неизменных межъядерных расстояниях rX–Y исходного состояния. Выражение “вертикальный переход” используется
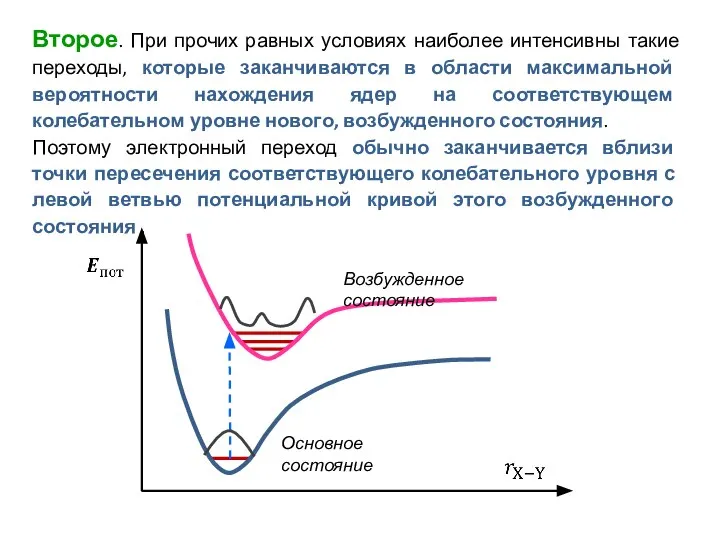
- 24. Второе. При прочих равных условиях наиболее интенсивны такие переходы, которые заканчиваются в области максимальной вероятности нахождения
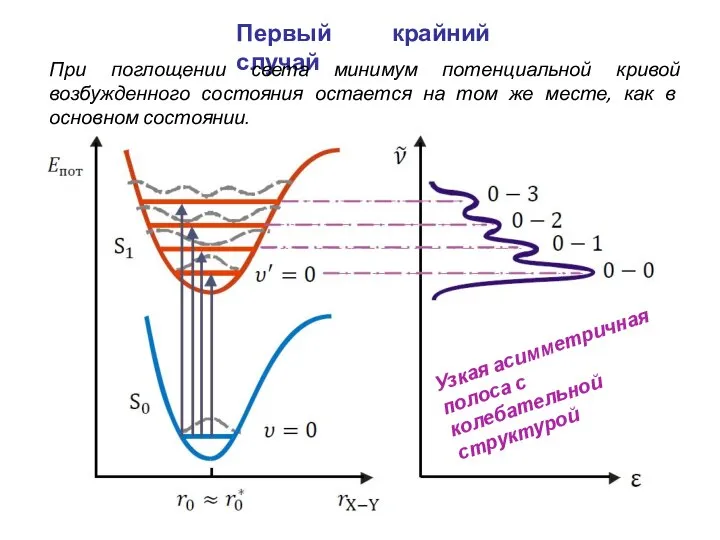
- 25. Первый крайний случай Узкая асимметричная полоса с колебательной структурой При поглощении света минимум потенциальной кривой возбужденного
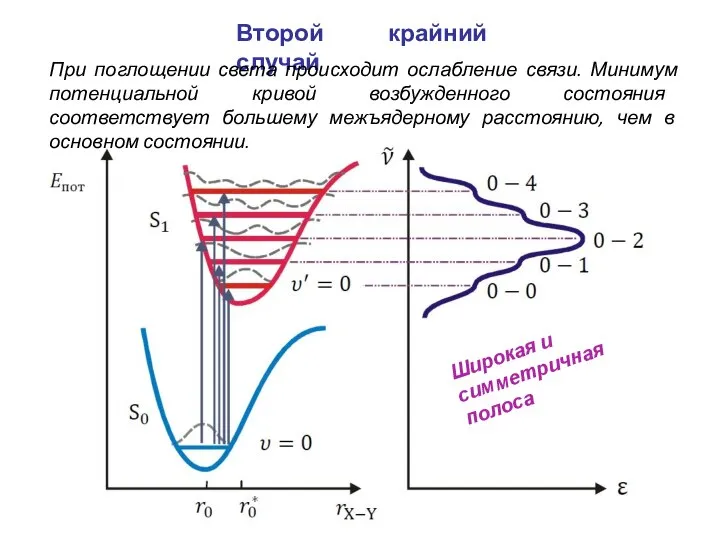
- 26. Широкая и симметричная полоса Второй крайний случай При поглощении света происходит ослабление связи. Минимум потенциальной кривой
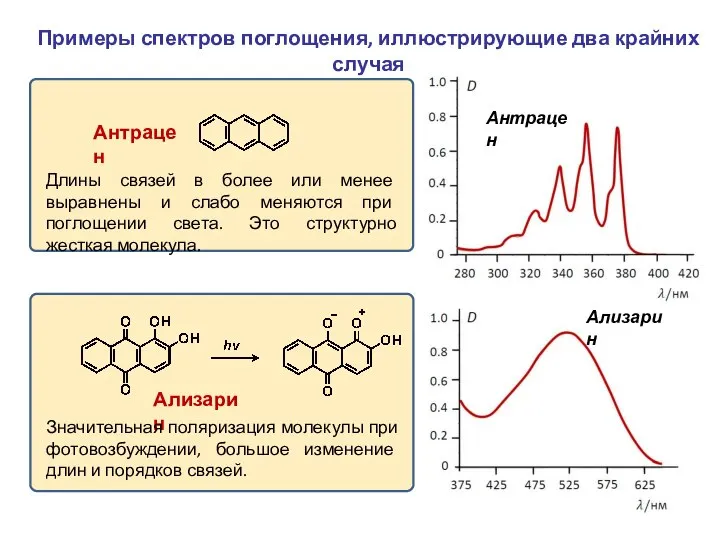
- 27. Примеры спектров поглощения, иллюстрирующие два крайних случая
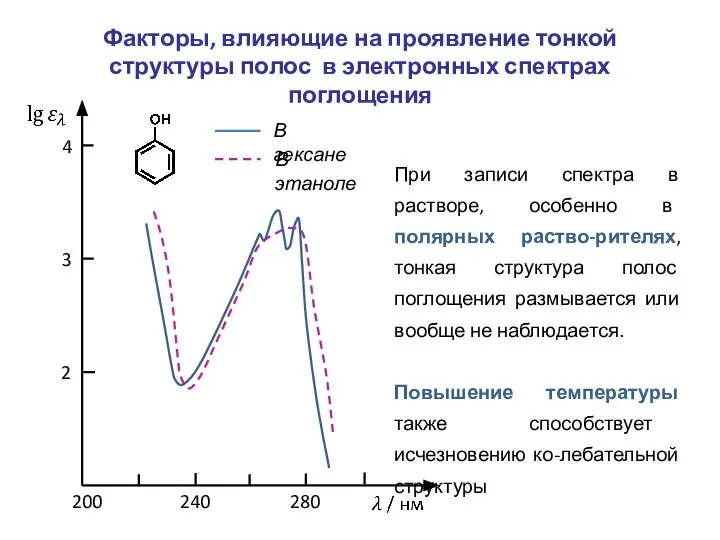
- 28. Факторы, влияющие на проявление тонкой структуры полос в электронных спектрах поглощения В гексане В этаноле При
- 29. Формирование МО и основные типы электронных переходов
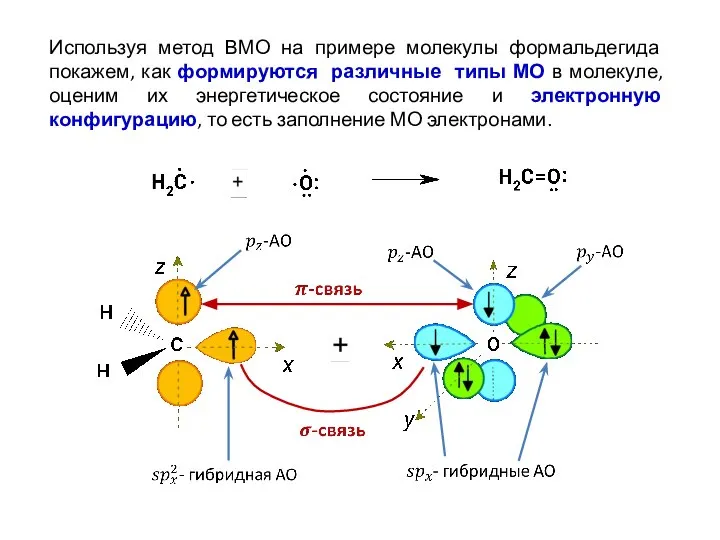
- 30. Используя метод ВМО на примере молекулы формальдегида покажем, как формируются различные типы МО в молекуле, оценим
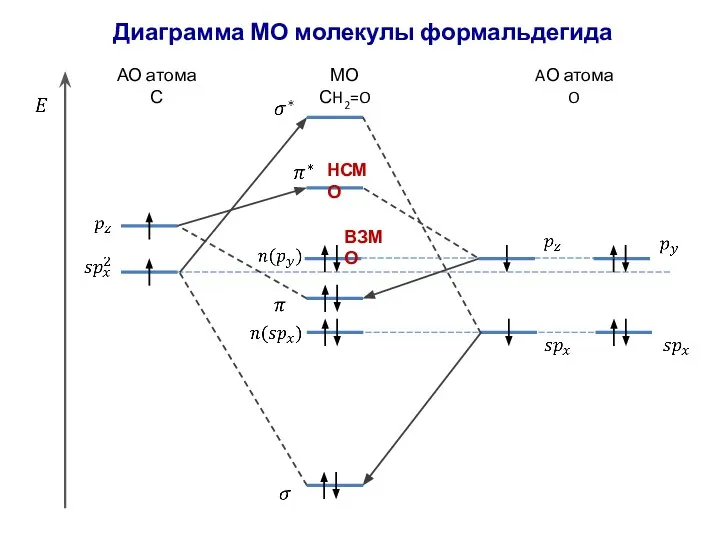
- 31. Диаграмма МО молекулы формальдегида АО атома С AО атома O МО СH2=O ВЗМО НСМО
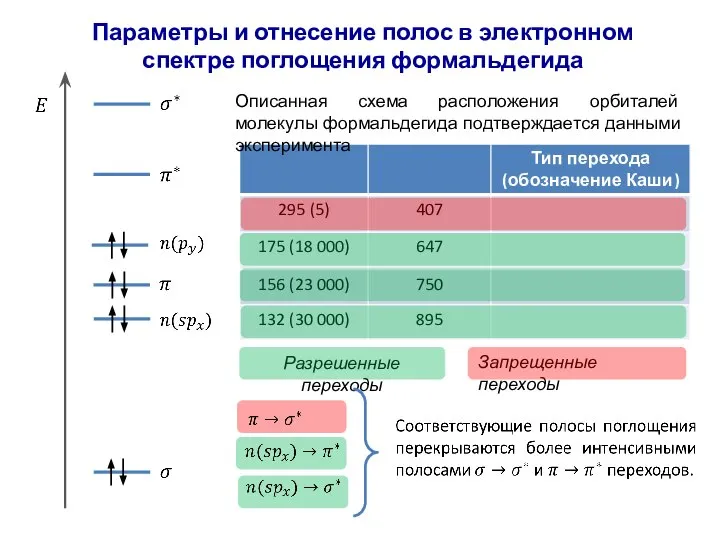
- 32. Параметры и отнесение полос в электронном спектре поглощения формальдегида Описанная схема расположения орбиталей молекулы формальдегида подтверждается
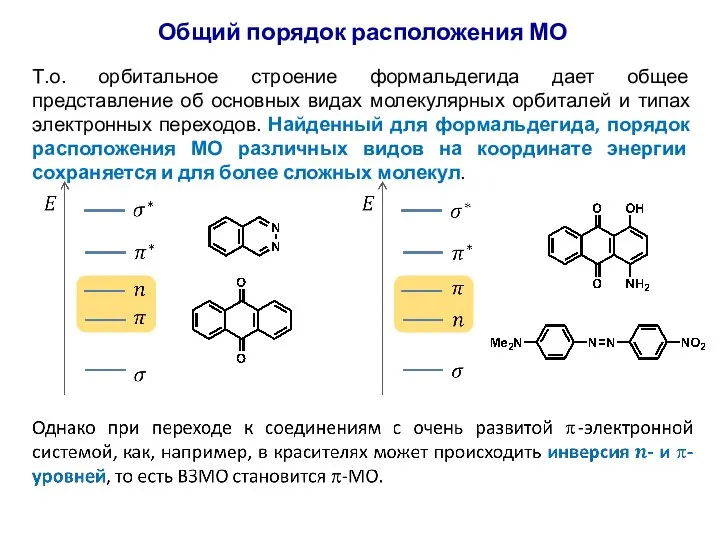
- 33. Общий порядок расположения МО Т.о. орбитальное строение формальдегида дает общее представление об основных видах молекулярных орбиталей
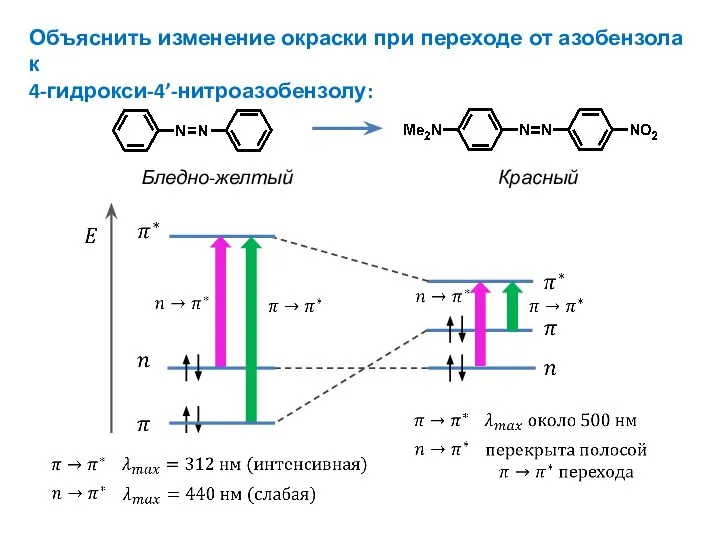
- 34. Бледно-желтый Красный Объяснить изменение окраски при переходе от азобензола к 4-гидрокси-4’-нитроазобензолу:
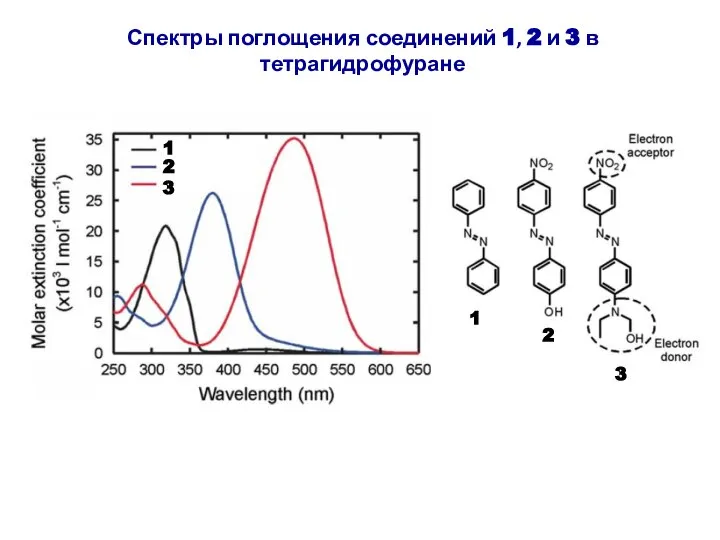
- 35. 1 2 3 1 2 3 Спектры поглощения соединений 1, 2 и 3 в тетрагидрофуране
- 36. Электронные конфигурации и электронные состояния
- 37. Электронная конфигурация – распределение электронов по орбиталям в системе Электронное состояние – те свойства системы, которые
- 38. Спин электрона
- 39. Спиновые характеристики многоэлектронной системы Для данной электронной конфигурации:
- 40. Система с замкнутой электронной оболочкой Система с незамкнутой электронной оболочкой (радикал, ион-радикал) Синглетное состояние (обозначается S)
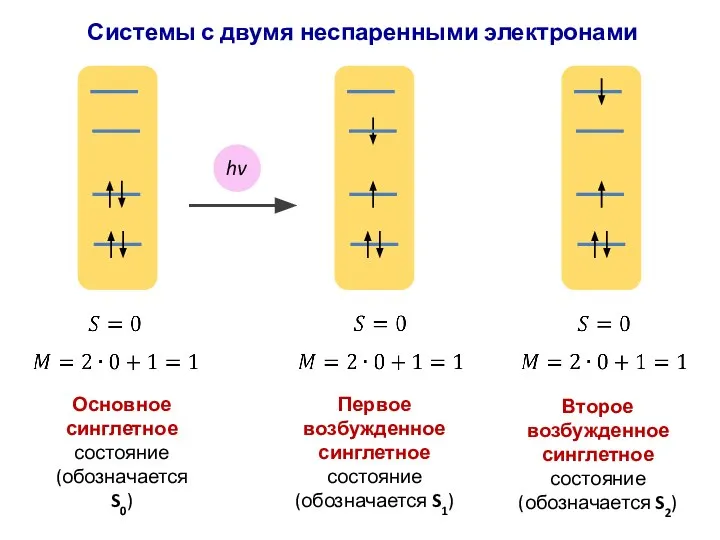
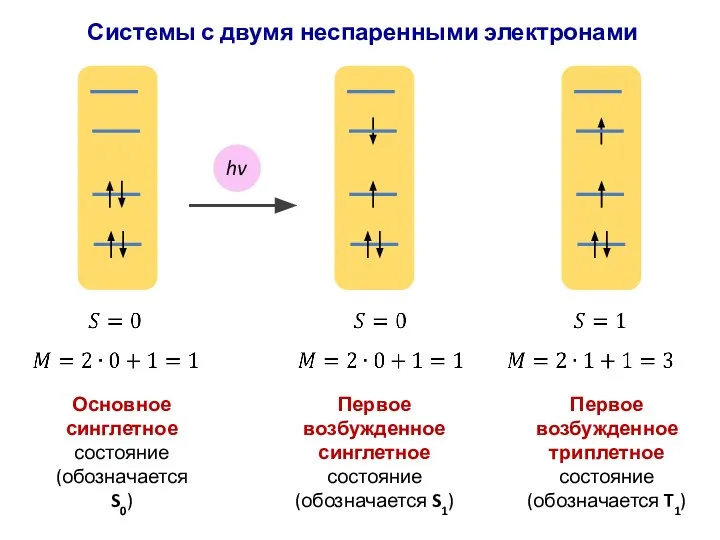
- 41. Основное синглетное состояние (обозначается S0) hv Первое возбужденное синглетное состояние (обозначается S1) Системы с двумя неспаренными
- 42. Основное синглетное состояние (обозначается S0) hv Первое возбужденное синглетное состояние (обозначается S1) Первое возбужденное триплетное состояние
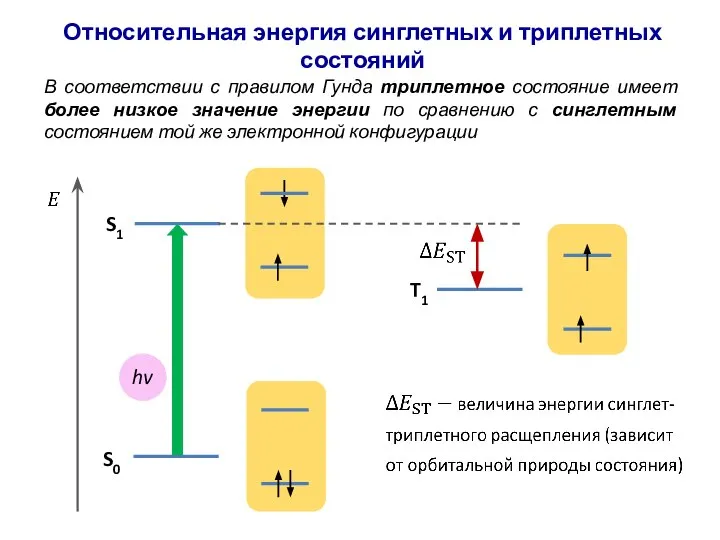
- 43. В соответствии с правилом Гунда триплетное состояние имеет более низкое значение энергии по сравнению с синглетным
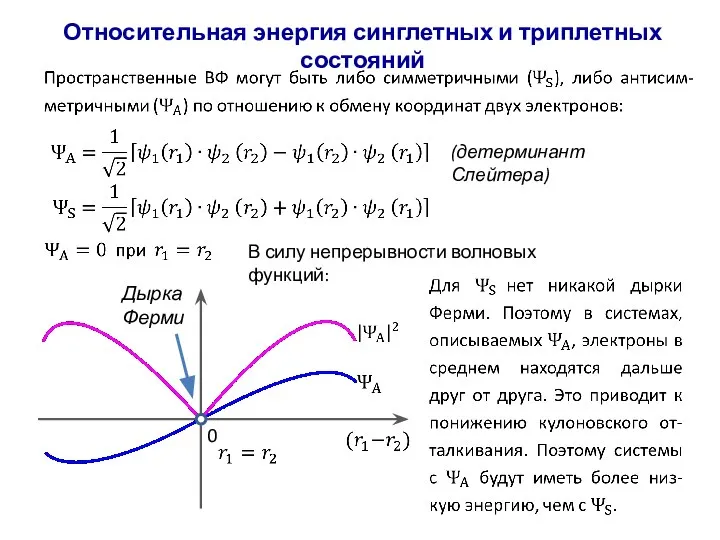
- 44. Относительная энергия синглетных и триплетных состояний В силу непрерывности волновых функций: 0 Дырка Ферми (детерминант Слейтера)
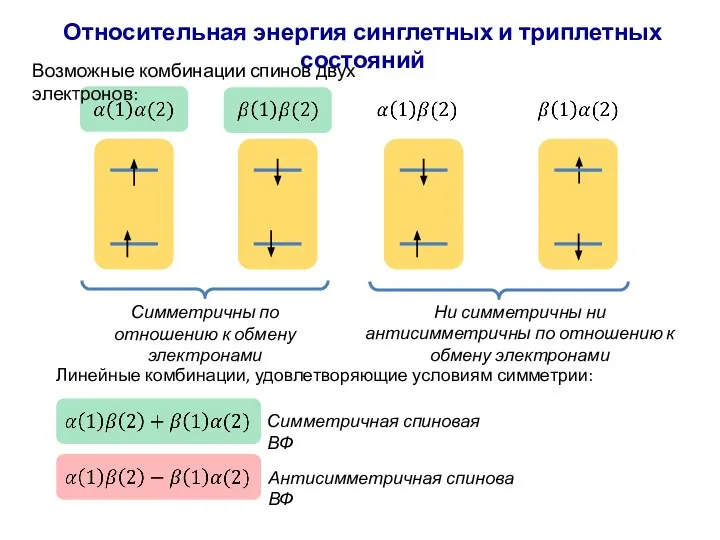
- 45. Относительная энергия синглетных и триплетных состояний Возможные комбинации спинов двух электронов: Симметричны по отношению к обмену
- 46. Относительная энергия синглетных и триплетных состояний Триплетная спиновая ВФ (симметричная) Синглетная спиновая ВФ (антисимметрияная) Поэтому у
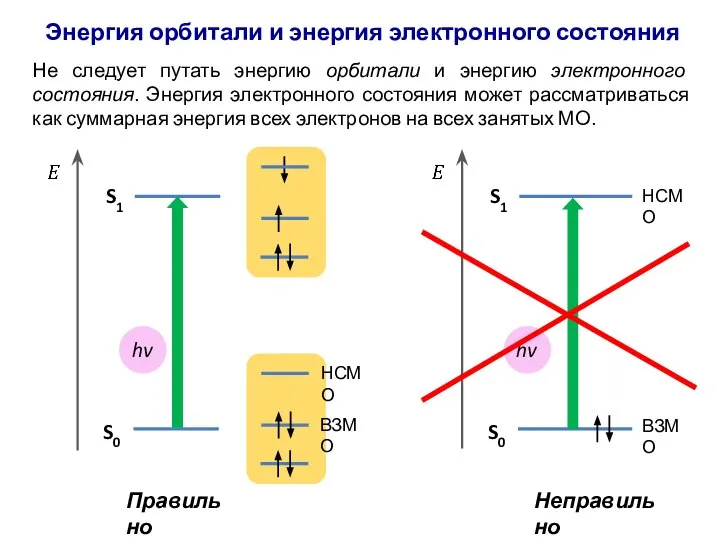
- 47. Энергия орбитали и энергия электронного состояния Не следует путать энергию орбитали и энергию электронного состояния. Энергия
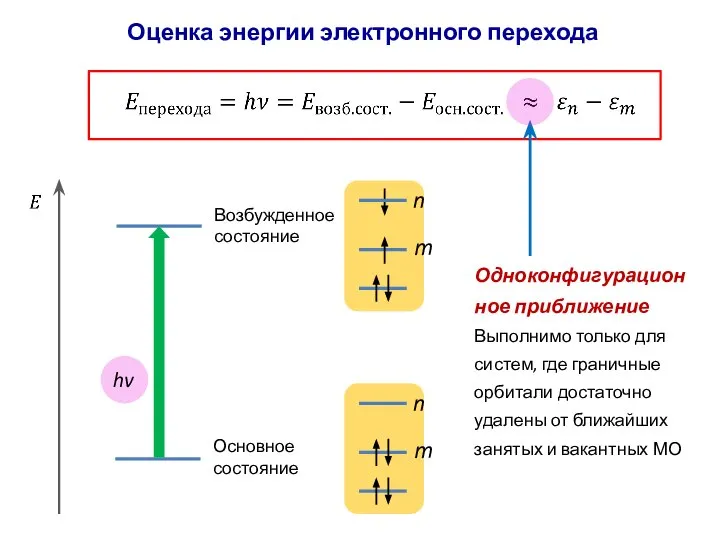
- 48. Оценка энергии электронного перехода hv m n Основное состояние Возбужденное состояние Одноконфигурационное приближение Выполнимо только для
- 50. Скачать презентацию













 Движение тела по окружности под действием силы тяжести
Движение тела по окружности под действием силы тяжести Суперпроводники. История открытия
Суперпроводники. История открытия Газовые законы
Газовые законы Проводники с током в магнитном поле. Лекция 7
Проводники с током в магнитном поле. Лекция 7 Тормозные системы
Тормозные системы Кинематика
Кинематика Электромагнитные волны. Лекция 11
Электромагнитные волны. Лекция 11 Презентация на тему Выталкивающая сила
Презентация на тему Выталкивающая сила  Определение проекции силы на координатную ось
Определение проекции силы на координатную ось Инновационные технологии в машиностроении. Лекция 1, 2. Общая характеристика машиностроительного производства
Инновационные технологии в машиностроении. Лекция 1, 2. Общая характеристика машиностроительного производства Разработка инструментария для решения задачи вычислительной гидродинамики при моделировании воздушных потоков
Разработка инструментария для решения задачи вычислительной гидродинамики при моделировании воздушных потоков Радиоактивные превращения атомных ядер
Радиоактивные превращения атомных ядер Общие сведения о системах радиосвязи. Электропитание средств связи
Общие сведения о системах радиосвязи. Электропитание средств связи Общий осмотр автомобиля Toyota Mark II
Общий осмотр автомобиля Toyota Mark II Презентация на тему Интерференция. Дифракция
Презентация на тему Интерференция. Дифракция  Неразъемные соединения
Неразъемные соединения Слесарные инструменты
Слесарные инструменты Урок 12 Електродвигуни. Електровимірювальні прилади
Урок 12 Електродвигуни. Електровимірювальні прилади Моделирование процессов преобразования сигналов и помех линейными и нелинейными звеньями
Моделирование процессов преобразования сигналов и помех линейными и нелинейными звеньями Международная система единиц СИ
Международная система единиц СИ Презентация на тему Источники электрического тока
Презентация на тему Источники электрического тока  Фильтры с бесконечной импульсной характеристикой. Синтез БИХ-фильтров методом билинейного Z-преобразования''
Фильтры с бесконечной импульсной характеристикой. Синтез БИХ-фильтров методом билинейного Z-преобразования'' Однородные уравнения. Уравнения, приводящиеся к однородным
Однородные уравнения. Уравнения, приводящиеся к однородным Построение изображений, полученных с помощью линз
Построение изображений, полученных с помощью линз Определение коэффициента поверхностного натяжения синтетических моющих средств
Определение коэффициента поверхностного натяжения синтетических моющих средств Электроэнергия Ксенон (Светодиоды)
Электроэнергия Ксенон (Светодиоды) Графическое представление результатов измерений
Графическое представление результатов измерений Блоки цилиндров и цилиндровые втулки
Блоки цилиндров и цилиндровые втулки