Содержание
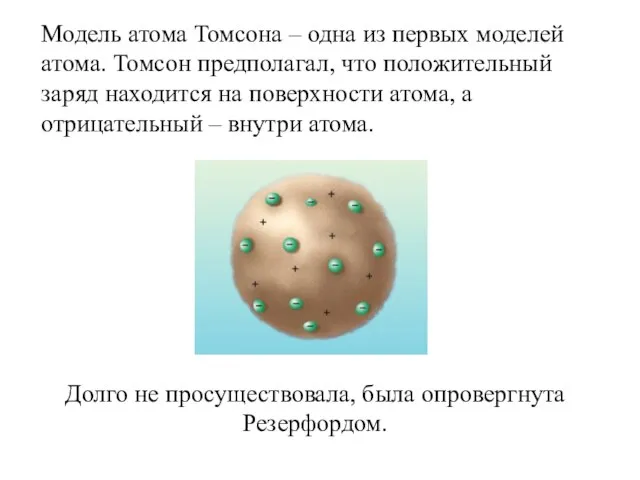
- 2. Модель атома Томсона – одна из первых моделей атома. Томсон предполагал, что положительный заряд находится на
- 3. Планетарная (ядерная) модель атома В 1911 г английский физик Э.Резерфорд предложил планетарную модель атома.
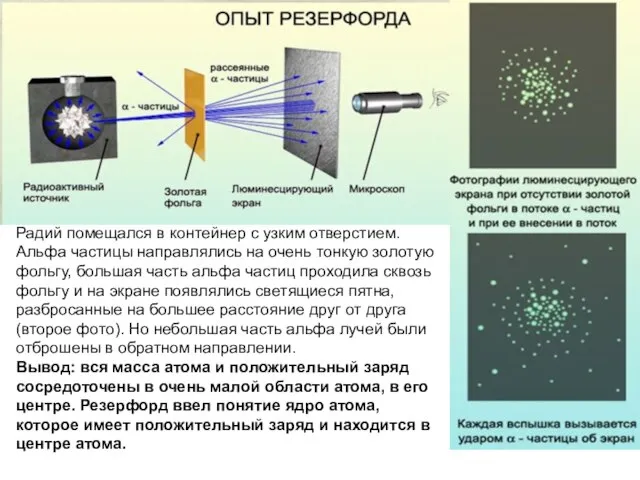
- 4. Радий помещался в контейнер с узким отверстием. Альфа частицы направлялись на очень тонкую золотую фольгу, большая
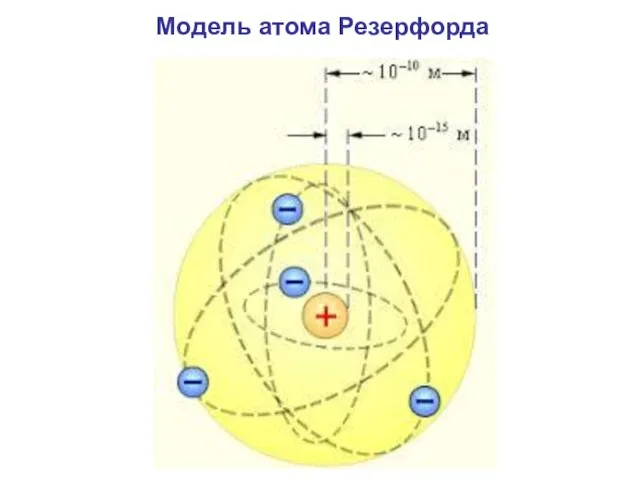
- 5. Модель атома Резерфорда
- 6. В центре атома – положительно заряженная частица – ядро. Заряд ядра: qя = +Z·e Z- порядковый
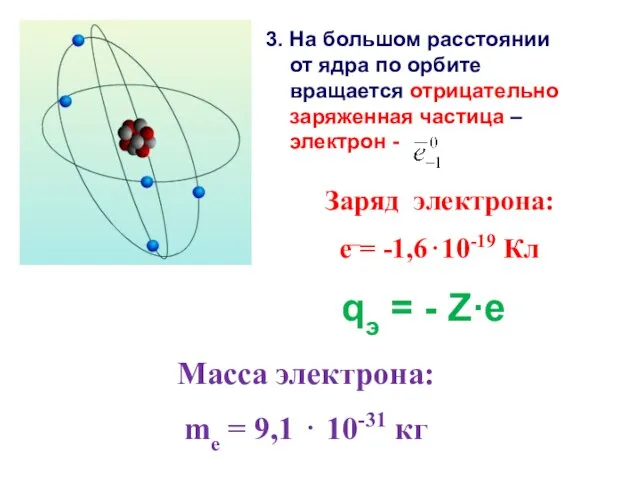
- 7. 3. На большом расстоянии от ядра по орбите вращается отрицательно заряженная частица – электрон - Заряд
- 8. В обычном состоянии атом нейтрален. Потому что, количество протонов в ядре атома любого элемента равно количеству
- 9. Нейтроны вместе с протонами называются нуклонами. Ядро называется нуклид. AZХ – произвольный химический элемент где А
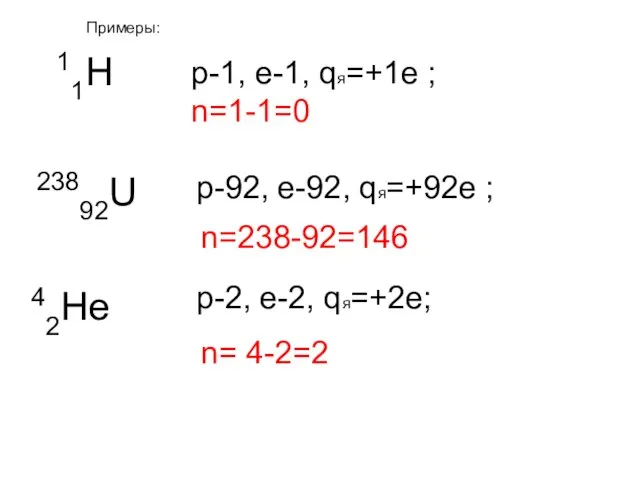
- 10. 11Н 23892U 42He p-1, e-1, qя=+1e ; n=1-1=0 p-92, e-92, qя=+92e ; p-2, e-2, qя=+2e; n=238-92=146
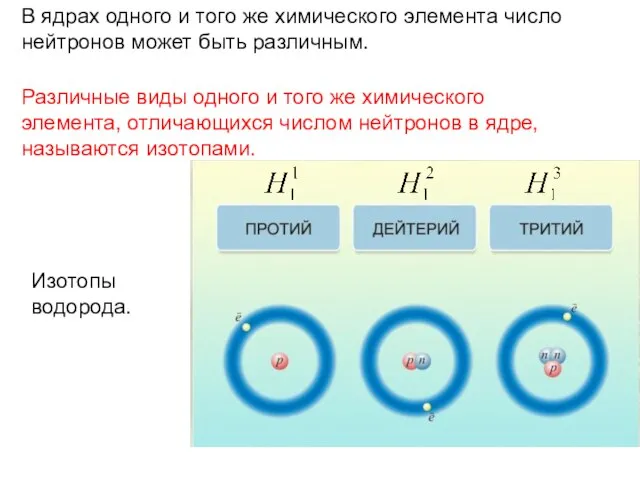
- 11. В ядрах одного и того же химического элемента число нейтронов может быть различным. Различные виды одного
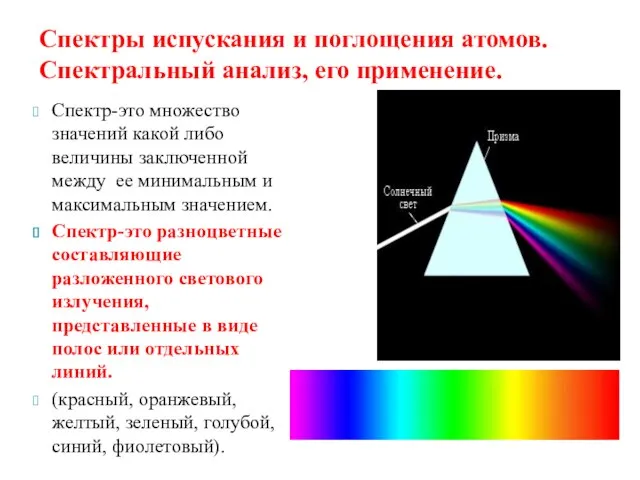
- 12. Спектр-это множество значений какой либо величины заключенной между ее минимальным и максимальным значением. Спектр-это разноцветные составляющие
- 13. Непрерывные спектры дают тела, находящиеся в твердом , жидком состоянии, а также сильно сжатые газы. Линейчатые
- 14. Атомы любого химического элемента излучают строго определенный набор длин волн, дают спектр, не похожий на спектры
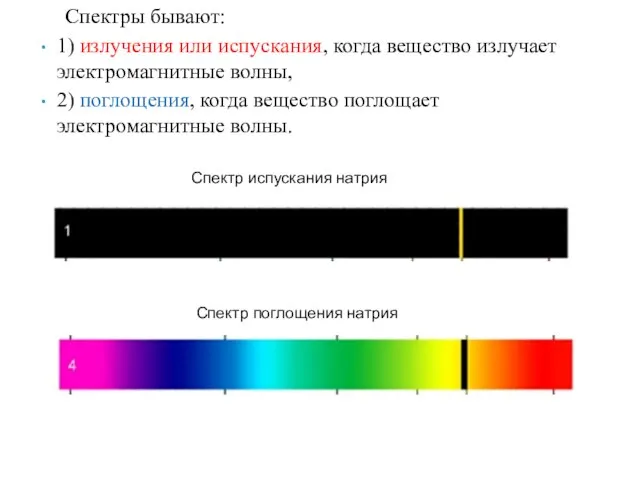
- 15. Спектры бывают: 1) излучения или испускания, когда вещество излучает электромагнитные волны, 2) поглощения, когда вещество поглощает
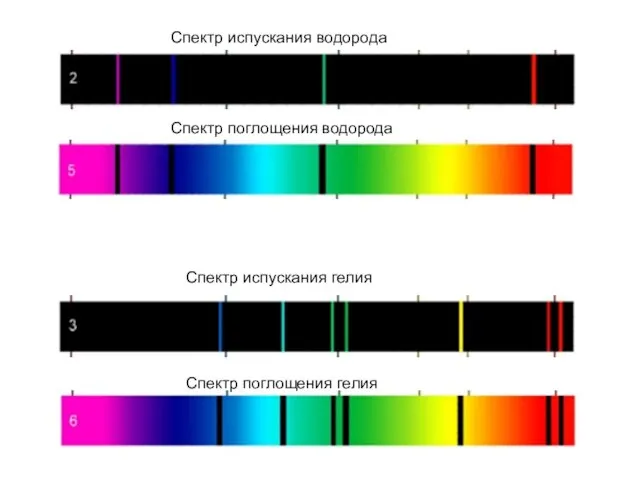
- 16. Спектр испускания водорода Спектр испускания гелия Спектр поглощения водорода Спектр поглощения гелия
- 17. Спектроскоп. Спектроскоп - это прибор для наблюдения спектров. Спектрограф - это прибор для получения фотографий спектров.
- 18. Спектральный анализ. Спектральный анализ -это метод определения химического состава вещества по его спектру. Спектральный анализ основан
- 19. Лаборатория спектрального анализа.
- 20. С помощью спектрального анализа можно обнаружить данный элемент в составе сложного вещества. Благодаря универсальности спектральный анализ
- 21. В настоящее время в криминалистике широко используются телевизионные спектральные системы (ТСС). - обнаружение различного рода подделок
- 22. В 1913 году датский физик Нильс Бор сформулировал основные положения квантовой физики в виде постулатов. В
- 23. Постулаты Бора: 1. (постулат стационарных состояний) Атом может находится в особых квантовых или стационарных состояниях, каждому
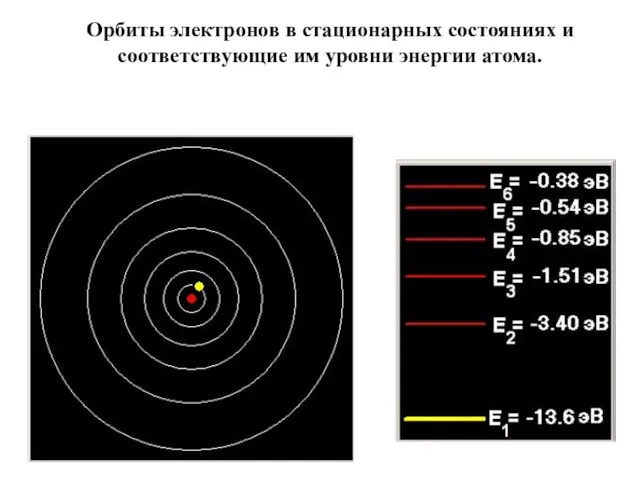
- 24. Орбиты электронов в стационарных состояниях и соответствующие им уровни энергии атома.
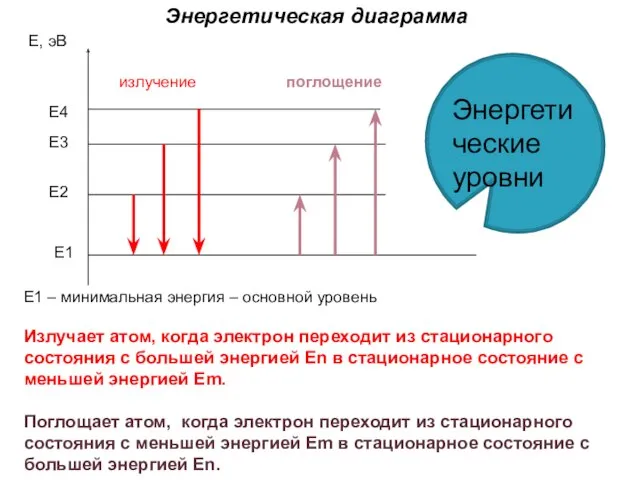
- 25. Е, эВ Е2 Е1 Е3 Е4 излучение поглощение Энергетическая диаграмма Энергетические уровни Е1 – минимальная энергия
- 26. Тест на самопроверку 1. Какие опыты послужили основанием для создания ядерной модели атома? А) опыты по
- 27. 2. Сколько электронов содержится в электронной оболочке нейтрального атома, в атомном ядре которого содержится 7 протонов
- 28. 4. Светящаяся поверхность Солнца-фотосфера создает А) спектр только из желтых и оранжевых линий; В) спектр только
- 29. 5. Частота света, соответствующая фотонам с энергией 50∙10-19 Дж, равна ( h = 6,62∙10-34 Дж∙с) А)
- 31. Скачать презентацию

















 Презентация на тему Сила трения покоя
Презентация на тему Сила трения покоя  Закон радиоактивного распада. Период полураспада
Закон радиоактивного распада. Период полураспада Движение тела по окружности с постоянной по модулю скоростью
Движение тела по окружности с постоянной по модулю скоростью Второй закон Ньютона. Динамика материальной точки
Второй закон Ньютона. Динамика материальной точки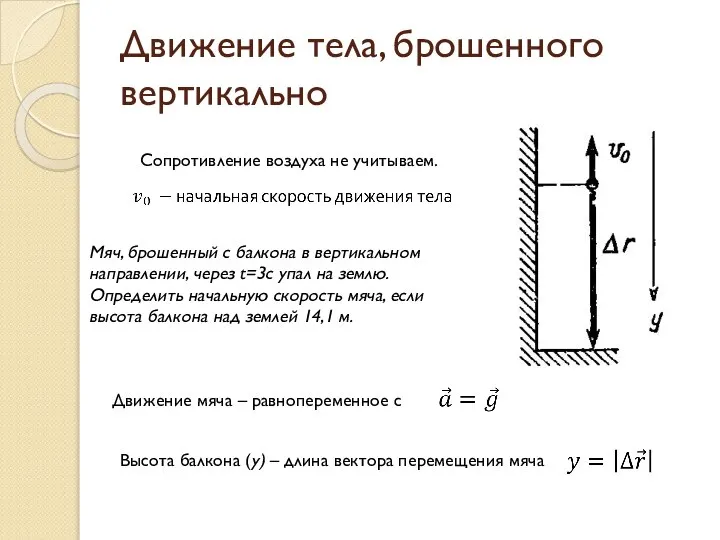 Движение тела, брошенного вертикально
Движение тела, брошенного вертикально Некоторые положения Теории относительности
Некоторые положения Теории относительности Перемещение при прямолинейном равноускоренном движении. Урок 1
Перемещение при прямолинейном равноускоренном движении. Урок 1 Расчёт аэродинамических характеристик самолётов
Расчёт аэродинамических характеристик самолётов Энергия заряженного конденсата
Энергия заряженного конденсата Переменное прямолинейное движение
Переменное прямолинейное движение Решение задач на закон электромагнитной индукции
Решение задач на закон электромагнитной индукции Презентация на тему Строение и свойства вещества
Презентация на тему Строение и свойства вещества  Control of nonlinear dynamics of electromechanical systems
Control of nonlinear dynamics of electromechanical systems Масса молекул. Количество вещества
Масса молекул. Количество вещества Классификация нагрузок
Классификация нагрузок Сообщающиеся сосуды
Сообщающиеся сосуды Соединения фитингами
Соединения фитингами Электромагнитная индукция
Электромагнитная индукция Теоретическая механика
Теоретическая механика Электрический ток. Источники тока
Электрический ток. Источники тока Специзмерения системах автоматики и телемеханики
Специзмерения системах автоматики и телемеханики Изучение явления электромагнитной индукции. Лабораторная работа
Изучение явления электромагнитной индукции. Лабораторная работа Магнитное поле
Магнитное поле Запись и воспроизведение звука
Запись и воспроизведение звука Фотоэффект
Фотоэффект Вечный двигатель в истории
Вечный двигатель в истории Физика. Вводная лекция
Физика. Вводная лекция Электроэнергетические системы и сети. Определение параметров элементов электрической сети
Электроэнергетические системы и сети. Определение параметров элементов электрической сети