Содержание
- 2. Работой называется обобщенная форма обмена энергией между системой и окружающей средой, в основе которой лежит изменение
- 3. dV- бесконечно малое изменение объёма системы. Функция процесса первого типа; δA - элементарная работа, бесконечно малая
- 4. Пусть a и b - две замкнутые равновесные системы с температурами Ta и Tb. Пусть Ta
- 5. Энергия, которую получает система при теплообмене с окружающей средой, называется теплом (количеством теплоты) и обозначается буквой
- 6. 1. Первое начало термодинамики. 2. Работа и теплота идеального газа в изопроцессах. 3. Устройство тепловой машины.
- 7. Первый принцип (первое начало) термодинамики Если система получает тепло δQ из окружающей среды, увеличивается внутренняя энергия
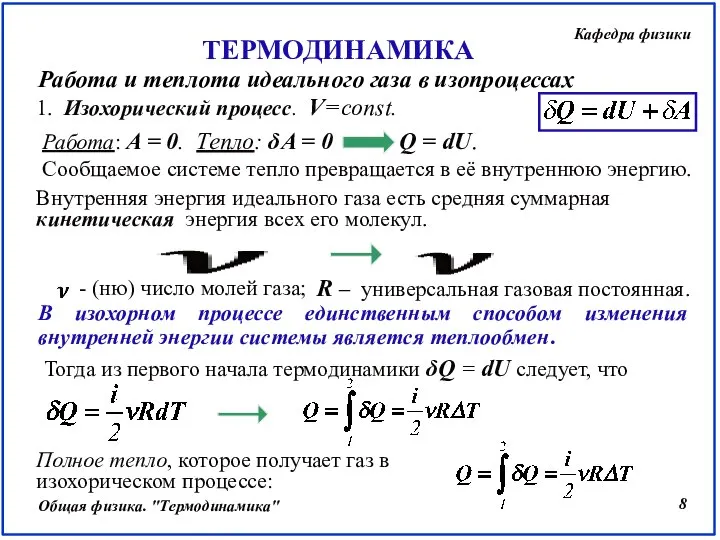
- 8. Работа и теплота идеального газа в изопроцессах 1. Изохорический процесс. V=const. Внутренняя энергия идеального газа есть
- 9. 2. Изобарный процесс. р=const. В изобарном процессе p = const, тогда При изобарном расширении ΔV>0, и
- 10. 2. Изобарный процесс. Р=const. Тепло. При расширении газ совершает работу. Источник энергии - внутренняя энергия газа.
- 11. 2. Изобарный процесс . Р=const. Увеличение объёма dV и температуры dT в изобарном процессе связаны уравнением
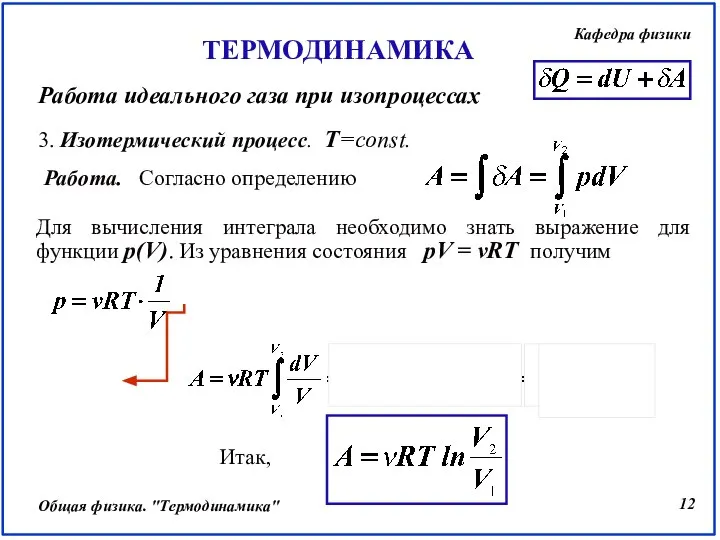
- 12. 3. Изотермический процесс. Т=const. Для вычисления интеграла необходимо знать выражение для функции p(V). Из уравнения состояния
- 13. 3. Изотермический процесс. Т=const. Тепло. Источником работы A, как следует из первого начала термодинамики, является внутренняя
- 14. 4. Адиабатический процесс. Работа. Для определения работы требуется вычислить интеграл При адиабатном расширении работа положительна (её
- 15. 4. Адиабатический процесс. Тепло. По определению адиабатического процесса система в этом процессе не получает и не
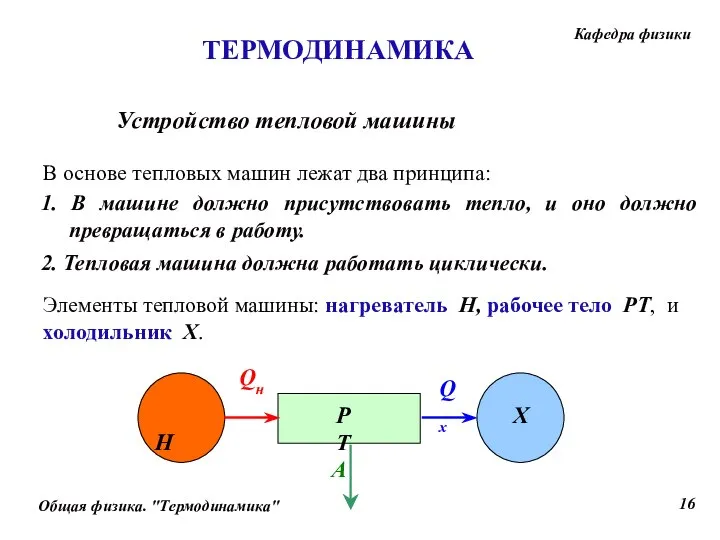
- 16. Устройство тепловой машины Qн Qх A В основе тепловых машин лежат два принципа: 1. В машине
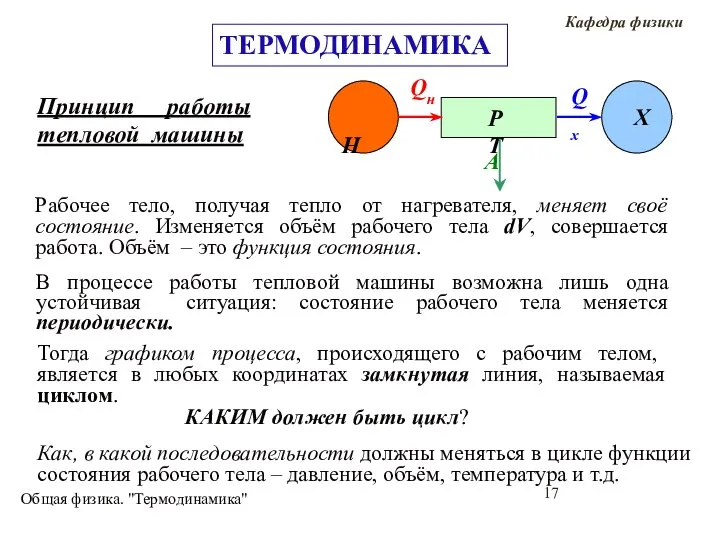
- 17. Общая физика. "Термодинамика" Принцип работы тепловой машины Рабочее тело, получая тепло от нагревателя, меняет своё состояние.
- 18. Общая физика. "Термодинамика" Работа тепловой машины Решение: нарисовать на графике в каких-либо координатах произвольную замкнутую линию,
- 19. Общая физика. "Термодинамика" Коэффициентом полезного действия тепловой машины (цикла) называется отношение работы A, совершаемой машиной за
- 20. Общая физика. "Термодинамика" Коэффициент полезного действия (к.п.д.) тепловой машины. 1 2 P V 2 1 Цилиндр,
- 22. Скачать презентацию















 Фотоэлектрические датчики
Фотоэлектрические датчики Уравнения и диапазоны. Лекция 2
Уравнения и диапазоны. Лекция 2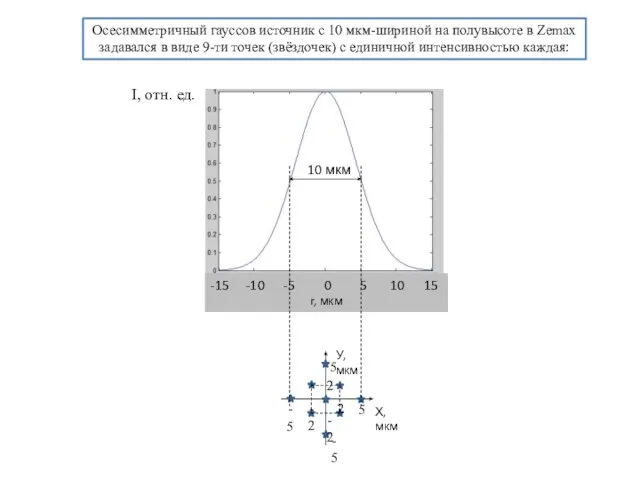 Схема Кирпатрика-Баеза
Схема Кирпатрика-Баеза Автономные инверторы
Автономные инверторы Ясси электромагнит тўлқин ва унинг хоссалари. Элeктромагнит тўлқин шкаласи
Ясси электромагнит тўлқин ва унинг хоссалари. Элeктромагнит тўлқин шкаласи laboratorn_2
laboratorn_2 Магнитное поле. Тема № 6
Магнитное поле. Тема № 6 Квантовая теория теплоемкости
Квантовая теория теплоемкости Интерференция и дифракция механических волн
Интерференция и дифракция механических волн Презентация по физике "Работа электростатического поля по перемещению заряда" -
Презентация по физике "Работа электростатического поля по перемещению заряда" -  Презентация на тему Способы теплопередачи
Презентация на тему Способы теплопередачи  Последовательное соединение
Последовательное соединение Сопротивление материалов
Сопротивление материалов Элементарные частицы
Элементарные частицы Питание
Питание Электрический ток. Сила тока
Электрический ток. Сила тока Потенциальная энергия
Потенциальная энергия Презентация на тему: Идеальный газ в МКТ
Презентация на тему: Идеальный газ в МКТ Бесциркуляционное течение около цилиндра. Лекция 7
Бесциркуляционное течение около цилиндра. Лекция 7 Электрический ток
Электрический ток Две задачи
Две задачи Строение атома. Опыты Резерфорда
Строение атома. Опыты Резерфорда Классификация и основные характеристики механических передач
Классификация и основные характеристики механических передач Спрощення складних 1Н-ЯМР-спектрів. Гомоядерний декаплінг
Спрощення складних 1Н-ЯМР-спектрів. Гомоядерний декаплінг Активные диэлектрики. Сегнетоэлектрики. Пьезоэлектрики
Активные диэлектрики. Сегнетоэлектрики. Пьезоэлектрики Теория управления. Устойчивость
Теория управления. Устойчивость Градиент и его свойства
Градиент и его свойства Колесные пары локомотива
Колесные пары локомотива