Содержание
- 2. Домашнее задание § 113 (учебник физики 10 класс, Г.Я.Мякишев, Б.Б.Буховцев, Н.Н.Соцкий, М. Просвещение, 2016) ЕГЭ с.
- 3. По электрическим свойствам все жидкости можно разделить на 2 группы ПРОВОДЯЩИЕ НЕПРОВОДЯЩИЕ Содержащие свободные заряженные частицы
- 4. Проводимость разных веществ
- 5. Na Cl Na+ Cl- NaCl → Na+ + Cl- При диссоциации ионы металлов и водорода всегда
- 6. Электролиты обладают ионной проводимостью. Степень диссоциации – отношение числа молекул, диссоциировавших на ионы, к общему количеству
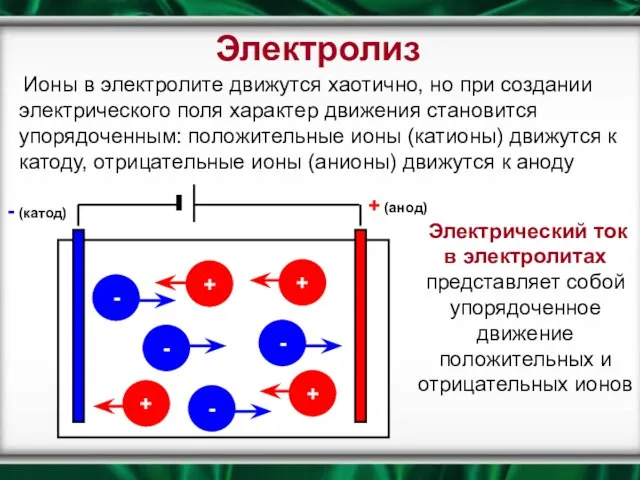
- 7. Ионы в электролите движутся хаотично, но при создании электрического поля характер движения становится упорядоченным: положительные ионы
- 8. Рассмотрим, что происходит, когда ионы достигают электродов (на примере СuCl2) CuCl2 → Cu2+ + 2Cl -
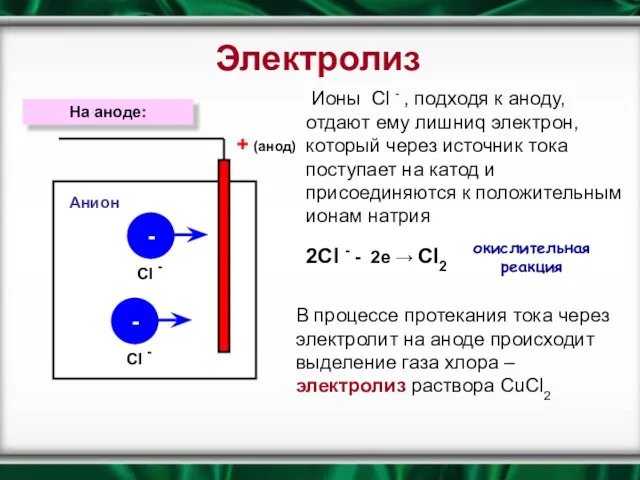
- 9. На аноде: + (анод) - - Ионы Сl - , подходя к аноду, отдают ему лишниq
- 10. При ионной проводимости прохождение тока связано с переносом вещества. Выделение вещества на электродах вследствие окислительно –
- 11. Сопротивление растворов электролитов Закон Ома справедлив при неизменной концентрации раствора и температуре. Сопротивление растворов электролитов уменьшается
- 12. Законы электролиза Этот закон был открыт опытным путем в 1833 году английским ученым Майклом Фарадеем. Закон
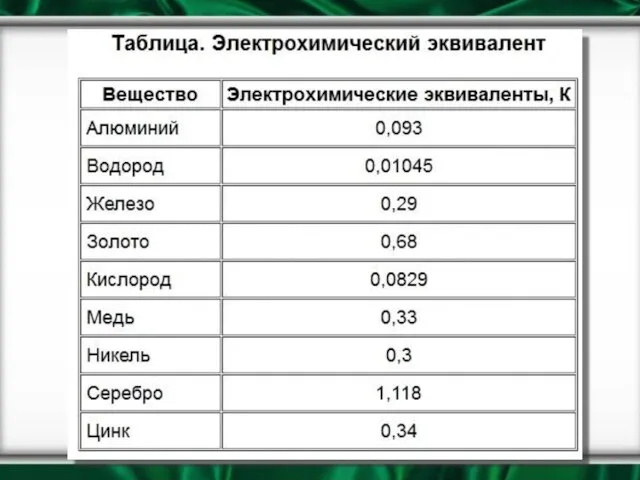
- 13. Электрохимический эквивалент вещества Электрохимический эквивалент вещества зависит от рода вещества (от молярной массы вещества «М» и
- 15. Определение заряда электрона с помощью электролиза Зная массу выделившегося вещества при прохождении заряда, молярную массу, валентность
- 16. Постоянная Фарадея Физический смысл: F – численно равна заряду, который надо пропустить через раствор электролита, чтобы
- 17. Применение электролиза Гальваностегия – декоративное или антикоррозийное покрытие металлических изделий тонким слоем другого металла (никелирование, хромирование,
- 19. Применение электролиза Гальванопластика – электролитическое изготовление металлических копий, рельефных предметов Точность копирования формы предмета очень высокая,
- 21. Применение электролиза Гальванотехника - это отрасль прикладной электрохимии. Основателем гальванотехники и ее широчайшего применения является Борис
- 22. Применение электролиза Электрометаллургия – получение чистых металлов (Al, Na, Mg, Be) при электролизе расплавленных руд
- 24. Применение электролиза Рафинирование металлов – очистка металлов от примесей с помощью электролиза, когда неочищенный металл является
- 27. Скачать презентацию




















 Качество обработанной поверхности
Качество обработанной поверхности Презентация на тему Атомная физика (11 класс)
Презентация на тему Атомная физика (11 класс) 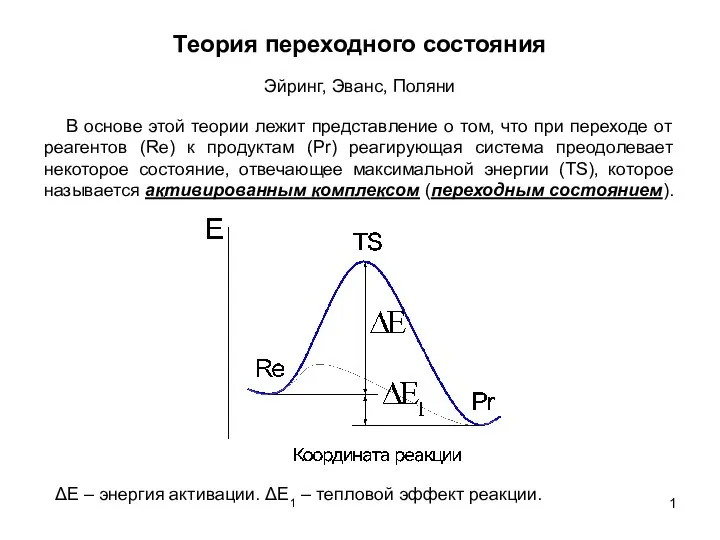 Теория переходного состояния. Эйринг, Эванс, Поляни. (Лекция 5)
Теория переходного состояния. Эйринг, Эванс, Поляни. (Лекция 5) Изобретение радио. Принципы радиосвязи
Изобретение радио. Принципы радиосвязи Надпровідність
Надпровідність Презентация на тему Последовательное соединение проводников (8 класс)
Презентация на тему Последовательное соединение проводников (8 класс)  Презентация на тему Законы термодинамики
Презентация на тему Законы термодинамики  Уход за швейной машиной
Уход за швейной машиной Сверхпроводимость материалов
Сверхпроводимость материалов Презентация на тему ПРОБЛЕМНОЕ ОБУЧЕНИЕ на уроках ФИЗИКИ
Презентация на тему ПРОБЛЕМНОЕ ОБУЧЕНИЕ на уроках ФИЗИКИ  Лекция 1
Лекция 1 Пример решения задачи. Изохорный процесс
Пример решения задачи. Изохорный процесс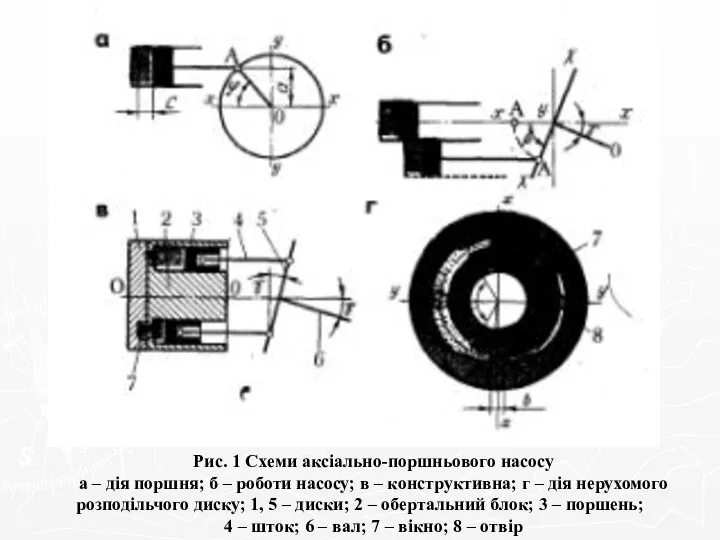 Схеми аксіально-поршньового насосу. Билет 8
Схеми аксіально-поршньового насосу. Билет 8 Основные понятия статики. Лекция 1
Основные понятия статики. Лекция 1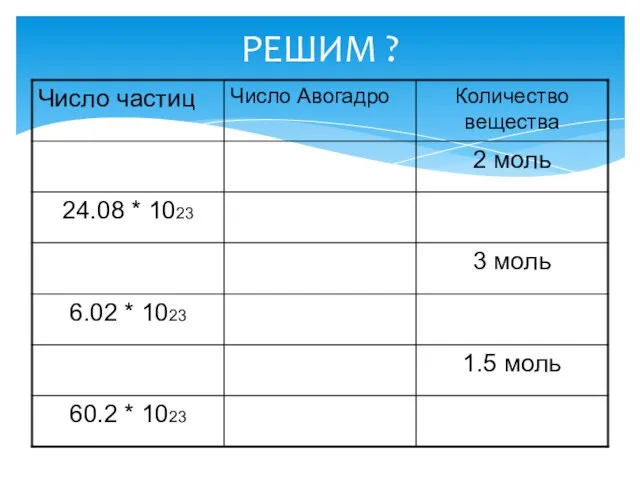 Молярный объем газообразных веществ
Молярный объем газообразных веществ Электричество. Простейшая электрическая цепь. Первая помощь при ударе электрическим током
Электричество. Простейшая электрическая цепь. Первая помощь при ударе электрическим током Понятие радиационной защиты. Классификация защит по объекту защиты. Другие классификации защит
Понятие радиационной защиты. Классификация защит по объекту защиты. Другие классификации защит Напряжённость электрического поля. Тест
Напряжённость электрического поля. Тест Давление. Свойства и сила давления
Давление. Свойства и сила давления Оптические датчики лазерный гироскоп, болометр, датчики освещенности
Оптические датчики лазерный гироскоп, болометр, датчики освещенности Квантовая природа света
Квантовая природа света Механическая работа. Единицы работы
Механическая работа. Единицы работы Валы и оси редуктора
Валы и оси редуктора Смачивание. Капиллярнность
Смачивание. Капиллярнность Презентация на тему Давление
Презентация на тему Давление  Продолжение молекулярной физики
Продолжение молекулярной физики Семинар повышения квалификации специалистов по установке и обслуживанию газобаллонного оборудования современных автомобилей
Семинар повышения квалификации специалистов по установке и обслуживанию газобаллонного оборудования современных автомобилей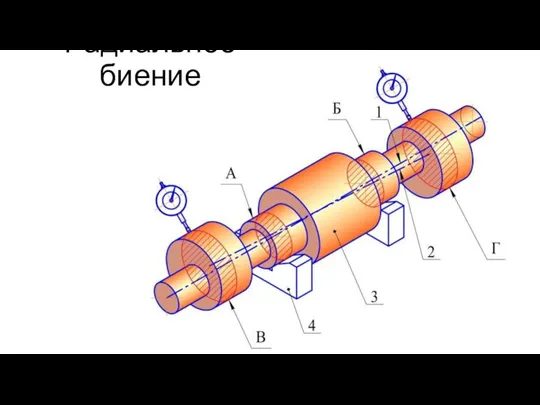 Радиальное биение
Радиальное биение