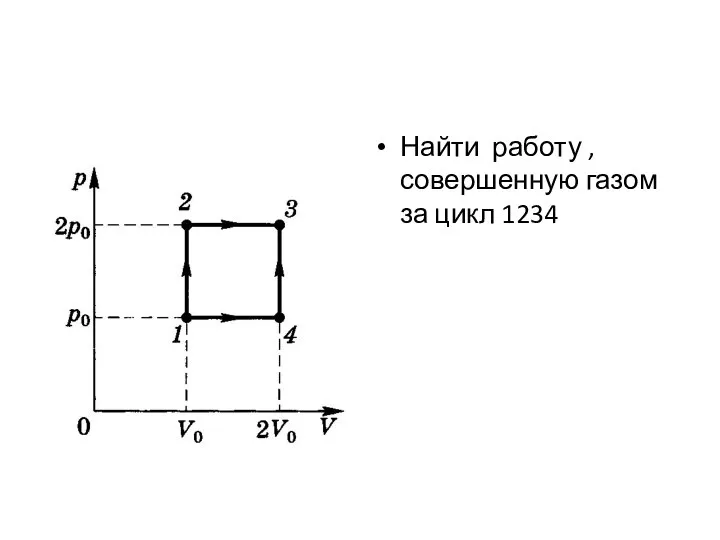
Слайд 2Найти работу , совершенную газом за цикл 1234
Слайд 3Количество теплоты пропорционально массе тела и изменению температуры. Но для газов коэффициент

пропорциональности зависит от способа изменения состояния газа:
для изохорного процесса
для изобарного процесса
Слайд 5Степень свободы
-любое независимое движение, которое может совершать тело.
Для одноатомной молекулы i=3
Для двухатомной

молекулы i=5
Для многоатомной молекулы i=6
Слайд 6Закон равнораспределения
На каждую степень свободы приходится 1/2kT Дж

Слайд 8Молярные теплоемкости
-теплоемкости газа в количестве 1 моль
С=сМ

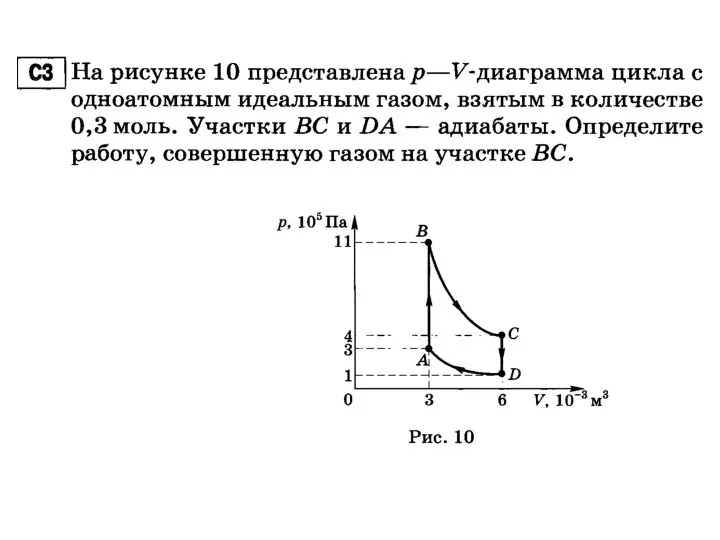
Слайд 9Адиабатный процесс – это модель термодинамического процесса, происходящего в системе без теплообмена

с окружающей средой.
Линия на термодинамической диаграмме состояний системы, изображающая равновесный (обратимый) адиабатический процесс, называется адиабатой
Для этого процесса , Q = 0, А=-ΔU
В случае одноатомного идеального газа


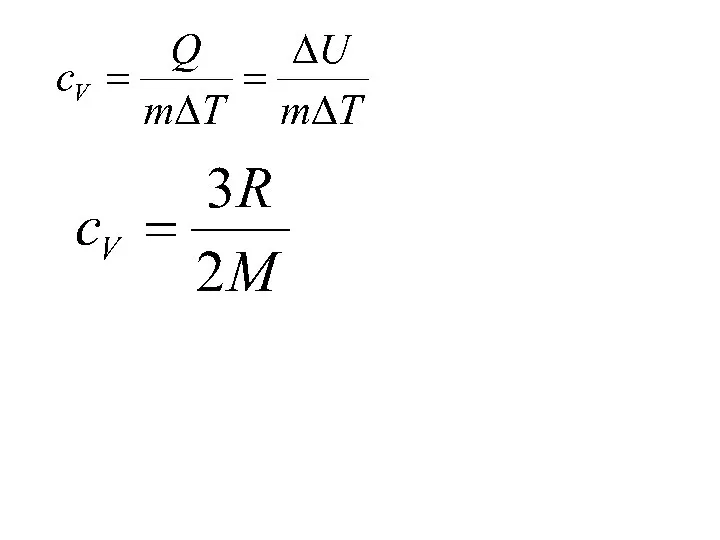


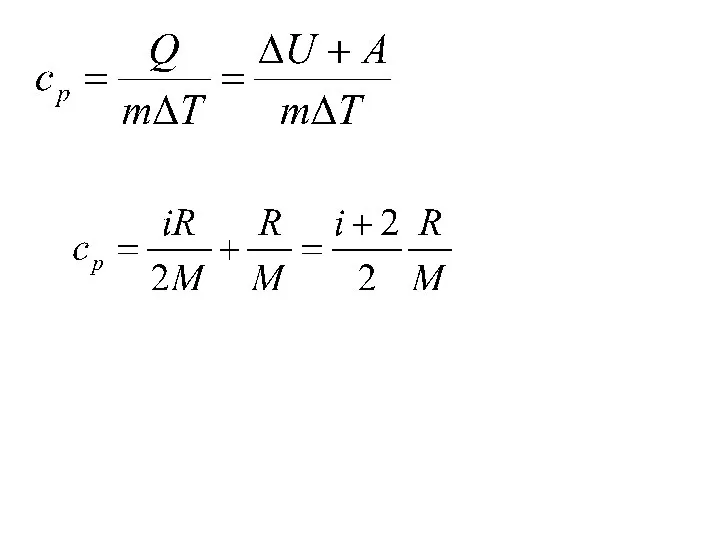




 tormoznaya_sistema_TO
tormoznaya_sistema_TO Движение по окружности
Движение по окружности Гидравлический удар и его предотвращение
Гидравлический удар и его предотвращение Движение тела, брошенного вертикально вверх. 9 класс
Движение тела, брошенного вертикально вверх. 9 класс Графен – бұл кәдімгі алмаз бен графиттен
Графен – бұл кәдімгі алмаз бен графиттен Механическое движение
Механическое движение Учение об атоме. Квантовая теория строения атома
Учение об атоме. Квантовая теория строения атома Светодиодный светильник
Светодиодный светильник Презентация на тему Снег
Презентация на тему Снег  Отражающие свойства объектов. Рефракция атмосферы
Отражающие свойства объектов. Рефракция атмосферы Цилиндрические зубчатые передачи
Цилиндрические зубчатые передачи Зависимость центростремительной силы от массы, радиуса и угловой скорости
Зависимость центростремительной силы от массы, радиуса и угловой скорости Молекулы и атомы. 7 класс
Молекулы и атомы. 7 класс Методика измерений. Виды измерений
Методика измерений. Виды измерений Пневматика
Пневматика История Ультразвукового Контроля
История Ультразвукового Контроля Практикум по решению задач на движение тела под действием нескольких сил
Практикум по решению задач на движение тела под действием нескольких сил Колебательный контур. Подготовка к ЕГЭ
Колебательный контур. Подготовка к ЕГЭ Зависимость давления твердых тел от силы давления и от площади поверхности, на которую действует сила давления
Зависимость давления твердых тел от силы давления и от площади поверхности, на которую действует сила давления Электрические машины
Электрические машины Дискретные случайные процессы (тема 7)
Дискретные случайные процессы (тема 7) Кодирование и обработка звуковой информации
Кодирование и обработка звуковой информации Что значит минута
Что значит минута 540576.pptx
540576.pptx Контактная разность потенциалов
Контактная разность потенциалов Простые механизмы. Работа
Простые механизмы. Работа Презентация по физике "Механическое движение" -
Презентация по физике "Механическое движение" -  Примеры наклонной плоскости
Примеры наклонной плоскости