Содержание
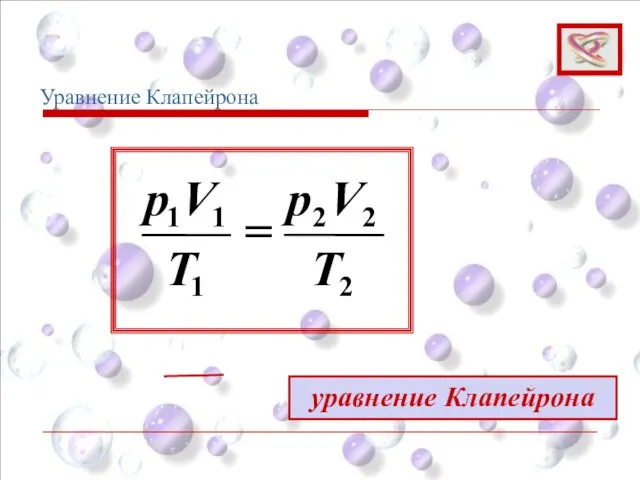
- 2. 2 2 2 1 1 1 T V р T V р = уравнение Клапейрона Уравнение
- 3. Уравнение Клапейрона (1)
- 4. Один моль любого газа при нормальных условиях (Т = 273 К и р = 1,013∙105 Па)
- 5. Уравнение Менделеева-Клапейрона
- 6. Уравнение Менделеева-Клапейрона (молярная газовая постоянная)
- 7. Тогда для 1 моль газа уравнение (1) можно записать в виде: Уравнение Менделеева-Клапейрона для 1 моль
- 8. Уравнение Менделеева-Клапейрона
- 9. Задача молекулярно-кинетической теории состоит в том, чтобы установить связь между микроскопическими (масса, скорость, кинетическая энергия молекул)
- 10. Газ, состоящий из отдельных атомов, а не молекул, называют одноатомным. К одноатомным газам относят инертные газы
- 11. Основное уравнение МКТ газов р – давление газа на стенку сосуда. С другой стороны, сила F,
- 12. Или Основное уравнение МКТ (5) Основное уравнение МКТ газов ‒ концентрация молекул
- 13. Основное уравнение МКТ газов Средняя кинетическая энергия хаотического движения молекул газа Откуда (5)
- 14. Основное уравнение МКТ газов (6) Основное уравнение МКТ
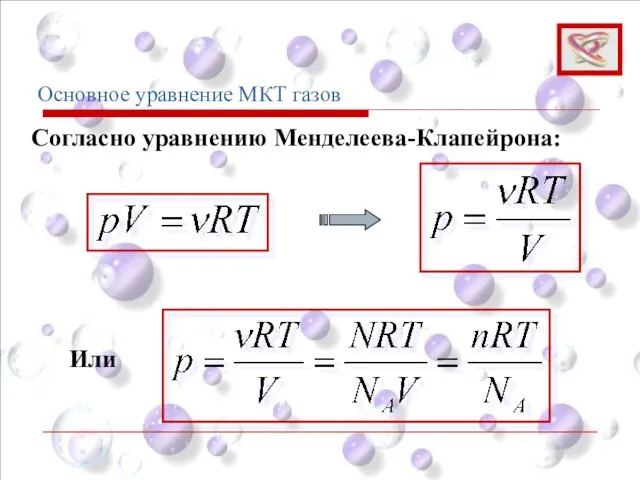
- 15. Основное уравнение МКТ газов Согласно уравнению Менделеева-Клапейрона: Или
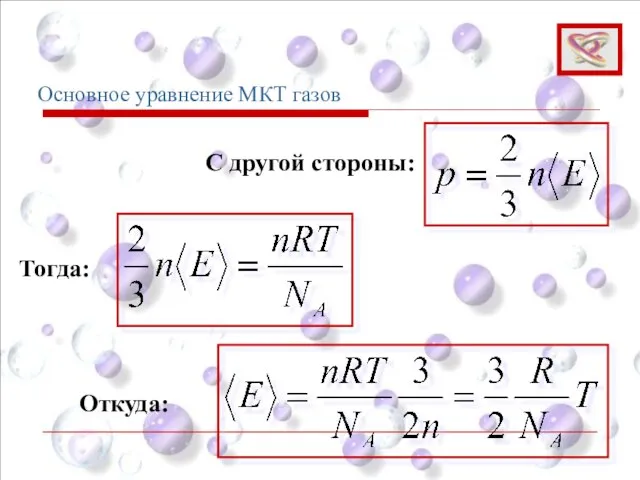
- 16. Основное уравнение МКТ газов Тогда: С другой стороны: Откуда:
- 17. Основное уравнение МКТ газов
- 18. Основное уравнение МКТ газов Тогда: Средняя кинетическая энергия хаотического движения молекул газа прямо пропорциональна абсолютной температуре.
- 20. Скачать презентацию














 Газовые законы
Газовые законы Презентация на тему Состояние невесомости
Презентация на тему Состояние невесомости  Законы сохранения в механике
Законы сохранения в механике Физика ядра
Физика ядра История Ультразвукового Контроля
История Ультразвукового Контроля Тяговый расчет трактора
Тяговый расчет трактора Закон Джоуля-Ленца
Закон Джоуля-Ленца Лекция 25
Лекция 25 Постоянные магниты. Магнитное поле Земли.
Постоянные магниты. Магнитное поле Земли. Упругие свойства среды. Лекция 1.13
Упругие свойства среды. Лекция 1.13 Решения задач по теме Механическое движение, 9 класс
Решения задач по теме Механическое движение, 9 класс Кең ауқымды вибратор
Кең ауқымды вибратор Радионавигация
Радионавигация Звуковые волны
Звуковые волны Линзы. Виды линз. Условное обозначение линз. Собирающие линзы
Линзы. Виды линз. Условное обозначение линз. Собирающие линзы Теория Бора для атома водорода
Теория Бора для атома водорода Контроль формы оптических поверхностей пробным стеклом, на интерферометре Физо и на неравноплечем лазерном интерферометре
Контроль формы оптических поверхностей пробным стеклом, на интерферометре Физо и на неравноплечем лазерном интерферометре Тезаурус
Тезаурус Повышение КПД ГТУ путём внедрения регенеративного цикла
Повышение КПД ГТУ путём внедрения регенеративного цикла Взрывозащищенный светильник для взрывоопасных зон(Серия А)
Взрывозащищенный светильник для взрывоопасных зон(Серия А) Построение изображеия в линзах и формула линзы. 11 класс
Построение изображеия в линзах и формула линзы. 11 класс Основы взаимозаменяемости и технические измерения
Основы взаимозаменяемости и технические измерения Короткое замыкание
Короткое замыкание Урок 21+ Розв'язування задач
Урок 21+ Розв'язування задач Презентация на тему Введение в космологию
Презентация на тему Введение в космологию  Сложное движение точки
Сложное движение точки Манометры
Манометры Модульные технологии как технологии здоровьесбережения
Модульные технологии как технологии здоровьесбережения