Содержание
- 2. План Классификация физических и физико-химических методов анализа. Достоинства и недостатки физических и физико-химических методов анализа. Классификация
- 3. Классификация физических и физико-химических методов анализа: Оптические методы. Хроматографические методы. Электрохимические методы. Радиометрические методы. Термические методы.
- 4. Достоинства физических и физико-химических методов анализа: Низкий предел обнаружения (1-10-9 мкг) определяемого вещества. Высокая чувствительность. Высокая
- 5. Недостатки физических и физико-химических методов анализа: Иногда воспроизводимость результатов хуже. Погрешности определений с использованием физических и
- 6. Классификация оптических методов анализа: По изучаемым объектам: атомный и молекулярный спектральный анализ. По характеру взаимодействия электромагнитного
- 7. По области электромагнитного спектра. Спектроскопия (спектрофотометрия) в УВИ области спектра, т.е. в ближней ультрафиолетовой (УФ) области
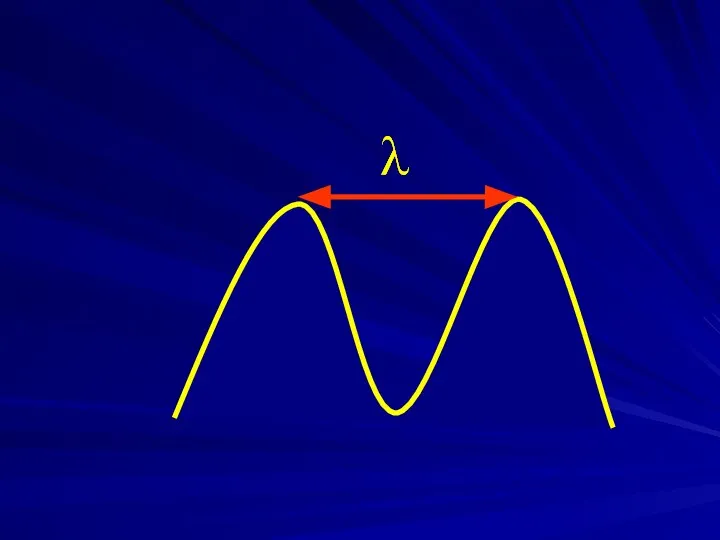
- 8. Общие положения Длина волны λ - расстояние, проходимое волной за время одного полного колебания. Чаще измеряют
- 10. A B Г
- 11. Пропускание
- 12. Оптическая плотность
- 13. Закон Бугера-Ламберта (в 1729 г. - Бугер, в 1760 г. - Ламберт): однородные слои одного и
- 14. Закон Бера (1852 г.): оптическая плотность раствора прямопропорциональна концентрации растворенного вещества при постоянной толщине слоя ,
- 15. Объединенный закон Бугера-Ламберта-Бера: оптическая плотность прямопропорциональна концентрации растворенного вещества и толщине поглощающего слоя раствора. k -
- 16. Если концентрация С выражена в молях на литр, l - в см, то k представляет собой
- 17. Если концентрация раствора выражена в процентах, то k представляет собой удельный коэффициент поглощения и обозначается или
- 18. Связь между молярным и удельным коэффициентами поглощения выражается уравнениями: М - молекулярная масса вещества
- 19. К физико-химическим причинам относятся: 1. Несоответствие подставляемого в уравнение значения С истинной концентрации поглощающего вещества. Это
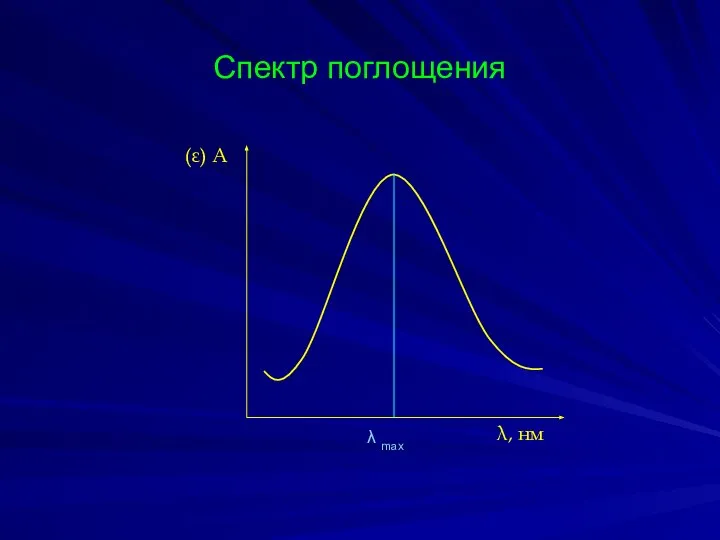
- 20. Спектр поглощения (ε) А λ, нм λ max
- 21. Выбор длины волны Величина молярного коэффициента поглощения должна быть большой. Поэтому в большинстве случаев λанал выбирают
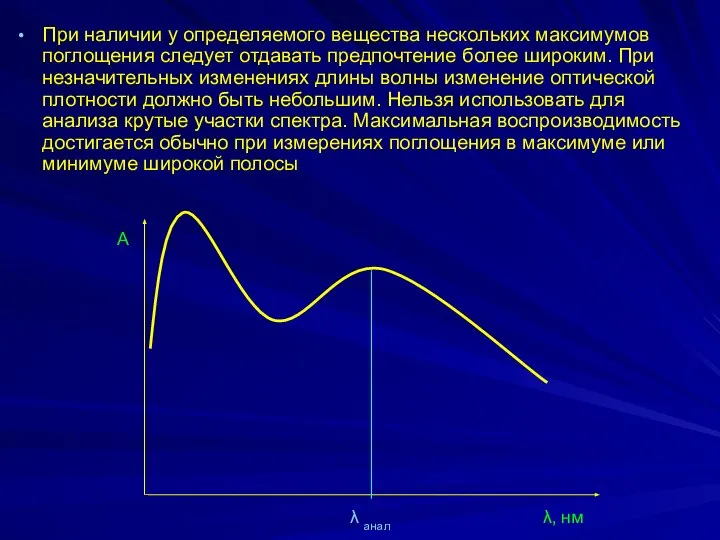
- 22. При наличии у определяемого вещества нескольких максимумов поглощения следует отдавать предпочтение более широким. При незначительных изменениях
- 23. Некоторые вещества изменяют свои свойства при изменении рН среды, окислительно-восстановительного потенциала, а также при таутомерных превращениях.
- 24. Если в исследуемом растворе присутствуют примеси, выбор длины волны проводят так, чтобы отношение показателя поглощения вещества
- 25. Проверка подчинения поглощения исследуемыми растворами закону Бугера-Ламберта-Бера
- 26. Параллельно с исследуемым в тех же условиях готовят стандартный раствор (раствор с точно известной концентрацией определяемого
- 27. 2. Определение по удельному или молярному показателю поглощения Требует обязательного соблюдения основного закона светопоглощения:
- 28. 3. По калибровочной кривой Для построения калибровочного графика готовят серию стандартных растворов (5-8 растворов, отличающихся по
- 29. 4. Метод добавок Представляет собой разновидность метода стандарта. Определение основано на сравнении оптической плотности исследуемого раствора
- 30. 5. Дифференциальный метод Измеряют оптические плотности исследуемого и стандартного окрашенных растворов не по отношению к чистому
- 31. Графический способ Для построения градуировочного графика готовят серию стандартных растворов с концентрациями С1, С2....Сn (Сn>…С2>C1) и
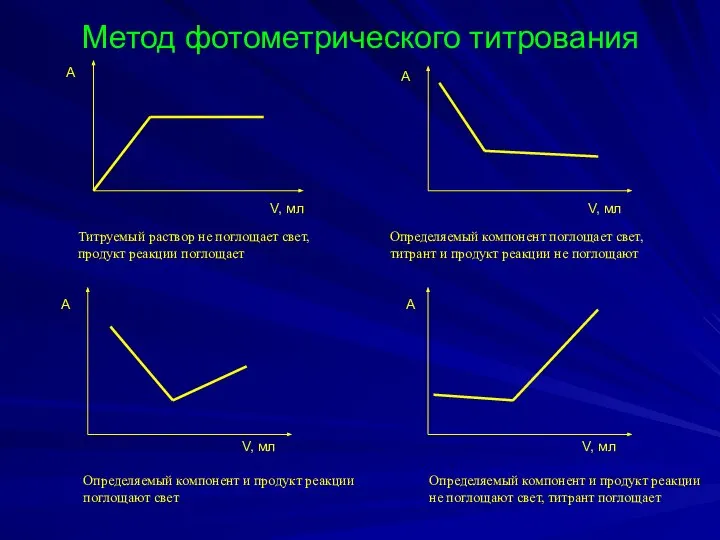
- 32. Метод фотометрического титрования V, мл V, мл V, мл V, мл А А А А Титруемый
- 33. Анализ многокомпонентных систем В 1873 г. К. Фирордтом на примере двухкомпонентной смеси был впервые сформулирован и
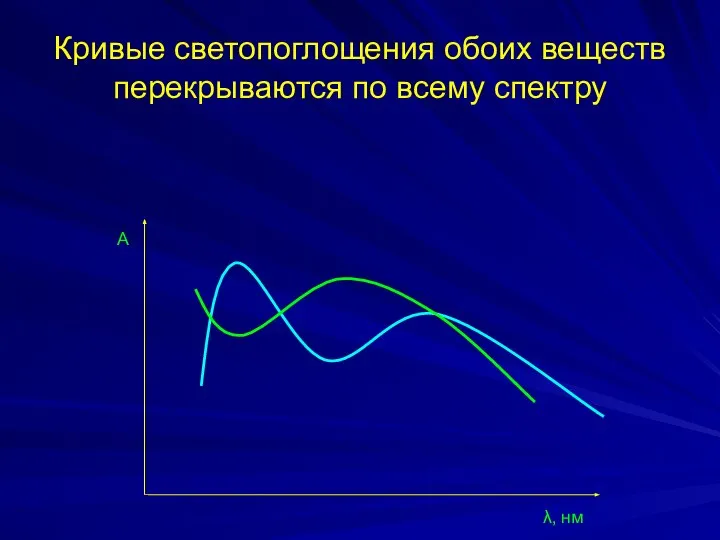
- 34. Спектрофотометрический анализ двухкомпонентных систем Кривые светопоглощения обоих веществ перекрываются по всему спектру. Кривые светопоглощения обоих веществ
- 35. Кривые светопоглощения обоих веществ перекрываются по всему спектру А λ, нм
- 36. С1 и С2 – концентрации компонентов в моль/л; - молярные коэффициенты поглощения при λ1 и λ2.
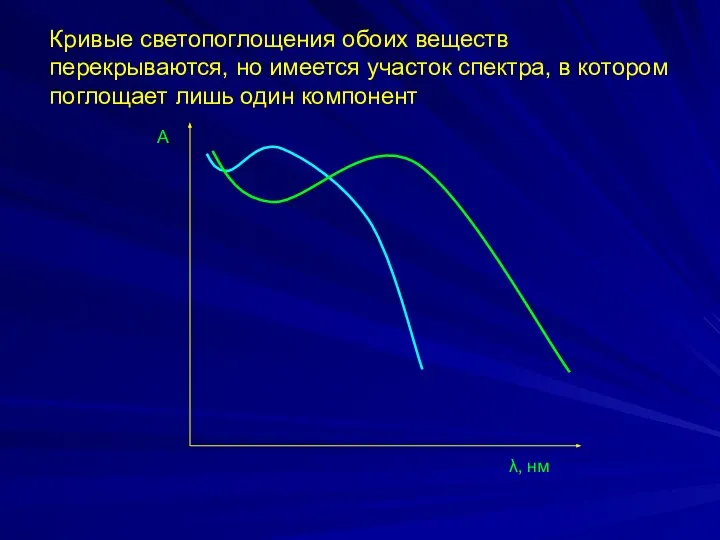
- 37. А λ, нм Кривые светопоглощения обоих веществ перекрываются, но имеется участок спектра, в котором поглощает лишь
- 40. Скачать презентацию






























 Электронные средства обучения
Электронные средства обучения Электрический ток в различных средах
Электрический ток в различных средах Явление тяготения. Сила тяжести
Явление тяготения. Сила тяжести Тепловые двигатели
Тепловые двигатели Силы всемирного тяготения
Силы всемирного тяготения Переменный электрический ток. Вынужденные электромагнитные колебания
Переменный электрический ток. Вынужденные электромагнитные колебания Волоконная оптика, ее применение в медицине
Волоконная оптика, ее применение в медицине Некогерентность рассеяния. (Тема 15)
Некогерентность рассеяния. (Тема 15) Допуски и посадки
Допуски и посадки Сила тока и напряжение
Сила тока и напряжение Закон сохранения энергии, работа и мощность в механике
Закон сохранения энергии, работа и мощность в механике Электромагнитные колебания. Переменный электрический ток
Электромагнитные колебания. Переменный электрический ток Опиливание заготовок из металла и пластмассы
Опиливание заготовок из металла и пластмассы Основы магнитных явлений и их применения в электротехнике
Основы магнитных явлений и их применения в электротехнике Технические противоречия и приемы их разрешения
Технические противоречия и приемы их разрешения Zakon_vsemirnogo_tyagotenia
Zakon_vsemirnogo_tyagotenia Електромагнітні явища
Електромагнітні явища Колебания. Лекция № 8
Колебания. Лекция № 8 Равномерное движение
Равномерное движение Механика. Гравитационные силы. Силы инерции
Механика. Гравитационные силы. Силы инерции Понятие импульса
Понятие импульса Методы измерения длительности люминесценции
Методы измерения длительности люминесценции Экзотические виды радиоактивности. (Тема 1.6)
Экзотические виды радиоактивности. (Тема 1.6) Что такое давление?
Что такое давление? Презентация на тему Физика в картинках
Презентация на тему Физика в картинках  Плавание тел. Условие плавания тел
Плавание тел. Условие плавания тел Статика. Устойчивое равновесие тел
Статика. Устойчивое равновесие тел Презентация на тему История изобретения паровых машин
Презентация на тему История изобретения паровых машин