Слайд 2Три пути ведут к знанию:
Путь размышления – это путь самый благородный,
Путь подражания

– это путь самый легкий,
И путь опыта – это путь самый горький.
Конфуций
древний мыслитель и философ Китая
Слайд 3
ПУТЬ РАЗМЫШЛЕНИЯ – ЭТО ПУТЬ САМЫЙ БЛАГОРОДНЫЙ
Предложите способ вычисления атмосферного давления
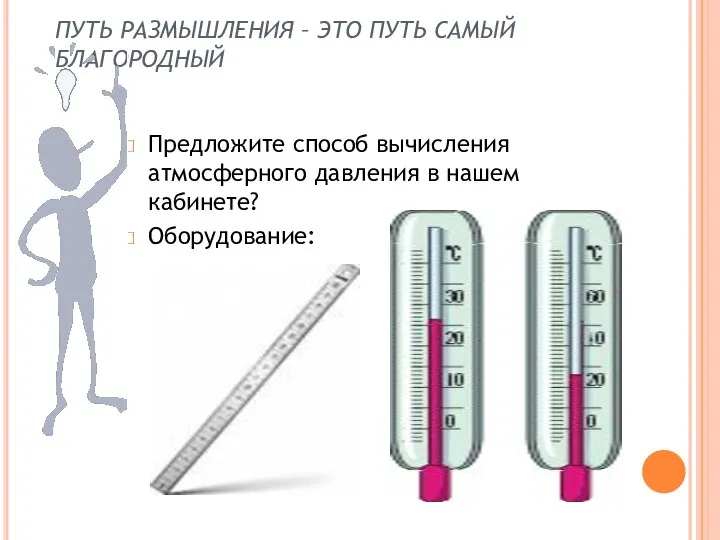
в нашем кабинете?
Оборудование:
Слайд 4ПРОБЛЕМА
Термометром можно измерить температуру, линейкой измерить размеры комнаты и вычислить объем.

А как установить зависимость между давлением, объемом и температурой?
Уравнение, определяющее связь температуры, объема и давления тел, называется уравнением состояния.
Слайд 5
ДЛЯ ЧЕГО НУЖНО УРАВНЕНИЕ СОСТОЯНИЯ?
1) Уравнение состояния позволяет определить одну из

величин, характеризующих состояние, например, температуру, если известны две другие величины. Это используется в термометрах.
2) Зная уравнение состояния можно сказать, как протекают процессы при определенных внешних условиях: например, как будет меняться давление газа, если увеличить его объем при неизменной температуре.
3) Зная уравнение состояние, можно определить, как меняется состояние системы, если она совершает работу, или получает теплоту от окружающих тел.
Слайд 6 УРАВНЕНИЕ СОСТОЯНИЯ ИДЕАЛЬНОГО ГАЗА
Клапейрон
Бенуа Поль Эмиль
(1799-1864 г.г.)
Дмитрий Иванович Менделеев

(1834 – 1907г.г.)
Слайд 7ПОЗНАВАТЕЛЬНАЯ ЗАДАЧА
Вывести физический закон, устанавливающий зависимость между тремя макроскопическими параметрами — p,

V, T идеального газа.
Слайд 8РАССУЖДАЕМ!
1. От чего зависит давление газа?
2. Сформулируйте зависимость давления идеального газа

от концентрации и температуры?
3. Что называется концентрацией?
4. Выразите число молекул N через микропараметры
3. Какую физическую величину называют постоянной Авогадро?
4. Каков физический смысл постоянной Больцмана? Чему она равна?
Слайд 9РАССУЖДАЕМ
P = nkT
n = N/V
N = mNA /M
Подумайте, каким образом можно связать

три последних выражения, которые содержат интересующие нас макропараметры P, V, T?
Слайд 10СЛЕДУЮЩИЙ ПУТЬ - ПУТЬ ПОДРАЖАНИЯ – ЭТО ПУТЬ САМЫЙ ЛЕГКИЙ.
Работа с учебником

§68.
План работы:
1.Вывести уравнение состояния идеального газа Менделеева-Клапейрона
2.Ввести универсальную газовую постоянную R. Выяснить физический смысл универсальной газовой постоянной R.
3. Вывести связь между давлением, объемом и температурой идеального газа в двух любых состояниях – уравнение Клапейрона.
Слайд 11И ПУТЬ ОПЫТА – ЭТО ПУТЬ САМЫЙ ГОРЬКИЙ
2. Работа с ЭОР.
Уравнение состояния

идеального газа (П)
Самооценка по журналу успеваемости ОМС
Оценку по пятибалльной системе можно выставить по следующему принципу:
«5» ставится, если тестовый балл превышает 80 %;
«4» ставится, если тестовый балл находится в промежутке от 60 % до 80 %;
«3» ставится, если тестовый балл находится в промежутке от 40 % до 60 %;
«2» ставится, если тестовый балл находится в промежутке менее 40 %.
Слайд 12ИНФОРМАЦИЯ О ДОМАШНЕМ ЗАДАНИИ
§ 68 Стр.189 Пример 1, 2 решения задач

(конспект) Упр. 13 (4, 5, 6)
Дополнительные задания (по желанию):
1.Изложите в форме эссе своё мнение взаимосвязи между величинами уравнения состояния идеального газа и его практического применения.
2. Подготовьте сообщение о великом русском ученом Д.И. Менделееве и его вкладе в развитие МКТ.
3. Подготовьте сообщение о Клапейроне.











 Исследование электромагнитного загрязения города Челябинска
Исследование электромагнитного загрязения города Челябинска Лекция 3 Электромагнитные переходные процессы электрических цепях
Лекция 3 Электромагнитные переходные процессы электрических цепях Закон Джоуля-Ленца. Плотность тока. Скорость движения электронов в проводнике
Закон Джоуля-Ленца. Плотность тока. Скорость движения электронов в проводнике Презентация на тему Электрический ток
Презентация на тему Электрический ток  Тела, вещества, частицы
Тела, вещества, частицы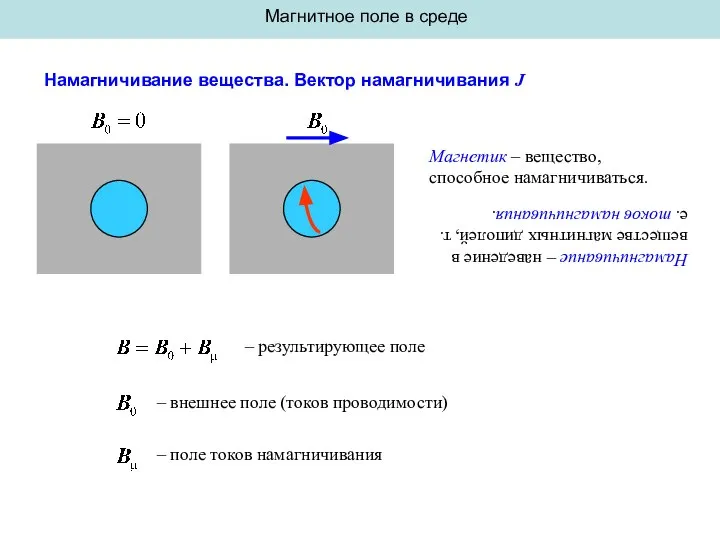 Намагничивание вещества. Вектор намагничивания J
Намагничивание вещества. Вектор намагничивания J Опрделение силы веса, координат центра тяжести и предельных значений статических углов против опрокидывания трактора
Опрделение силы веса, координат центра тяжести и предельных значений статических углов против опрокидывания трактора Дисперсия света. Опыт И. Ньютона
Дисперсия света. Опыт И. Ньютона Модуль Юнга
Модуль Юнга Конфигурации (проводка) моторов HI-FINITY
Конфигурации (проводка) моторов HI-FINITY Задача по физике. Вариант №9 (решение)
Задача по физике. Вариант №9 (решение) Электризация. Взаимодействие заряженных тел
Электризация. Взаимодействие заряженных тел Тепловое излучение. Лекция 30
Тепловое излучение. Лекция 30 Отражение света
Отражение света ВКР: Система стеклоочистки лобового стекла
ВКР: Система стеклоочистки лобового стекла Переменное прямолинейное движение
Переменное прямолинейное движение Применение переменного тока. (Лекция 9)
Применение переменного тока. (Лекция 9) Роль машиностроения и этапы его развития. Тема 1
Роль машиностроения и этапы его развития. Тема 1 Растяжение и сжатие
Растяжение и сжатие Постоянный электрический ток. Конденсаторы
Постоянный электрический ток. Конденсаторы 2_Dinamika
2_Dinamika Электростатика. Лекция 1
Электростатика. Лекция 1 Закон сохранения импульса. Законы Ньютона
Закон сохранения импульса. Законы Ньютона Электрические цепи переменного тока
Электрические цепи переменного тока Энергия — Жизнь
Энергия — Жизнь Электромонтажные и сборочные технологии
Электромонтажные и сборочные технологии Закон сохранения импульса
Закон сохранения импульса Индуктивный преобразователь
Индуктивный преобразователь