Слайд 3ИЗОТОПЫ
Изотопы – это разновидности атомов одного химического элемента, которые отличаются числом нейтронов

в ядре, то есть массой ядра
Слайд 4ХИМИЧЕСКИЙ ЭЛЕМЕНТ представляет собой совокупность его изотопов

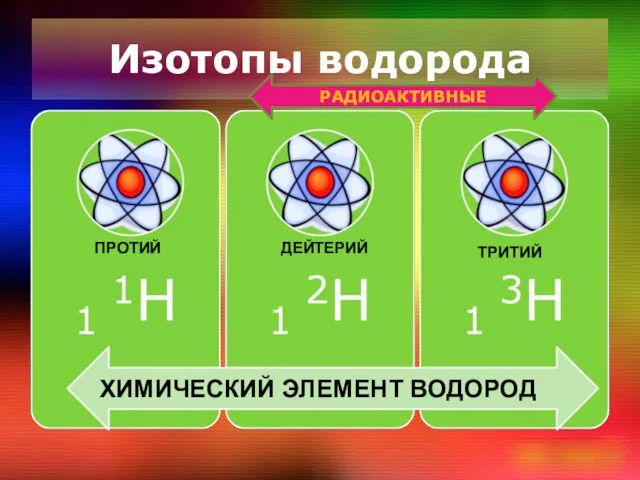
Слайд 5Изотопы водорода
ХИМИЧЕСКИЙ ЭЛЕМЕНТ ВОДОРОД
ПРОТИЙ
ДЕЙТЕРИЙ
ТРИТИЙ
РАДИОАКТИВНЫЕ
Слайд 6ХИМИЧЕСКИЕ ЭЛЕМЕНТЫ, КОТОРЫЕ СОСТОЯТ ТОЛЬКО ИЗ РАДИОАКТИВНЫХ ИЗОТОПОВ, НАЗЫВАЮТСЯ РАДИОАКТИВНЫМИ
(порядковые номера более

83)
Слайд 7Почему относительная атомная масса выражается не целым числом?
ОТНОСИТЕЛЬНАЯ АТОМНАЯ МАССА ХИМИЧЕСКОГО

ЭЛЕМЕНТА РАССЧИТЫВАЕТСЯ С УЧЕТОМ РАСПРОСТРАНЕННОСТИ ЕГО ИЗОТОПОВ В ПРИРОДЕ
Слайд 8Например,
Хлор в природе встречается в виде изотопов 35Cl (75%) и 37Cl (25%)
Вычислите

относительную атомную массу хлора:
Ar = 35∙0,75 + 37∙0,25 = 35,5








 MadameTussaud’s Музей Восковых фигур Мадам Тюссо
MadameTussaud’s Музей Восковых фигур Мадам Тюссо Место учебного исследования в программе Intel «Обучение для будущего»
Место учебного исследования в программе Intel «Обучение для будущего» Потребительские кредиты
Потребительские кредиты Организация пастбищного содержания животных
Организация пастбищного содержания животных А
А Структура ВС РФ
Структура ВС РФ Северная Америка
Северная Америка «Как продолжается детство»
«Как продолжается детство» Молодые менеджеры и предприниматели Кубани
Молодые менеджеры и предприниматели Кубани Презентация на тему Углекислый газ СО2
Презентация на тему Углекислый газ СО2  Солнце воздух и вода – наши лучшие друзья
Солнце воздух и вода – наши лучшие друзья Лапта. История развития
Лапта. История развития Что такое система LanDrive ? LanDrive – это универсальная система управления по витой паре. Предназначена для автоматического и централиз
Что такое система LanDrive ? LanDrive – это универсальная система управления по витой паре. Предназначена для автоматического и централиз Презентация на тему Экологические кризисы и экологические катастрофы
Презентация на тему Экологические кризисы и экологические катастрофы История Громова Процессы на постсоветском пространстве
История Громова Процессы на постсоветском пространстве Шамшур
Шамшур Приобщение дошкольников к народной культуре в разных видах музыкальной деятельности»
Приобщение дошкольников к народной культуре в разных видах музыкальной деятельности» Тема урока
Тема урока Понятие о причастном обороте. Знаки препинания в предложениях с причастными оборотами. 6 класс
Понятие о причастном обороте. Знаки препинания в предложениях с причастными оборотами. 6 класс Презентация на тему Свет и его законы
Презентация на тему Свет и его законы  Презентация "Николай I и его портреты в изобразительном искусстве" - скачать презентации по МХК
Презентация "Николай I и его портреты в изобразительном искусстве" - скачать презентации по МХК Art City. Подбор квартиры
Art City. Подбор квартиры Фалсафа - 5
Фалсафа - 5 врол
врол Бабаево – взгляд с любовью (городской путеводитель)
Бабаево – взгляд с любовью (городской путеводитель) Бесприборные тесты для подтверждения ВИЧ-Инфекции
Бесприборные тесты для подтверждения ВИЧ-Инфекции Техника безопасностииорганизация рабочего места
Техника безопасностииорганизация рабочего места Конспект урока по окружающему миру (история)с использованием информационно-коммуникационных технологий (3 класс, программа 1-4).
Конспект урока по окружающему миру (история)с использованием информационно-коммуникационных технологий (3 класс, программа 1-4).