Содержание
- 2. Задача. Найти объем кислорода (при н.у.), который потребуется для полного сгорания 10,8 г алюминия m(Al) n(Al)
- 3. Решение 4Al + 3O2 = 2Al2O3
- 4. Задача на примеси Найти объем кислорода (при н.у.), который потребуется для полного сгорания 10,2 г сероводорода,
- 5. Решение 2H2S + 3O2 = 2H2O + 2SO2
- 6. Задача на выход Найти массу фосфора, который требуется для получения 25,2 г оксида фосфора(V), если выход
- 7. Решение 4P + 5O2 = 2P2O5 (продукт реакции)
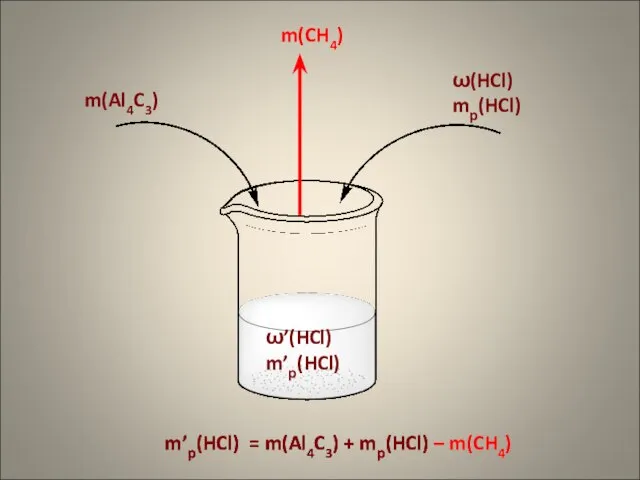
- 8. Задание С4 1. При обработке карбида алюминия раствором соляной кислоты, масса которого 320 г и массовая
- 9. m(Al4C3) ω(HCl) mр(HCl) m(CH4) m’р(HCl) = m(Al4C3) + mр(HCl) ω’(HCl) m’р(HCl) m’р(HCl) = m(Al4C3) + mр(HCl)
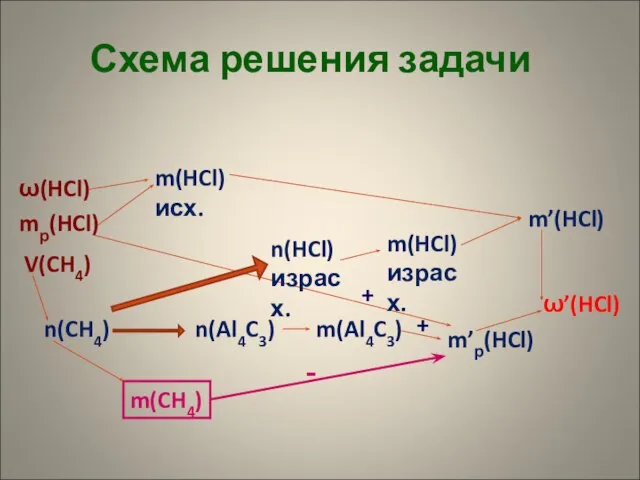
- 10. + ω(HCl) mр(HCl) V(CH4) m(HCl) исх. ω’(HCl) m’р(HCl) m’(HCl) n(CH4) m(CH4) n(Al4C3) m(Al4C3) n(HCl) израсх. m(HCl)
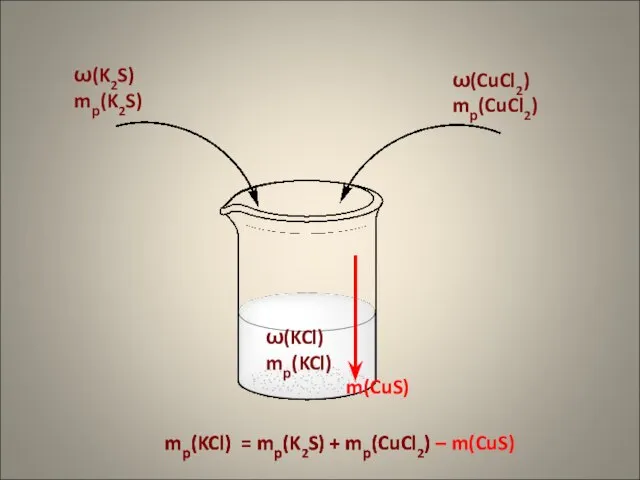
- 11. Задание С4 1. Смешали 200 г 10%-ного раствора хлорида меди(II) и 200 г 5%-ного раствора сульфида
- 12. mр(KCl) = mр(K2S) + mр(CuCl2) – m(CuS) ω(K2S) mр(K2S) ω(CuCl2) mр(CuCl2) m(CuS) ω(KCl) mр(KCl) mр(KCl) =
- 14. Скачать презентацию








 Merci professeur!
Merci professeur! Обучение персонала. Тема 7
Обучение персонала. Тема 7 Правописание падежных окончаний имен существительных единственного числа
Правописание падежных окончаний имен существительных единственного числа Презентация на тему Рельеф Южной Америки (7 класс)
Презентация на тему Рельеф Южной Америки (7 класс) Популяции
Популяции Частые и популярные вопросы, а также помощь новичку.
Частые и популярные вопросы, а также помощь новичку. Урок рисования
Урок рисования Почему мы часто слышим слово «экология»? (1 класс)
Почему мы часто слышим слово «экология»? (1 класс) Сгибание и разгибание рук в упоре лежа на полу
Сгибание и разгибание рук в упоре лежа на полу Лекція 2 Принципи та методи психологічних досліджень (1)
Лекція 2 Принципи та методи психологічних досліджень (1) 5096c16a06984dc6b0c01fd05158c787
5096c16a06984dc6b0c01fd05158c787 Правила техники безопасности при работе с тканью
Правила техники безопасности при работе с тканью Влияние компьютера на здоровье человека
Влияние компьютера на здоровье человека Первое сентября
Первое сентября Прямые паруса и их бегучий такелаж шлюпа Мирный
Прямые паруса и их бегучий такелаж шлюпа Мирный Плоскостопие
Плоскостопие Правительство Пермского края Об итогах социально-экономического развития Октябрьского муниципального района Пермского края за
Правительство Пермского края Об итогах социально-экономического развития Октябрьского муниципального района Пермского края за  Когда в сердце разгорается любовь
Когда в сердце разгорается любовь Есть или не есть –вот в чем вопрос?
Есть или не есть –вот в чем вопрос? Скарбнiца народнай мудрасцi
Скарбнiца народнай мудрасцi Как образуются кристаллы?
Как образуются кристаллы? ТАТАРО-МОНГОЛЬСКОЕ НАШЕСТВИЕ НА РУСЬ
ТАТАРО-МОНГОЛЬСКОЕ НАШЕСТВИЕ НА РУСЬ  Научные базы данных EBSCO - основной электронный ресурс для академических библиотек
Научные базы данных EBSCO - основной электронный ресурс для академических библиотек Порядок и хаос 5 класс
Порядок и хаос 5 класс Взаимоотношения между организмами
Взаимоотношения между организмами Память и внимание
Память и внимание Биологические системы самоорганизации
Биологические системы самоорганизации Работа: «Дух русского народа крепче всякого оружия»
Работа: «Дух русского народа крепче всякого оружия»