Содержание
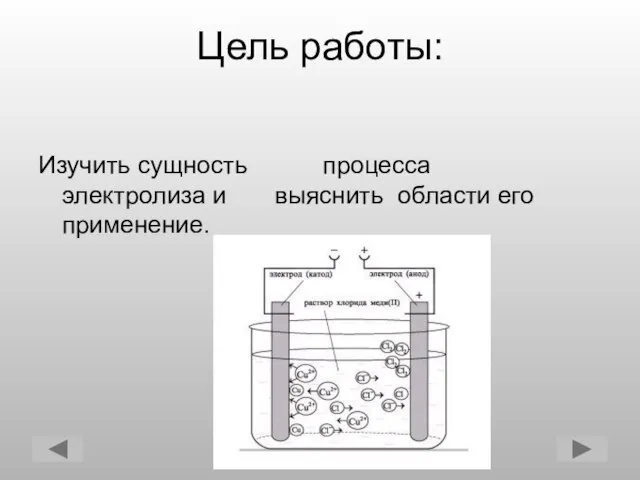
- 2. Цель работы: Изучить сущность процесса электролиза и выяснить области его применение.
- 3. Содержание: Электролиз расплава Электролиз раствора Схема электролиза Сущность электролиза Применение электролиза Выводы Источники информации
- 4. Электролиз расплава Если расплавить поваренную соль, то произойдет расщепление кристаллической решетки на ионы. При этом образуются
- 5. Примеры электролиза расплавов: Электролиз- окислительно-восстановительный процесс, который возникает на электродах при прохождении электрического тока через раствор
- 6. Электролиз раствора В водных растворах процесс приобретает ряд особенностей, так как в нем принимает участие вода.
- 7. Электролиз раствора К аноду направятся анионы CI- и OH-, восстановительные свойства которых также неодинаковы (см. ряд
- 8. Электролиз воды проводится всегда в присутствии инертного электролита (для увеличения электропроводности очень слабого электролита - воды):
- 9. Примеры электролиза растворов солей: на аноде окисляются анионы Сl, а не кислород O молекул воды, так
- 10. Сущность электролиза В результате электролиза на электродах (катоде и аноде) выделяются соответствующие продукты восстановления и окисления,
- 11. Восстановительный процесс на катоде в водных растворах: Катионы металлов со стандартным электродным потенциалом, больше, чем у
- 12. Электрическая энергия Химическая энергия Электролиз Раствор NaCl Катод(-) Анод(+) H20 Расплав NaCl Катод(-) Анод(+) Na+ +
- 13. Преимущества электролиза перед химическим методами получения целевых продуктов заключаются в возможности сравнительно просто (регулируя ток) управлять
- 14. Электрохимическое процессы широко применяют в различных областях современной техники, в аналитической химии, биохимии и т.д. В
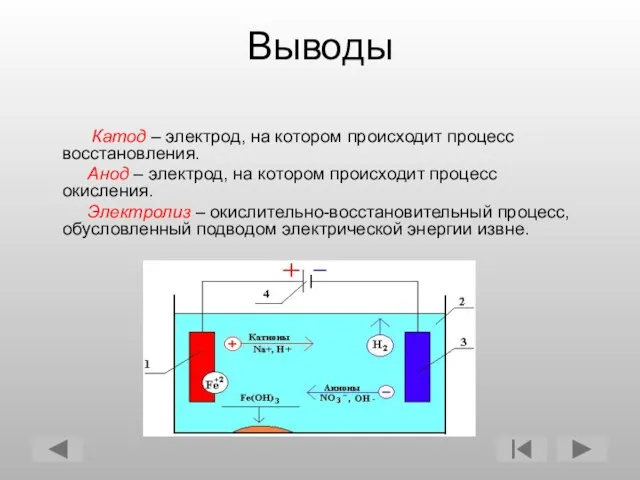
- 15. Выводы Катод – электрод, на котором происходит процесс восстановления. Анод – электрод, на котором происходит процесс
- 17. Скачать презентацию











 Самооценка подростка
Самооценка подростка ОЛЕГ САМОЙЛОВ
ОЛЕГ САМОЙЛОВ Нематериальные активы. Ресурсное обеспечение деятельности хозяйствующего субъекта
Нематериальные активы. Ресурсное обеспечение деятельности хозяйствующего субъекта Чудеса кулинарии
Чудеса кулинарии Тайна личности Шекспира
Тайна личности Шекспира Инновационные и неинновационные препараты: Особенности их продвижения и восприятия целевыми группами
Инновационные и неинновационные препараты: Особенности их продвижения и восприятия целевыми группами Танцуем вместе!
Танцуем вместе! Городское и сельское население
Городское и сельское население Инерция 7 класс
Инерция 7 класс Фотозвіт про проходження виробничої практики на підприємствах Києва
Фотозвіт про проходження виробничої практики на підприємствах Києва Почему мы часто слышим слово «экология»? (1 класс)
Почему мы часто слышим слово «экология»? (1 класс) Основные исходные положения и представления по теории радиоэлектронных систем. (Лекция 1.1)
Основные исходные положения и представления по теории радиоэлектронных систем. (Лекция 1.1) Эти знакомые и незнакомые
Эти знакомые и незнакомые Презентация на тему Сергиев Посад
Презентация на тему Сергиев Посад  Лыжный спорт
Лыжный спорт СТРАТЕГИЯ РАЗВИТИЯ Усть-Лабинского района Краснодарского края до 2022 года
СТРАТЕГИЯ РАЗВИТИЯ Усть-Лабинского района Краснодарского края до 2022 года Олимпийские игры в Древней Греции
Олимпийские игры в Древней Греции Презентация на тему Экологические законы природопользования
Презентация на тему Экологические законы природопользования Маска. История масок
Маска. История масок Запреты, связанные с гражданской службой
Запреты, связанные с гражданской службой Всемирный День Культуры
Всемирный День Культуры Регионы проекта ИСО ШКОЛА Социализация Психологический комфорт ЗдоровьеУспешность.
Регионы проекта ИСО ШКОЛА Социализация Психологический комфорт ЗдоровьеУспешность. Назначение и устройство компьютера
Назначение и устройство компьютера Картины Микеланджело
Картины Микеланджело Произведения Исаака Ильича Левитана
Произведения Исаака Ильича Левитана История стекольной промышленности
История стекольной промышленности Тайм-менеджмент в логистике и ВЭД
Тайм-менеджмент в логистике и ВЭД Тропический и внетропический циклоны
Тропический и внетропический циклоны