Содержание
- 2. Дать понятие об амфотерности, амфотерных оксидах и гидроксидах, переходных металлах; Повторить, закрепить и развить знания о
- 3. Основные классы сложных веществ: Вещества Кислоты Основания Оксиды Соли
- 4. Оксиды – это сложные вещества, состоящие из двух химических элементов, один из которых – кислород со
- 5. Задание 1 Выберите из списка веществ оксиды: H2O, CO2, P2O5, WO3 Fe2O3 SO3, CaCl2, SCl6, CuO,
- 7. Распределите вещества по классам
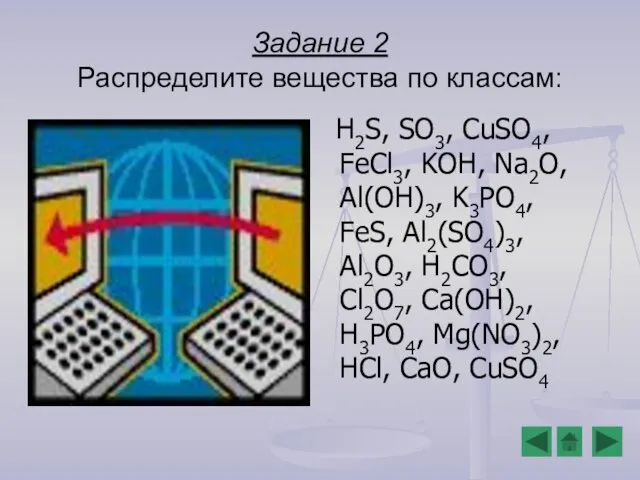
- 8. Задание 2 Распределите вещества по классам: H2S, SO3, CuSO4, FeCl3, KOH, Na2O, Al(OH)3, K3PO4, FeS, Al2(SO4)3,
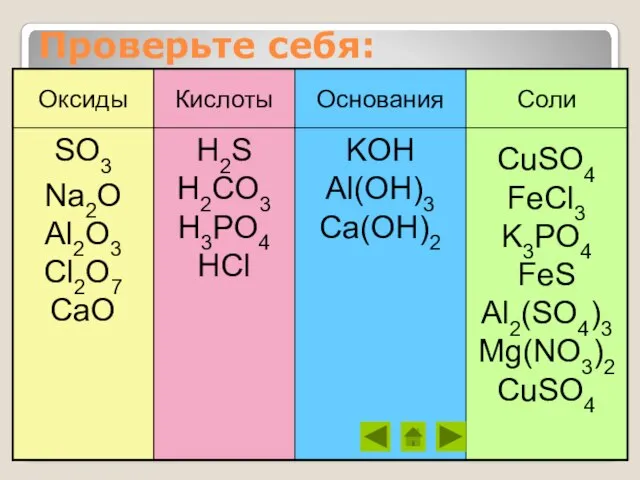
- 9. Проверьте себя:
- 10. Получение гидроксида алюминия В 2 пробирки налейте по 1 мл раствора соли алюминия В обе пробирки
- 11. Доказательство амфотерности: 1.Взаимодействие с кислотами В одну пробирку с осадком прилейте раствор соляной кислоты. 2.Взаимодействие со
- 12. Что наблюдали? Осадки гидроксида алюминия в обеих пробирках растворяются. Вывод: гидроксид алюминия проявляет свойства оснований, взаимодействуя
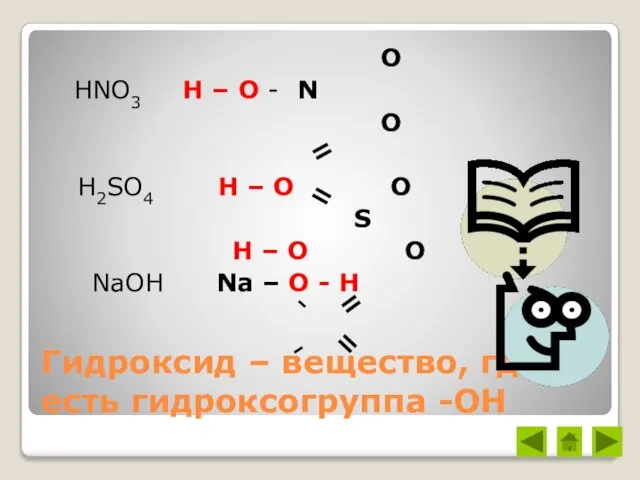
- 13. Гидроксид – вещество, где есть гидроксогруппа -ОН O HNO3 H – O - N O H2SO4
- 14. Гидроксид алюминия можно записать как основание и как кислоту Al(OH)3 = H3AlO3 AlO3H3 = = Кислота
- 15. Al(OH)3 + 3HCl = AlCl3 +3H2O H3AlO3 + 3NaOH = Na3AlO3+3H2O Хлорид алюминия Алюминат натрия Запишите
- 16. Al2O3 + 6HCl = 2AlCl3 + 3H2O Al2O3 + 3NaOH = Na3AlO3 + 3H2O Как основный
- 17. Амфотерные Оксиды металлов (с.о. +2,+3,+4)
- 18. Какие из групп веществ проявляют амфотерные свойства? Ca(ОН)2, Cu(ОН)2, NaОН, Fe(OН)2 Fe2O3, Al2O3, Fe(OН)3 , ZnO,
- 19. Допишите уравнение реакции: Zn(OH)2 + 2NaOH в результате образуются Na2ZnO2 + 2H2O Zn(OH)2 + Na2O ZnSO4
- 21. Скачать презентацию













 Архитектура современных православных храмов
Архитектура современных православных храмов Мораль. Общество. 8 класс
Мораль. Общество. 8 класс Вас приветствует Больше–Ломовисский филиал
Вас приветствует Больше–Ломовисский филиал Разработка корпоративной структуры
Разработка корпоративной структуры Дрожь земли
Дрожь земли Профессия Строитель
Профессия Строитель Клиническое значение и лечение хронических гепатитов В и С у больных ВИЧ-инфекцией Шахгильдян В.И. Федеральный научно-методичес
Клиническое значение и лечение хронических гепатитов В и С у больных ВИЧ-инфекцией Шахгильдян В.И. Федеральный научно-методичес Perfect Continuous tenses in the active voice
Perfect Continuous tenses in the active voice Униформа горничных
Униформа горничных Мини-презентация SEO для тендера по ГК Гранель
Мини-презентация SEO для тендера по ГК Гранель Типичные ошибки стилистики русского языка и методы и способы их преодоления
Типичные ошибки стилистики русского языка и методы и способы их преодоления Возникновение жизни. Развитие жизни. Животные прошлого
Возникновение жизни. Развитие жизни. Животные прошлого Формирование эстетических суждений младших школьников в процессе художественно-практической деятельности
Формирование эстетических суждений младших школьников в процессе художественно-практической деятельности Бизнес_Захматов_05_21_Запомнить
Бизнес_Захматов_05_21_Запомнить Бюджетирование в системе управленческого учета организации: порядок разработки, внедрение, эффективность
Бюджетирование в системе управленческого учета организации: порядок разработки, внедрение, эффективность Доклад Партнерские связи Лешуконского, Мезенского и Пинежского районов как способ развития территории
Доклад Партнерские связи Лешуконского, Мезенского и Пинежского районов как способ развития территории Сравнительно-правовая характеристика таможенных процедур, связанных с ввозом товаров в Евразийский экономический союз
Сравнительно-правовая характеристика таможенных процедур, связанных с ввозом товаров в Евразийский экономический союз Управление объектами инфраструктуры туризма
Управление объектами инфраструктуры туризма Зимние Сурдлимпийские игры 1971
Зимние Сурдлимпийские игры 1971 АВТО-МОБИЛЬНЫЙ ОФИС
АВТО-МОБИЛЬНЫЙ ОФИС Презентация на тему Набеги хана Тохтамыша на Русь
Презентация на тему Набеги хана Тохтамыша на Русь Основные типы реле
Основные типы реле NATURAL RESOURCE MANAGEMENT
NATURAL RESOURCE MANAGEMENT Мой город - моя малая родина
Мой город - моя малая родина Презентация на тему Конституция Российской Федерации
Презентация на тему Конституция Российской Федерации  Иң яҡшы башҡорт класы конкурсына
Иң яҡшы башҡорт класы конкурсына Интерьер жилого дома
Интерьер жилого дома Познавательные процессы человека
Познавательные процессы человека