Содержание
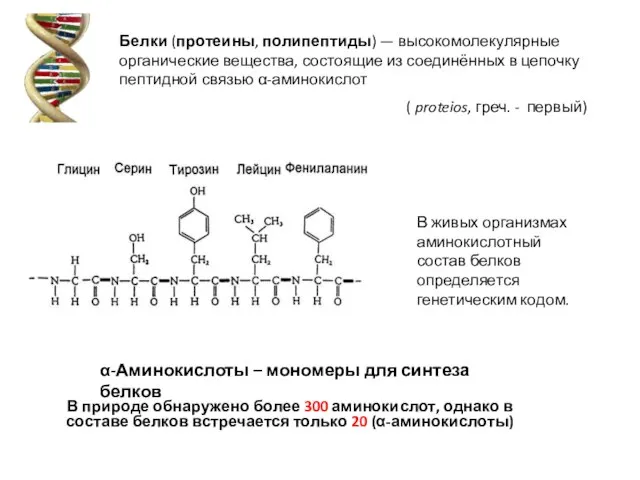
- 2. ( proteios, греч. - первый) Белки (протеины, полипептиды) — высокомолекулярные органические вещества, состоящие из соединённых в
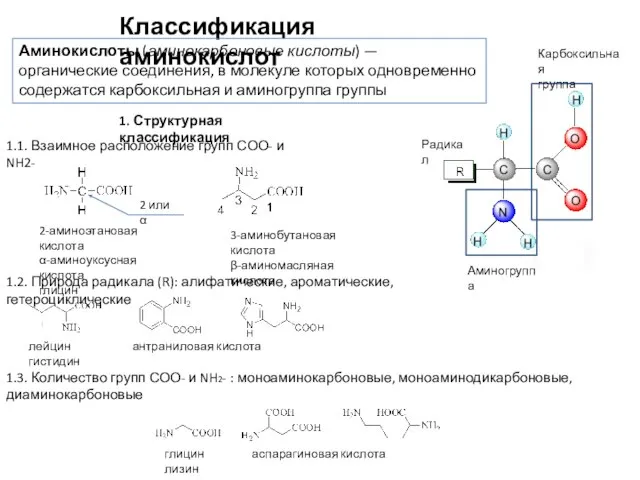
- 3. Классификация аминокислот Карбоксильная группа Радикал Аминогруппа Аминокислоты (аминокарбоновые кислоты) — органические соединения, в молекуле которых одновременно
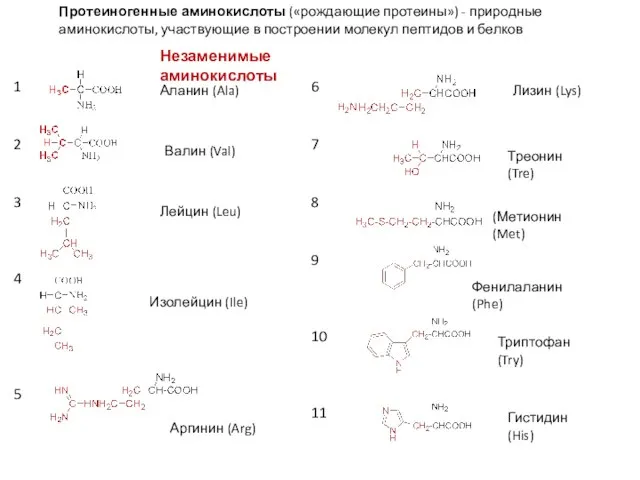
- 4. Протеиногенные аминокислоты («рождающие протеины») - природные аминокислоты, участвующие в построении молекул пептидов и белков Аланин (Ala)
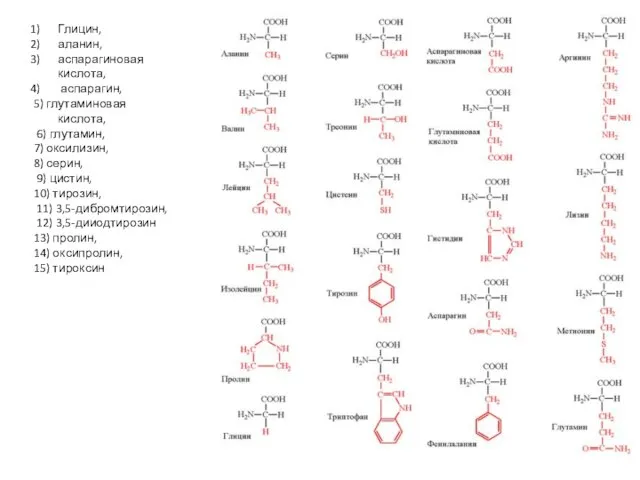
- 5. Глицин, аланин, аспарагиновая кислота, аспарагин, 5) глутаминовая кислота, 6) глутамин, 7) оксилизин, 8) серин, 9) цистин,
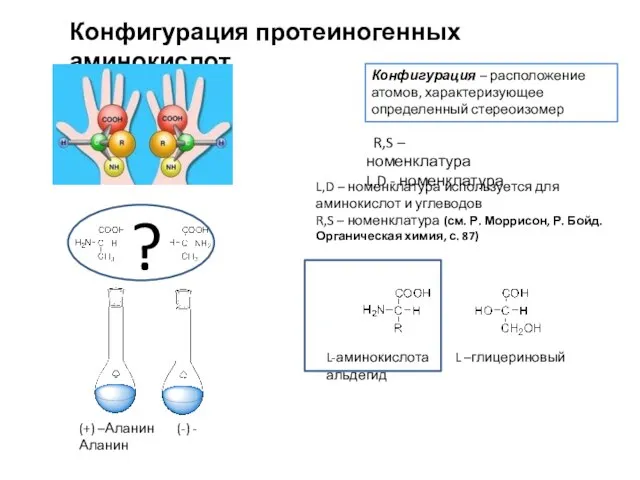
- 6. Конфигурация протеиногенных аминокислот Конфигурация – расположение атомов, характеризующее определенный стереоизомер (+) –Аланин (-) -Аланин ? L-аминокислота
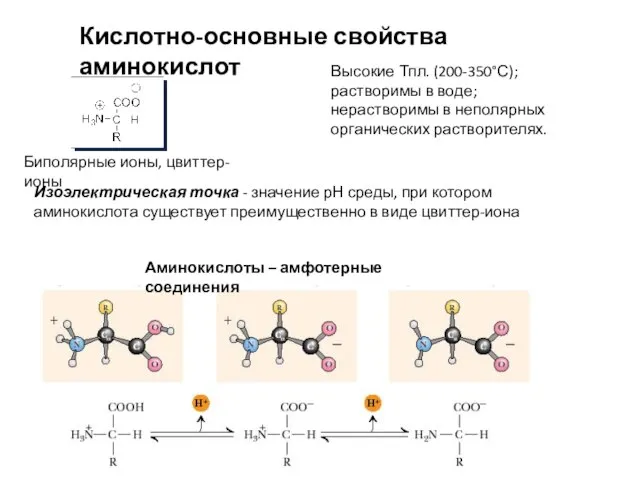
- 7. Кислотно-основные свойства аминокислот Биполярные ионы, цвиттер-ионы Высокие Тпл. (200-350°С); растворимы в воде; нерастворимы в неполярных органических
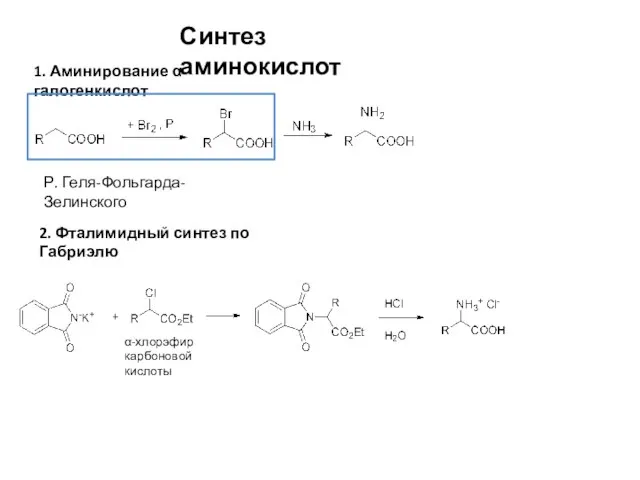
- 8. Синтез аминокислот 1. Аминирование α-галогенкислот Р. Геля-Фольгарда-Зелинского 2. Фталимидный синтез по Габриэлю α-хлорэфир карбоновой кислоты
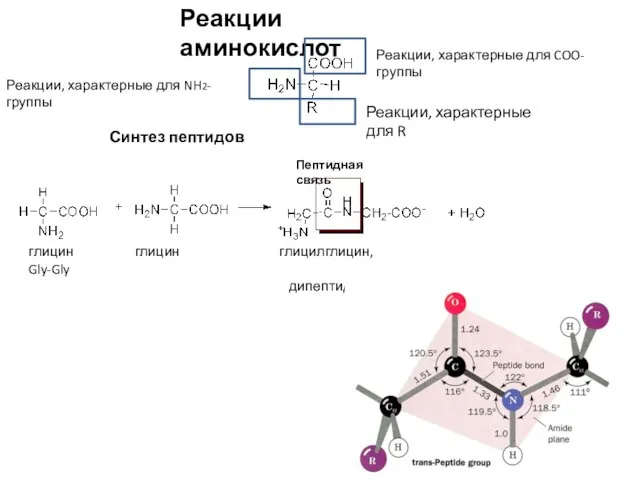
- 9. Реакции аминокислот Реакции, характерные для COO-группы Реакции, характерные для NH2-группы Реакции, характерные для R Синтез пептидов
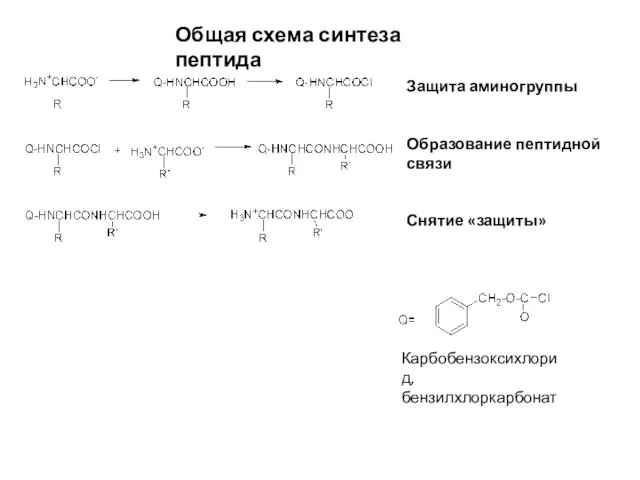
- 10. Общая схема синтеза пептида Защита аминогруппы Образование пептидной связи Снятие «защиты» Карбобензоксихлорид, бензилхлоркарбонат
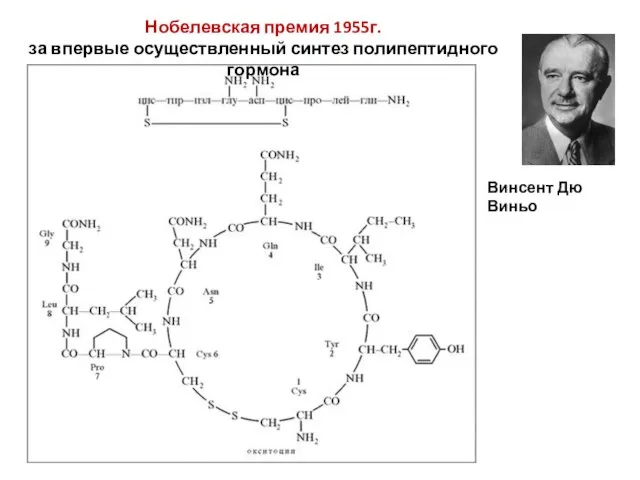
- 11. Нобелевская премия 1955г. за впервые осуществленный синтез полипептидного гормона Винсент Дю Виньо
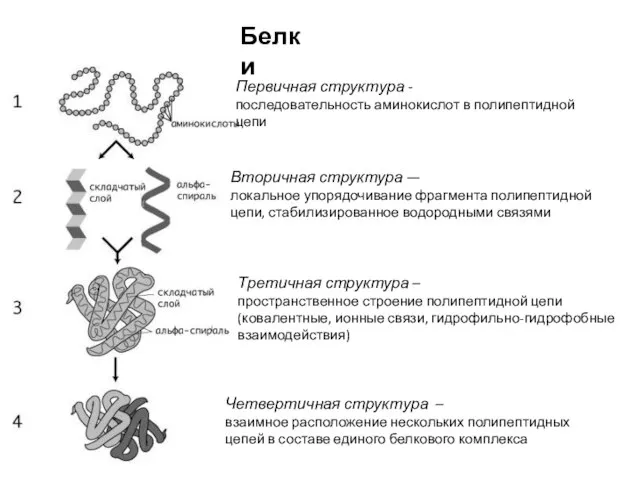
- 12. Белки Первичная структура - последовательность аминокислот в полипептидной цепи Вторичная структура — локальное упорядочивание фрагмента полипептидной
- 14. Скачать презентацию
 Пример схемы для ЕАСД. Схемы размещения моторовагонных депо
Пример схемы для ЕАСД. Схемы размещения моторовагонных депо CTI приложения для офисных АТС Panasonic KX-TD/KX-TDA семейства BLITZ. Описание и функции
CTI приложения для офисных АТС Panasonic KX-TD/KX-TDA семейства BLITZ. Описание и функции Моя любимая группа
Моя любимая группа Поэтический образ Родины
Поэтический образ Родины Исследовательская работа на тему: «В старопольской кухне и за польским столом»
Исследовательская работа на тему: «В старопольской кухне и за польским столом» Презентация на тему Воспитательно-образовательная работа с детьми подготовительной к школе группы
Презентация на тему Воспитательно-образовательная работа с детьми подготовительной к школе группы Физические и
Физические и Что такое JavaScriptЧто такое JavaScriptC# C++ Java Delphi Eiffel Simula D Io Objective-C Object Pascal VB.NET Visual DataFlex Perl PowerBuilder Python. - презентация
Что такое JavaScriptЧто такое JavaScriptC# C++ Java Delphi Eiffel Simula D Io Objective-C Object Pascal VB.NET Visual DataFlex Perl PowerBuilder Python. - презентация 2_5328138068648009249
2_5328138068648009249 Прикладное искусство первой половины ХХ века
Прикладное искусство первой половины ХХ века Счастливы те люди. Кто учит Библию.
Счастливы те люди. Кто учит Библию. Структура активов и пассивов предприятия АПК
Структура активов и пассивов предприятия АПК Колобок
Колобок День народного единства
День народного единства Продвижение в торговых сетях. Активные методы продвижения.
Продвижение в торговых сетях. Активные методы продвижения. Презентация на тему Моя малая Родина (1 класс)
Презентация на тему Моя малая Родина (1 класс) КУРС ИНФОРМАЦИОННАЯ КУЛЬТУРА И/ИЛИ КОМПЬЮТЕР НА УРОКЕ БИОЛОГИИ
КУРС ИНФОРМАЦИОННАЯ КУЛЬТУРА И/ИЛИ КОМПЬЮТЕР НА УРОКЕ БИОЛОГИИ Белорусский костюм (1)
Белорусский костюм (1) Новая Букмекерская контора BINOM
Новая Букмекерская контора BINOM Собачка из кругов
Собачка из кругов Презентация на тему Функциональная схема компьютера
Презентация на тему Функциональная схема компьютера  Пересмотр ГОСТ 32600. Версия ООО НПК Герметика
Пересмотр ГОСТ 32600. Версия ООО НПК Герметика Произведения искусства Микеланджело
Произведения искусства Микеланджело Психология как профессия
Психология как профессия Avez-vous des tomates?
Avez-vous des tomates? Волшебный мир
Волшебный мир Рентгенография черепа
Рентгенография черепа Пробелы в области юридических и иных знаний у сотрудников таможенных органов
Пробелы в области юридических и иных знаний у сотрудников таможенных органов