Содержание
- 2. Вспомните! Какие степени окисления проявляет азот в своих оксидах? Какие окислы азота вы знаете? Расскажите о
- 4. Изучение свойств азотной кислоты, Её значения в хозяйственной деятельности человека.
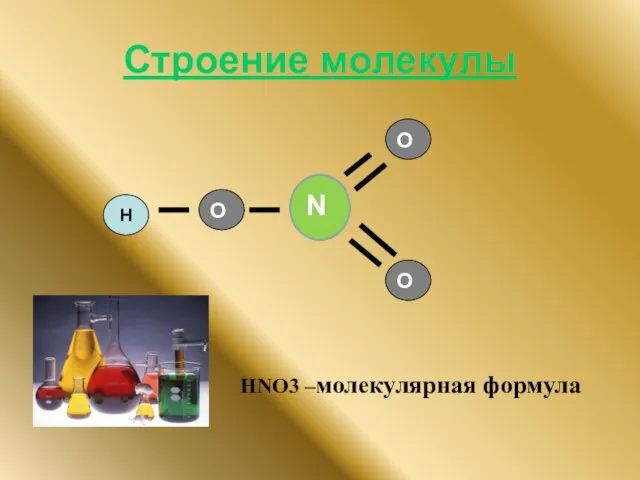
- 5. Строение молекулы Н O O O HNO3 –молекулярная формула N
- 6. Физические свойства азотной кислоты Рассмотрите выданные вам образцы азотной кислоты. Проверьте цвет, прозрачность, растворимость в воде.
- 7. Химические свойства азотной кислоты Очень сильная кислота В водном растворе диссоциирует: НNO3 ↔NO3 + H Взаимодействует:
- 8. Особые свойства Cu +4HNO3 = Cu(NO3)2 +2NO2↑ +2H2O При нагревании выделяется бурый газ, он ядовит для
- 9. Производство азотной кислоты Окисление азота воздуха. Доокисление оксида азота+2 в оксид азота +4 Получение азотной кислоты.
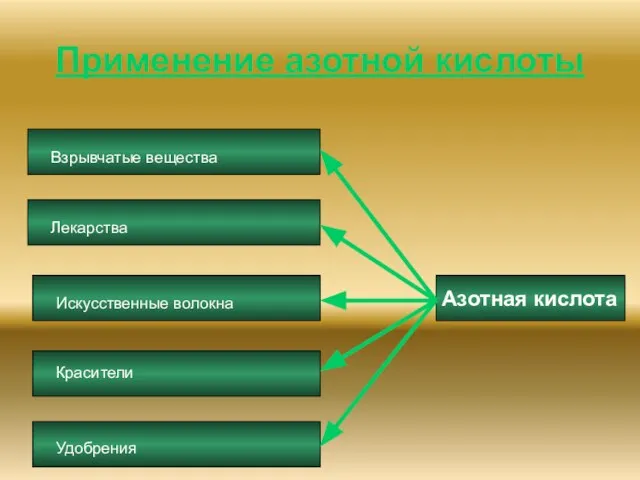
- 10. Применение азотной кислоты Азотная кислота Взрывчатые вещества Лекарства Искусственные волокна Красители Удобрения
- 11. Нитраты NaNO3 KNO3 NH4NO3 Ca(NO3)2 Соли азотной кислоты называются ещё селитрами. Они применяются при производстве спичек,
- 12. Закрепление 2KNO3→2KNO2 +O2 Качественная реакция на нитраты. Решите правильно или неправильно предложенное Вам выссказывание: 1. Азотная
- 13. Закрепление 3. Азотная кислота образует соли – нитриты. 4. Азотная кислота образует соли- нитраты. 5. В
- 14. Закрепление 8. Азотная кислота не реагирует с любыми металлами. 9. Азотная кислота реагирует с оксидами металлов.
- 15. Проверьте свои знания: Правильные ответы: 1,4,5, 9,10,11,12.
- 17. Скачать презентацию












 Колейдоскоп школьной жизни
Колейдоскоп школьной жизни Употребление числительных в речи
Употребление числительных в речи Тайны света и цвета
Тайны света и цвета Общение в условиях конфликта
Общение в условиях конфликта STATE
STATE Металлы 9 класс
Металлы 9 класс Интеллектуальная викторина «Мир животных»
Интеллектуальная викторина «Мир животных» Презентация на тему Быт простых и знатных людей
Презентация на тему Быт простых и знатных людей  Где пропадали вчера днём?
Где пропадали вчера днём? Витамины нужны всем
Витамины нужны всем Земноводные и пресмыкающиеся
Земноводные и пресмыкающиеся Культура Московской Руси
Культура Московской Руси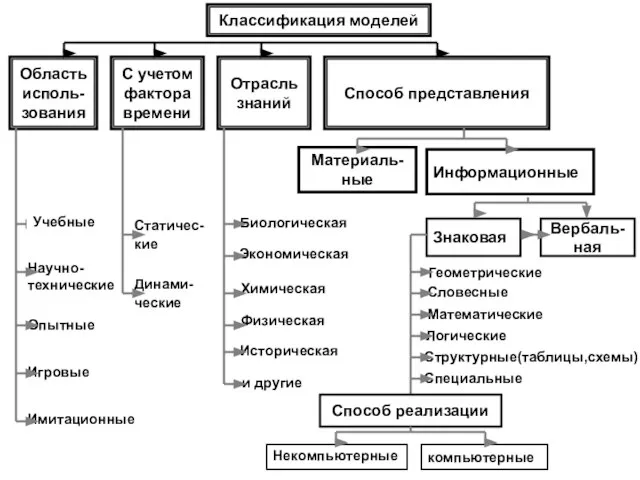 Классификация моделей
Классификация моделей ПоленовВасилий Дмитриевич(1 июня 1844 года – 18 июля 1927 года)
ПоленовВасилий Дмитриевич(1 июня 1844 года – 18 июля 1927 года) Христианская семья
Христианская семья Оформление документации по итогам ежемесячного пересчета
Оформление документации по итогам ежемесячного пересчета Формирование системы трудового воспитания в условиях школы – интерната
Формирование системы трудового воспитания в условиях школы – интерната Лидерские компетенции в построении успешной карьеры
Лидерские компетенции в построении успешной карьеры Поверхности. Классификация, образование, задание на чертеже. Лекция 4
Поверхности. Классификация, образование, задание на чертеже. Лекция 4 Ребенок и его права
Ребенок и его права Инновация в организации оптовой торговли. ФРУТЭП для ритейлеров Урал и Сибирь
Инновация в организации оптовой торговли. ФРУТЭП для ритейлеров Урал и Сибирь Н.Н.Носов «Приключения Незнайки»
Н.Н.Носов «Приключения Незнайки» Центр олимпийского резерва г. Жлобина
Центр олимпийского резерва г. Жлобина Презентация на тему ЖИВОПИСЬ И МИФЫ
Презентация на тему ЖИВОПИСЬ И МИФЫ  Формальные и неформальные организации
Формальные и неформальные организации Презентация на тему "Мудрый старик" татарская сказка
Презентация на тему "Мудрый старик" татарская сказка TaxoPhone 12.0. Обучение сервисного департамента
TaxoPhone 12.0. Обучение сервисного департамента Целеполагание и рефлексия как элементы технологии эвристического обучения
Целеполагание и рефлексия как элементы технологии эвристического обучения