Содержание
- 2. БРОМ (лат. Bromum), Br - химический элемент VII группы периодической системы Менделеева, относится к галогенам, атомный
- 3. Исходным сырьём для получения брома служат морская вода, озёрные и подземные рассолы и щелока калийного происхождения,
- 4. Бром ядовит. Поэтому, работая с ним, нужно быть осторожным. Предельно допустимая концентрация паров брома в воздухе
- 5. Физические и химические свойства брома При -7,2°С жидкий бром застывает, превращаясь в красно-коричневые игольчатые кристаллы со
- 6. Бром - постоянная составная часть тканей животных и растений. Наземные растения содержат в среднем 7*10-4% брома
- 7. В земле бром присутствует главным образом в виде ионов, которые путешествуют вместе с грунтовыми водами. Часть
- 8. Бром и серебро сопутствуют друг другу не только в минералах. Не будет преувеличением сказать, что бромистое
- 10. Скачать презентацию
Слайд 2БРОМ (лат. Bromum), Br - химический элемент VII группы периодической системы Менделеева,
БРОМ (лат. Bromum), Br - химический элемент VII группы периодической системы Менделеева,

БРОМ
Слайд 3Исходным сырьём для получения брома служат морская вода, озёрные и подземные рассолы
Исходным сырьём для получения брома служат морская вода, озёрные и подземные рассолы

ПОЛУЧЕНИЕ
БРОМА
Слайд 4Бром ядовит. Поэтому, работая с ним, нужно быть осторожным. Предельно допустимая концентрация
Бром ядовит. Поэтому, работая с ним, нужно быть осторожным. Предельно допустимая концентрация

техника безопасности
Слайд 5Физические и химические свойства брома
При -7,2°С жидкий бром застывает, превращаясь в
Физические и химические свойства брома
При -7,2°С жидкий бром застывает, превращаясь в
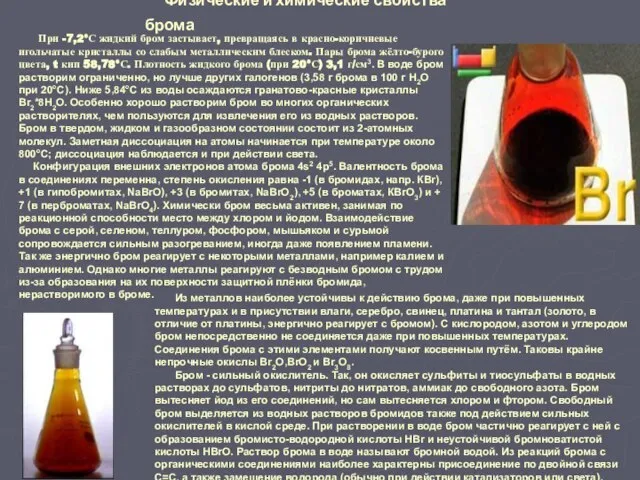
Из металлов наиболее устойчивы к действию брома, даже при повышенных температурах и в присутствии влаги, серебро, свинец, платина и тантал (золото, в отличие от платины, энергично реагирует с бромом). С кислородом, азотом и углеродом бром непосредственно не соединяется даже при повышенных температурах. Соединения брома с этими элементами получают косвенным путём. Таковы крайне непрочные окислы Br2O,BrO2 и Вr3О8.
Бром - сильный окислитель. Так, он окисляет сульфиты и тиосульфаты в водных растворах до сульфатов, нитриты до нитратов, аммиак до свободного азота. Бром вытесняет йод из его соединений, но сам вытесняется хлором и фтором. Свободный бром выделяется из водных растворов бромидов также под действием сильных окислителей в кислой среде. При растворении в воде бром частично реагирует с ней с образованием бромисто-водородной кислоты НВr и неустойчивой бромноватистой кислоты НВrО. Раствор брома в воде называют бромной водой. Из реакций брома с органическими соединениями наиболее характерны присоединение по двойной связи С=С, а также замещение водорода (обычно при действии катализаторов или света).
Слайд 6
Бром - постоянная составная часть тканей животных и растений. Наземные растения содержат
Бром - постоянная составная часть тканей животных и растений. Наземные растения содержат

бром в организме
Слайд 7
В земле бром присутствует главным образом в виде ионов, которые путешествуют вместе
В земле бром присутствует главным образом в виде ионов, которые путешествуют вместе

Довольно много брома в съедобных грибах. В боровиках, подберезовиках, подосиновиках – примерно 1,4·10–3% элемента №35. Есть он и в воде соленых озер, и в подземных «водохранилищах», сопутствующих месторождениям горючих ископаемых, а также калийных солей и каменной соли.
Есть бром и в атмосфере. Подсчитано, что ежегодно вместе с морской водой в воздух переходит около 4 млн. т брома, причем содержание этого элемента в воздухе приморских районов всегда больше, чем в районах с резко континентальным климатом.
Море – главный поставщик брома. Довольно много брома в организмах рыб. Он всегда присутствует и в организмах земных животных, не исключая человека. Потребность в броме у разных органов и систем разная. В человеческом организме этот элемент обнаружен в крови, почках, печени и больше всего в мозге.
бром всюду
Слайд 8
Бром и серебро сопутствуют друг другу не только в минералах. Не будет
Бром и серебро сопутствуют друг другу не только в минералах. Не будет

Бромистый натрий добавляют в дубильные растворы, благодаря чему кожа становится тверже.
Из прозрачных кристаллов бромистого калия делают линзы, великолепно пропускающие инфракрасные лучи. Бактерицидные свойства бромистого калия помогают дольше сохранять овощи и фрукты.
Много «профессий» у бромистого лития. Он предотвращает коррозию в холодильных установках, обезвоживает минеральные масла, помогает кондиционировать воздух.
Текстильщики широко применяют органический краситель броминдиго, с помощью которого получают целую гамму ярких и чистых тонов – от синего до красного. Другое бром органическое соединение – бром хлорметан – отличный огнетушитель, который к тому же не проводит электричества и потому особенно эффективен, когда нужно, например, потушить загоревшуюся проводку. Бром органикой пропитывают древесину, чтобы придать ей большую стойкость к атмосферным воздействиям, грибкам, плесени.
Для получения большинства этих полезных соединений, прежде всего органических, нужен ядовитый, зловонный, агрессивный, крайне неприятный в общении, но тем не менее незаменимый бром.
применение брома
 Вкусное и красивое лакомство для неожиданных гостей
Вкусное и красивое лакомство для неожиданных гостей Состав международной ассоциации горных гидов (IFMGA*)
Состав международной ассоциации горных гидов (IFMGA*) Презентация крудо
Презентация крудо Изготовление лестницы из деталей конструктора
Изготовление лестницы из деталей конструктора Жлектронное декларирование 1
Жлектронное декларирование 1 Дневник Психеи.Любовь в жизни и творчестве М.Цветаевой
Дневник Психеи.Любовь в жизни и творчестве М.Цветаевой Химические свойства кислот
Химические свойства кислот Юношеский возраст. Лекция 8.2
Юношеский возраст. Лекция 8.2 A.С. Пушкин "Метель"
A.С. Пушкин "Метель" SAS սուպերմարկետի մատուցած ծառայությունները
SAS սուպերմարկետի մատուցած ծառայությունները Устная и письменная нумерация чисел в пределах 1000
Устная и письменная нумерация чисел в пределах 1000 Виды компьютерных сетей. Телекоммуникации
Виды компьютерных сетей. Телекоммуникации “Умом Россию не понять...”
“Умом Россию не понять...” Инновационный процесс: понятие, модели
Инновационный процесс: понятие, модели Lektsia_3
Lektsia_3 Презентация на тему Эхо афганской войны
Презентация на тему Эхо афганской войны знакомство с городом
знакомство с городом Электрическая цепь
Электрическая цепь Предмет буенча өлгереш һәм белем сыйфаты
Предмет буенча өлгереш һәм белем сыйфаты РДУ-99. Его значение и применение
РДУ-99. Его значение и применение Презентация на тему Экскурсионная работа в преподавании Мировой Художественной культуры
Презентация на тему Экскурсионная работа в преподавании Мировой Художественной культуры Синус, косинус, тангенс суммы и разности аргументов
Синус, косинус, тангенс суммы и разности аргументов Устав образовательного учреждения и его основные разделы
Устав образовательного учреждения и его основные разделы Женщины Маяковского
Женщины Маяковского Комментарий проблемы
Комментарий проблемы Туризм - отличный отдых
Туризм - отличный отдых Основы православной культуры. Монастырь
Основы православной культуры. Монастырь Табличный процессор Excel 2007
Табличный процессор Excel 2007