Содержание
- 2. Типы исследований (клинических) Фаза исследований I Фокус на безопасность, нежели на эффективность Исследования по подбору дозы,
- 3. Темы, которые мы уже затронули в первой сессии Контрольная группа Рандомизация Маскирование Параллельные / перекрестные исследования
- 4. Темы, которые затронем сегодня Зачем нам нужна контрольная группа? Для чего нужна рандомизация? Протокол Определение конечных
- 5. Зачем нам нужна контрольная группа Ранние клинические разработки были обычно так хороши, что контроль не всегда
- 6. Зачем нам нужна контрольная группа Сильвермен, 1985 – Эпидемия ретрорентальной фиброплазии у детей Неконтролируемые исследования говорили,
- 7. Зачем нам нужна контрольная группа Неконтролируемые исследования могут дать искаженный взгляд на новую терапию Пациентам со
- 8. Какая контрольная группа? – польза исторического и не рандомизированного контроля Контроль менее вероятно имеет четко определенные
- 9. Какая контрольная группа? – польза исторического и не рандомизированного контроля Качество записываемых данных может быть невысоким
- 10. Что такое рандомизация? Распределение пациентов по группам лечения производится методом случайного отбора Рандомизированные исследования имеют более
- 11. Почему необходимо рандомизировать исследования Нерандомизированные исследования могут быть очень предвзятыми Если в рамках исследования между группами
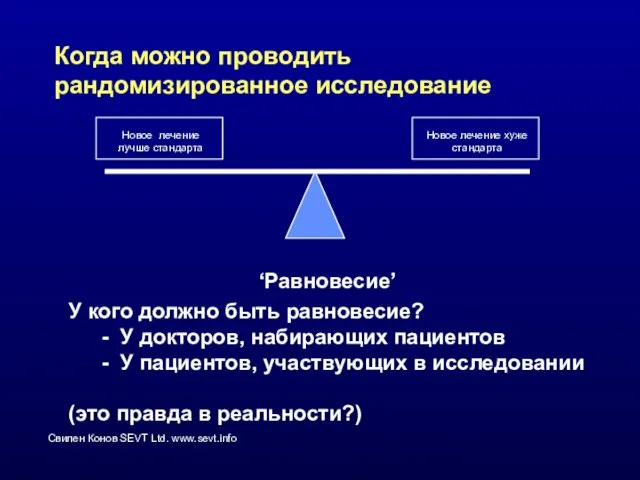
- 12. Когда можно проводить рандомизированное исследование Новое лечение лучше стандарта Новое лечение хуже стандарта ‘Равновесие’ У кого
- 13. Другие выгоды рандомизации Помогает с маскированием исследования (позже увидите) Предотвращает сознательную или несознательную предвзятость в выборе,
- 14. Отбор пациентов для исследования Обсудите исследование с пациентом и оцените его пригодность Получите информированное согласие Формально
- 15. Другие выгоды рандомизации (продолжение) Пример: Исследование антикоагулянтной терапии (Райт 1948) Пациенты по нечетным дням – антикоагулянты
- 16. Протокол Обоснование, цели и задачи Дизайн исследования Отбор пациентов – критерии включения/исключения Графики лечения Мониторинг Регистрация,
- 17. Отбор пациентов для участия в исследовании Исследования должны иметь четкие критерии включения и исключения – ясные
- 18. Оценка ответа – первичная конечная точка В любом исследовании нам необходимо определить (желательно) единственную первичную конечную
- 19. Оценка конечных точек – вторичные конечные точки В дополнение к первичным конечным точкам, мы можем также
- 20. Определение конечных точек – пример Замещение абакавира для нуклеозидных аналогов у пациентов с липоатрофией ВИЧ. Карр
- 21. Определение конечной точки В большинстве исследований пациенты часто проходят мониторинг (например, каждые 4 недели после рандомизации)
- 22. Определение конечных точек – пример Замещение абакавира для нуклеозидных аналогов у пациентов с липоатрофией ВИЧ. Карр
- 23. Клинические/суррогатные конечные точки Мы обычно более заинтересованы в эффекте нового лечения относительно клинического результата (например, новые
- 24. Суррогатные конечные точки “Лабораторные измерения или физические признаки, используемые для замещения клинически значимой конечной точки, которая
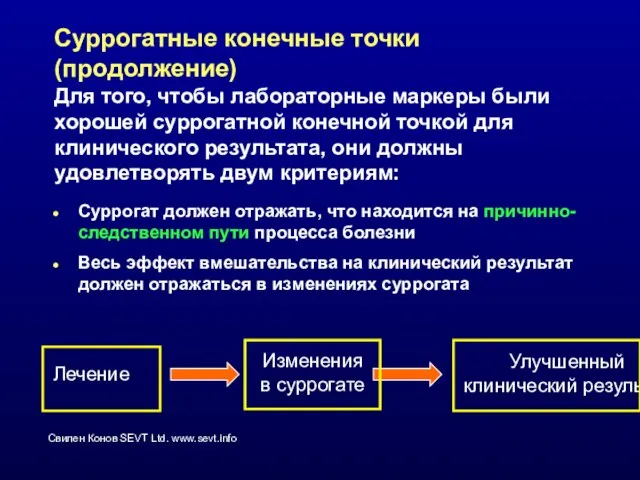
- 25. Суррогатные конечные точки (продолжение) Для того, чтобы лабораторные маркеры были хорошей суррогатной конечной точкой для клинического
- 26. Суррогатные конечные точки (продолжение) Количество CD4 до начала ВААРТ было установлено, как надежная суррогатная конечная точка
- 27. Определение конечных точек – пример Замещение абакавира для нуклеозидных аналогов у пациентов с липоатрофией ВИЧ. Карр
- 28. ‘Нарушение протоколов ’ Пациенты, не отвечающие критериям – могут быть набраны по ошибке Не приверженные –
- 29. Анализ по пациентам, прошедшим рандомизацию (ППР) Все пациенты, рандомизированные на лечение, должны быть включены в анализ
- 30. Анализ по пациентам, прошедшим рандомизацию (ППР) Обеспечивает измерение эффекта лечения в реальной жизни Единственная непредвзятая оценка
- 31. Анализ на лечении Включает только тех пациентов, которые завершили полный курс лечения, к которому были рандомизированы
- 32. Анализ на лечении Предполагается, что показывает оптимальный эффект лечения, когда применяется именно так, как назначено Однако,
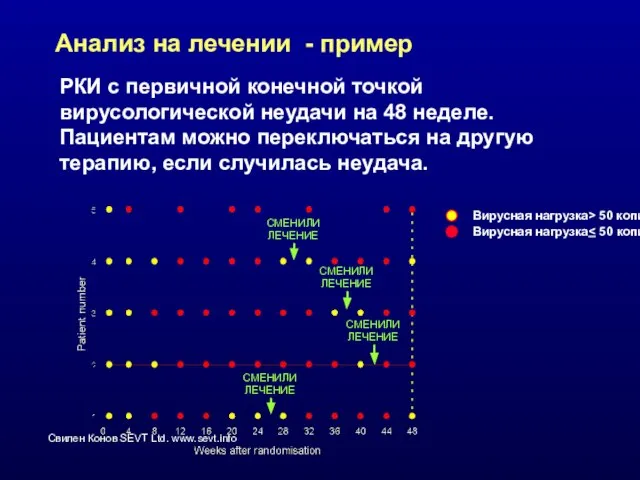
- 33. Анализ на лечении - пример РКИ с первичной конечной точкой вирусологической неудачи на 48 неделе. Пациентам
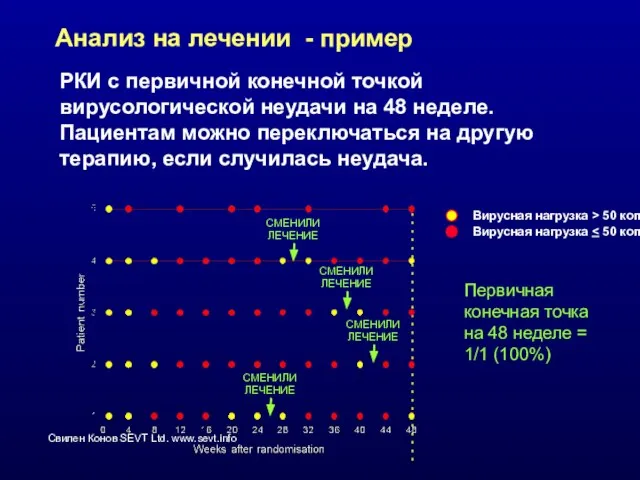
- 34. Анализ на лечении - пример РКИ с первичной конечной точкой вирусологической неудачи на 48 неделе. Пациентам
- 35. Анализ на лечении Остающиеся на рандомизированном лечении на 48 неделе будут, по определению, теми, кто не
- 36. Проблемы анализа по ППР с суррогатными конечными точками Если пациенты не доступны для сопровождения или выпадают
- 37. Альтернативные методы анализов на выборке ППР (пациенты, прошедшие рандомизацию) ППР, Данные отсутствуют (О) = Неудача (Н)
- 38. Альтернативные методы анализов на выборке ППР (пациенты, прошедшие рандомизацию) Перенос данных последнего наблюдения ППР (ПДПН, или
- 39. Альтернативные методы анализов на выборке ППР (пациенты, прошедшие рандомизацию) ППР, Данные отсутствуют (О) = Исключены Все
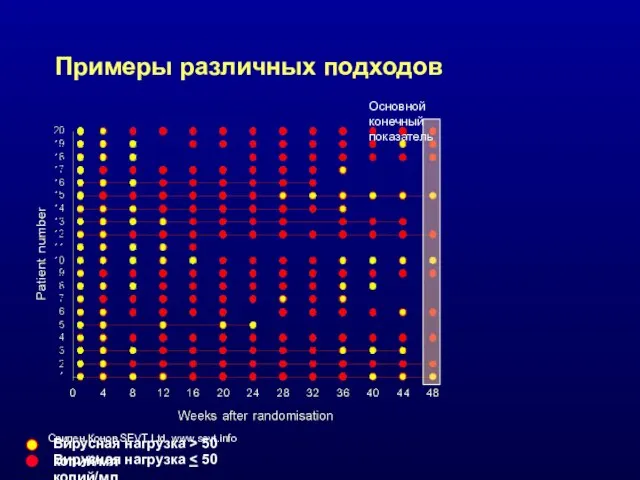
- 40. Примеры различных подходов Основной конечный показатель Вирусная нагрузка > 50 копий/мл Вирусная нагрузка
- 41. Примеры различных подходов Основной конечный показатель Вирусная нагрузка > 50 копий/мл Вирусная нагрузка Респондер: На лечении/
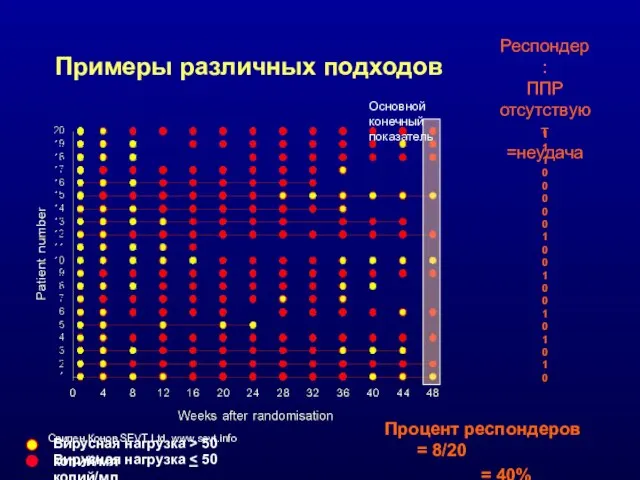
- 42. Примеры различных подходов Основной конечный показатель Вирусная нагрузка > 50 копий/мл Вирусная нагрузка Респондер: ППР отсутствуют
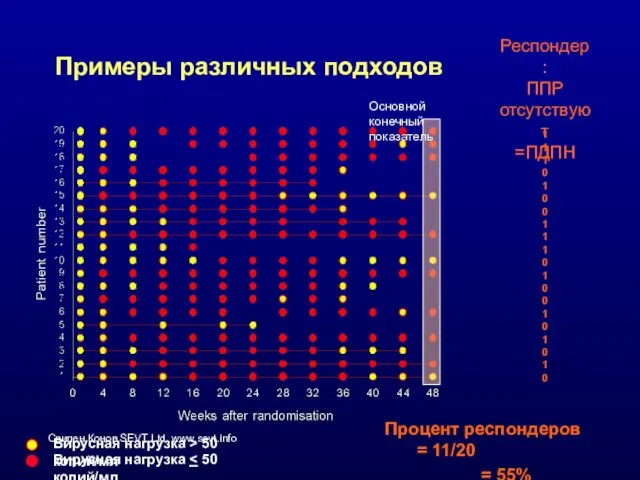
- 43. Примеры различных подходов Основной конечный показатель Вирусная нагрузка > 50 копий/мл Вирусная нагрузка Респондер: ППР отсутствуют
- 44. Примеры различных подходов - заключение Подход Процент респондеров На лечении/ППР отсутствуют = исключены 73% ППР отсутствуют
- 45. Анализы подгрупп Зачастую исследователи стремятся провести анализ эффекта схемы терапии в анализируемых подгруппах Например, можно проанализировать
- 46. Анализы подгрупп Существует ряд нюансов, которые нужно учитывать при выполнении большого количества анализов подгрупп. В частности,
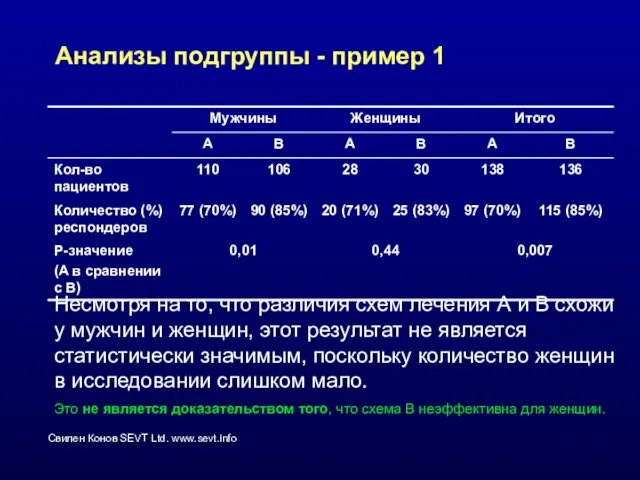
- 47. Анализы подгруппы - пример 1 Несмотря на то, что различия схем лечения А и В схожи
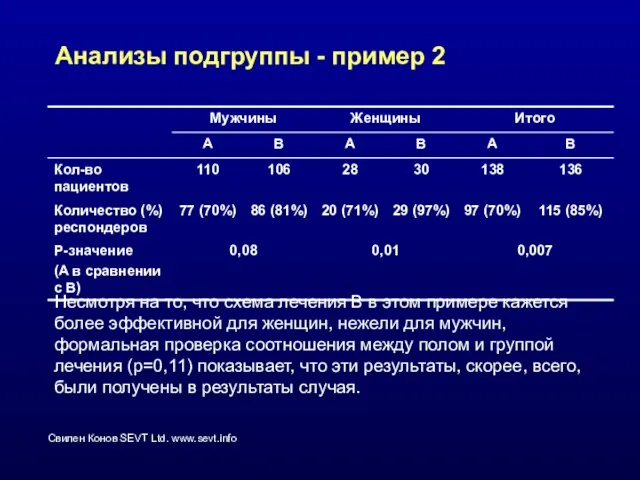
- 48. Анализы подгруппы - пример 2 Несмотря на то, что схема лечения В в этом примере кажется
- 49. Анализы подгрупп Если исследователи полагают, что проведение анализов подгрупп является важным для исследования, то необходимо априори
- 50. Промежуточные анализы В любом исследовании может возникнуть ситуация, когда одна схема лечения оказывается существенно хуже, чем
- 51. Промежуточные анализы Тем не менее, всегда существует вероятность того, что первоначальные результаты будут получены случайно, особенно
- 52. Промежуточные анализы – роль Комиссии по безопасности данных и мониторингу При необходимости можно собрать Комиссию по
- 53. Промежуточные анализы (продолжение) Если результаты промежуточных анализов показывают превосходство одного их исследуемых объектов, однако Комиссия не
- 54. Промежуточные анализы (продолжение) Если требуется опубликовать данные промежуточных анализов, важно либо сохранить исследование «слепым», либо не
- 55. Испытания на превосходство В стандартном исследовании мы обычно проводим испытания на предмет сравнения гипотезы о том,
- 56. Испытание на эквивалентность Иногда нам просто нужно установить, что два препарата являются эквивалентными Это нужно обычно
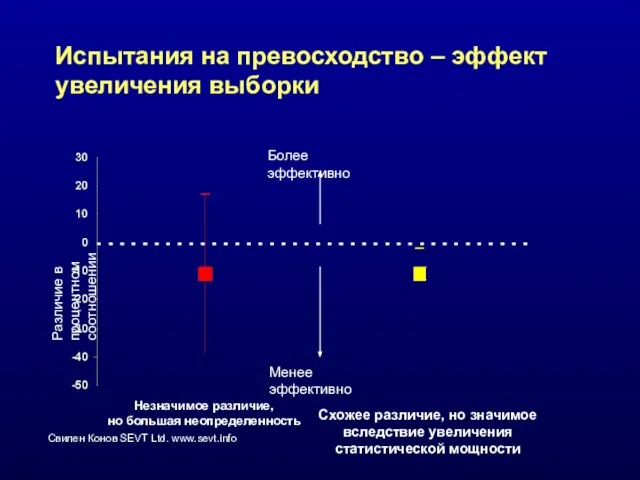
- 57. Испытания на превосходство – эффект увеличения выборки Различие в процентном соотношении Незначимое различие, но большая неопределенность
- 58. Испытание на эквивалентность (продолжение) При выполнении испытаний на эквивалентность мы в большей степени фокусируемся на интервалах
- 59. Пример - различие в процентном соотношении не определяется через 24 недели с интервалом доверия (схема А
- 60. Испытания на эквивалентность (продолжение) Необходимость установить максимальный диапазон, в пределах которого два лечения могут отличаться при
- 61. Испытания на отсутствие превосходства По сути схожи с испытаниями на эквивалентность Новый препарат может быть немного
- 62. Пример - различие в процентном соотношении не определяется через 24 недели с интервалом доверия (схема лечения
- 64. Скачать презентацию



















































 МИХАЛЕВ А.С. старший преподаватель кафедры Физики им. В.А. Фабриканта Московского энергетического института
МИХАЛЕВ А.С. старший преподаватель кафедры Физики им. В.А. Фабриканта Московского энергетического института Тундра (4 класс)
Тундра (4 класс) Портфель заместителя директора по информатизации ОУ
Портфель заместителя директора по информатизации ОУ Gоршки от Vовочки. Проект
Gоршки от Vовочки. Проект Кто какую пользу приносит
Кто какую пользу приносит Человек иинформация
Человек иинформация Будем знакомы:Воспитатель 1-ой квалификационной категории Маргарян Ирина Александровна
Будем знакомы:Воспитатель 1-ой квалификационной категории Маргарян Ирина Александровна Пейзаж родной земли. Урок №1
Пейзаж родной земли. Урок №1 РАСПРЕДЕЛЕНИЕ ЖИЗНИ В БИОСФЕРЕ И ОПРЕДЕЛЯЮЩИЕ ФАКТОРЫ
РАСПРЕДЕЛЕНИЕ ЖИЗНИ В БИОСФЕРЕ И ОПРЕДЕЛЯЮЩИЕ ФАКТОРЫ Презентация на тему Устройства компьютера
Презентация на тему Устройства компьютера  Детский лагерь Юность
Детский лагерь Юность ИКТ на уроках английского языка
ИКТ на уроках английского языка Презентация на тему Тест по математике 2 класс
Презентация на тему Тест по математике 2 класс  Основные ошибки рекламодателей в интернете.
Основные ошибки рекламодателей в интернете. ПЕРСПЕКТИВЫ РАЗВИТИЯ НЕФТЕГАЗОПЕРЕРАБАТЫВАЮЩЕЙ И ГАЗОХИМИЧЕСКОЙ ПРОМЫШЛЕННОСТИРЕСПУБЛИКИ САХА (ЯКУТИЯ)
ПЕРСПЕКТИВЫ РАЗВИТИЯ НЕФТЕГАЗОПЕРЕРАБАТЫВАЮЩЕЙ И ГАЗОХИМИЧЕСКОЙ ПРОМЫШЛЕННОСТИРЕСПУБЛИКИ САХА (ЯКУТИЯ) WSEI. Навчання у Польщі
WSEI. Навчання у Польщі Страховая компания с 2021 г
Страховая компания с 2021 г Диагностика острого аппендицита при различных локализациях червеобразного отростка
Диагностика острого аппендицита при различных локализациях червеобразного отростка Автоматизация соноров в словах сложной звукослоговой структуры слова
Автоматизация соноров в словах сложной звукослоговой структуры слова Методы логистического анализа машиностроительной продукции
Методы логистического анализа машиностроительной продукции Внутренние воды северной Америки 7 класс
Внутренние воды северной Америки 7 класс Типы персональных компьютеров
Типы персональных компьютеров Презентация на тему Производство чугуна и стали
Презентация на тему Производство чугуна и стали  Ужель та самая Татьяна?
Ужель та самая Татьяна? Издательство DELTA PUBLISHING
Издательство DELTA PUBLISHING Қисық11А
Қисық11А Методические рекомендации по организации самостоятельных занятий спортом
Методические рекомендации по организации самостоятельных занятий спортом Щеглов Андрей Серафимович. Менеджер по продажам
Щеглов Андрей Серафимович. Менеджер по продажам