Содержание
- 2. Электролитическая диссоциация – это процесс распада электролитов на ионы при их растворении в воде или расплавлении.
- 3. Слабый электролит – это вещество, частично диссоциирующее на ионы и плохо проводящее электрический ток. Сильный электролит
- 4. Реакция ионного обмена – это реакция между элетролитами в растворе. Катион – это положительно заряженный ион.
- 5. Разделите данные вещества на сильные и слабые электролиты: Al(OH)3 MgCl2 H2SO3 CO Ca HNO3 BaSO4 Ca(OH)2
- 6. Закончите молекулярные уравнения, составьте ионные: Zn(NO3)2 + HCl = NaOH + CaO = K2CO3 + H2SO4
- 7. Определите тип гидролиза солей, среду раствора: FeCl2 Ba(NO3)2 K2S
- 8. По сокращённым ионным уравнениям составьте полные ионные и молекулярные: Cu2+ + S2- = CuS H+ +
- 10. Скачать презентацию






 “ИНОВАТИВНА МРЕЖА ЗА РАЗВИТИЕНА СОЦИАЛНИ ПРЕДПРИЯТИЯ”
“ИНОВАТИВНА МРЕЖА ЗА РАЗВИТИЕНА СОЦИАЛНИ ПРЕДПРИЯТИЯ”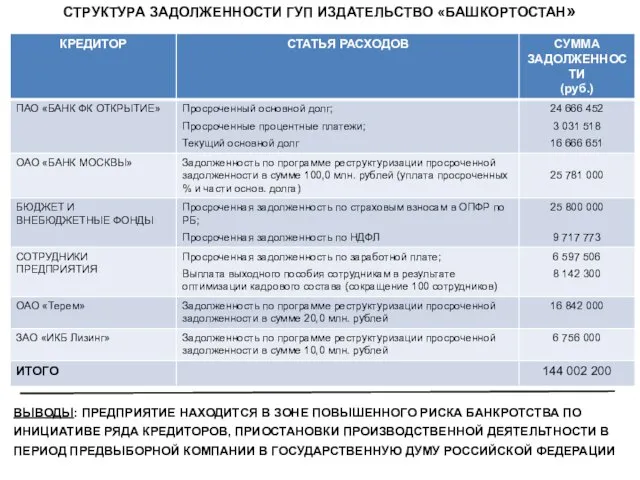 Проект реструктуризации задолженности ГУП Издательство Башкортостан
Проект реструктуризации задолженности ГУП Издательство Башкортостан Предупреждение заболеваний сердца и сосудов
Предупреждение заболеваний сердца и сосудов Где и как появились первые игрушки?
Где и как появились первые игрушки? Итоги работы секции языкознания: было представлено 5 работ.
Итоги работы секции языкознания: было представлено 5 работ. Внутренняя энергия
Внутренняя энергия Понятие и источники предпринимательского права
Понятие и источники предпринимательского права Управление контейнерным терминалом (CMS)
Управление контейнерным терминалом (CMS) Тема проповеди: Секрет 10 конвертов, или Как правильно планировать семейный бюджет
Тема проповеди: Секрет 10 конвертов, или Как правильно планировать семейный бюджет Здоровое питание. Правила
Здоровое питание. Правила Программы и файлы. Рабочий стол
Программы и файлы. Рабочий стол Олимпийские игры
Олимпийские игры Перспективные направления и формы работы с педагогами и обучающимися ММЦ ИТ Балаковского района
Перспективные направления и формы работы с педагогами и обучающимися ММЦ ИТ Балаковского района Оплодотворение и развитие организма
Оплодотворение и развитие организма Оздоровительные технологии в МОУ СОШ № 90 «Крепыш»
Оздоровительные технологии в МОУ СОШ № 90 «Крепыш» Евгений Родионов
Евгений Родионов Книжная полка:учебники и учебные пособия для преподавания русского языка как второго родного
Книжная полка:учебники и учебные пособия для преподавания русского языка как второго родного Новогодние традиции Южной Кореи
Новогодние традиции Южной Кореи Исследование функции на монотонность
Исследование функции на монотонность А.С. Пушкин и Костромской край
А.С. Пушкин и Костромской край Некрасов «Дедушка Мазай и зайцы»
Некрасов «Дедушка Мазай и зайцы» История Заглядинской средней школы
История Заглядинской средней школы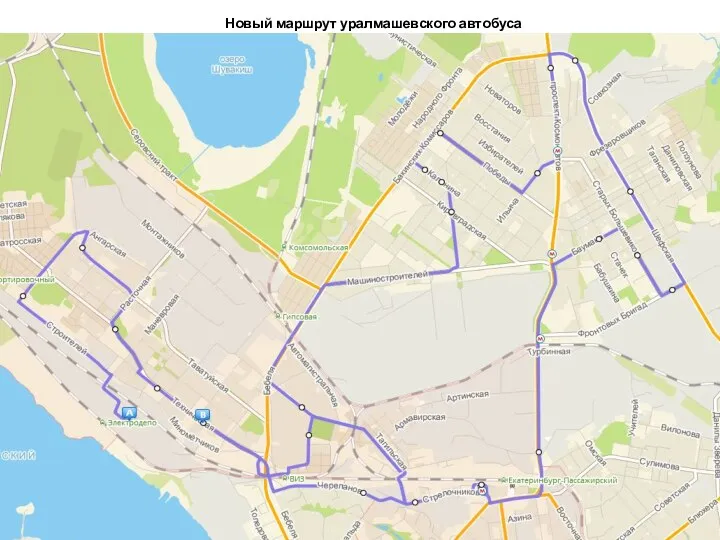 Новый маршрут уралмашевского автобуса
Новый маршрут уралмашевского автобуса Неповторний Киев. Фотоальбом
Неповторний Киев. Фотоальбом Растровые светильники
Растровые светильники Составление связного высказывания с использованием предложений определенной структуры, в том числе на лингвистическую тему
Составление связного высказывания с использованием предложений определенной структуры, в том числе на лингвистическую тему Отделение лесного хозяйства ВГМХА
Отделение лесного хозяйства ВГМХА Использование информационных технологий в обучении истории и обществознания
Использование информационных технологий в обучении истории и обществознания