Слайд 2Описание:
Коррозия металлов (от латинского corrodere - грызть) -процессы, происходящие в результате химического воздействия

окружающей среды, в результате которых происходит их разрушение.
электрохимическая коррозия - поверхностное разрушение в среде электролита с возникновением в системе электрического тока. Электрохимическая коррозия - разрушение в атмосфере, на почве, водоёмах, грунтах.
Слайд 3Электрохимическая коррозия
Примером электрохимической коррозии является, например, разрушение деталей машин, приборов и различных

металлических конструкций в почвенных, грунтовых, речных и морских водах, в атмосфере, под пленками влаги, в технических растворах, под действием смазочно-охлаждающих жидкостей и т.д.
Слайд 4электрохимическая коррозия протекает на поверхности металлов под действием электрических токов, то есть происходят окислительно-восстановительные

химические реакции-, характеризующиеся отдачей электронов и их переносом, так как образуются катодные и анодные участки.
Слайд 5Образованию катодов и анодов способствуют химическая неоднородность металлов (примеси и включения), наличие

участков остаточной деформации, неоднородность покрывающих металл защитных плёнок и т.д. Наиболее часто в образовании данного вида разрушения металла участвуют не один фактор, а несколько. Когда метал начинает корродировать, он превращается в многоэлектронный гальванический элемент.
Слайд 6Потенциал.
В отличии химического, электрохимические процессы контролируются (зависят) не только от концентрации реагирующих

веществ, но и, главным образом, зависят от потенциала поверхности металла. На границе раздела двух разнородных фаз происходит переход заряженных частиц - ионов или электронов из одной фазы в другую, следовательно, возникает разность электрических потенциалов, распределения упорядоченных электрических зарядов, т.е. образование двойного электрического слоя.
Слайд 7Методы борьбы:
Противостоять коррозии непросто. С точки зрения химии, это процесс окисления, в

котором принимает участие электрон. Не имеет значения, превратится ли при этом металл в оксид, карбонат, гидроксид или сульфид. Важно, что он отдает свои электроны, окисляется. Очень часто электроны достаются кислороду воздуха, а продуктом коррозии является оксид. Если в коррозии участвует еще и атмосферная влага, может образоваться и гидроксид. Так кислород воздуха совместно с влагой разъедают железо, при этом образуется ржавчина
Металлы высокой степени чистоты не подвергаются электрохимической коррозии.
Слайд 8Самый простой способ защиты от коррозии - это изолировать металл от окружающей

среды. Достаточно поместить металлическую деталь в инертную атмосферу или изолировать в вакууме - и все. Она сохранится.







 «Обзор законодательства Республики Казахстан в сфере социальной поддержки и обеспечения социальными услугами»
«Обзор законодательства Республики Казахстан в сфере социальной поддержки и обеспечения социальными услугами» Роспись петуха по мотивам Филимоновской росписи
Роспись петуха по мотивам Филимоновской росписи Гражданское право. Понятие и виды сроков в гражданском праве
Гражданское право. Понятие и виды сроков в гражданском праве Модернизм
Модернизм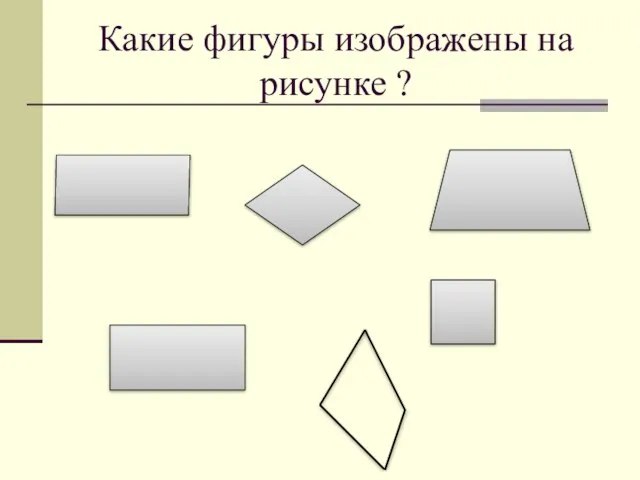 Какие фигуры изображены на рисунке ?
Какие фигуры изображены на рисунке ? Перенос слова переносятся по слогам
Перенос слова переносятся по слогам Принтеры
Принтеры Методическая разработка «Создание презентаций» Элективный курс для 10 класса.
Методическая разработка «Создание презентаций» Элективный курс для 10 класса. Вейк-лебедка - летний бизнес. Вейкпарк в пляжной зоне
Вейк-лебедка - летний бизнес. Вейкпарк в пляжной зоне Федеральное Собрание РФ
Федеральное Собрание РФ Инжиниринг нефтехимии и нефтегазопереработки
Инжиниринг нефтехимии и нефтегазопереработки Китайский клуб МИИТа
Китайский клуб МИИТа Мой город, с тебя начинается Родина (город Сатка)
Мой город, с тебя начинается Родина (город Сатка) Спартакиада пенсионеров муниципального образования Город Гатчина
Спартакиада пенсионеров муниципального образования Город Гатчина Эры. Основные события органического мира
Эры. Основные события органического мира Презентация на тему Операционные системы на мобильных устройствах
Презентация на тему Операционные системы на мобильных устройствах  Живопись
Живопись Михайленко Юлия Борисовна учитель начальных классов ГБОУ гимназии № 1518 г. Москвы
Михайленко Юлия Борисовна учитель начальных классов ГБОУ гимназии № 1518 г. Москвы Муниципальное общеобразовательное учреждение лингвистическая гимназия № 70
Муниципальное общеобразовательное учреждение лингвистическая гимназия № 70 МОСКВА- ГОРОД ГЕРОЙ . Битва за Москву(30 сентября 1941- 20 апреля 1942)
МОСКВА- ГОРОД ГЕРОЙ . Битва за Москву(30 сентября 1941- 20 апреля 1942) Векторы в пространстве и не только
Векторы в пространстве и не только Презентация на тему История развития отечественной вычислительной техники
Презентация на тему История развития отечественной вычислительной техники Трансформация изображения через трансформацию формы - серия открыток
Трансформация изображения через трансформацию формы - серия открыток ОРНАМЕНТЫ в национальном костюме
ОРНАМЕНТЫ в национальном костюме Цветник для солнечного места “Степной бриз ”
Цветник для солнечного места “Степной бриз ” Презентация на тему Тургенев. Стихи в прозе
Презентация на тему Тургенев. Стихи в прозе 287 Воскресшему служу я
287 Воскресшему служу я Берлину заменить Северный поток-2 другим проектом
Берлину заменить Северный поток-2 другим проектом