Содержание
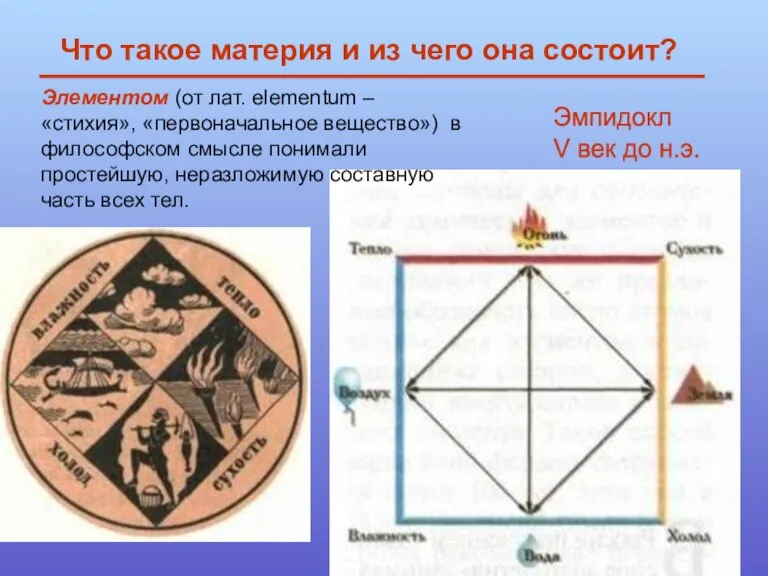
- 2. Элементом (от лат. еlementum – «стихия», «первоначальное вещество») в философском смысле понимали простейшую, неразложимую составную часть
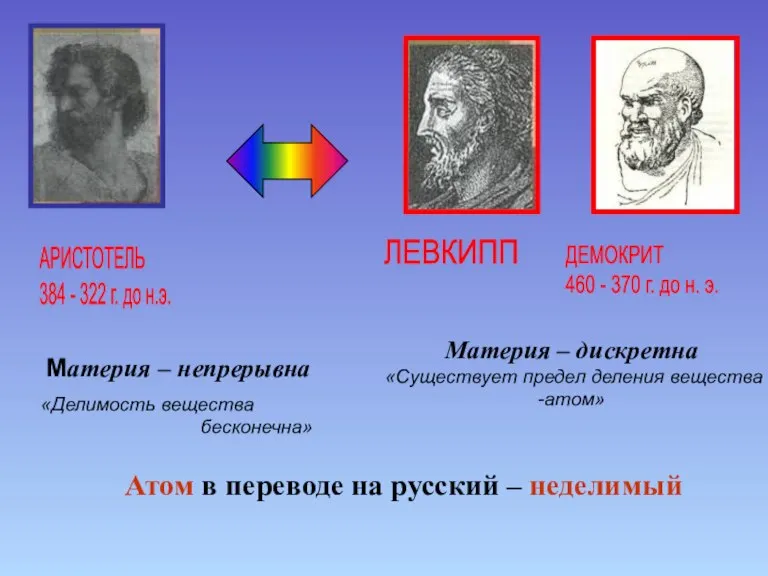
- 3. Материя – дискретна «Существует предел деления вещества -атом» АРИСТОТЕЛЬ 384 - 322 г. до н.э. ЛЕВКИПП
- 4. Учение Демокрита все тела состоят из бесчисленного количества сверхмалых, невидимых глазом, неделимых частиц-атомов; атомы непрерывно двигаются
- 5. Платон Элементы мира – правильные многогранники: тетраэдр - «частица огня», октаэдр - «частица воздуха», икосаэдр -
- 6. В середине XVII в. французский философ и физик Пьер Гассенди (1592—1655) заново пересказал учение Демокрита и
- 7. После 10 лет эксперимента Р. Бойль написал знаменитую книгу «Химик-скептик», в которой доказал нереальность «начал» Аристотеля
- 8. XVIII век Михаил Васильевич Ломоносов 1711-1765 «Химик без знания физики, — писал он,-- подобен человеку, который
- 9. Антуан Лоран Лавуазье 1743-1794 XVIII век А. Лавуазье описал и систематизировал все известные в то время
- 10. Джон Дальтон 1766-1844 XIX век 1810 Новая эпоха начинается в химии с атомистики (следовательно, не Лавуазье,
- 11. Жозеф Луи Гей-Люссак XIX век 1808 В 1808 г. французский исследователь Жозеф Луи Гей-Люссак сообщил об
- 12. Амедео Авогадро 1776-1856 На основе закона простых объемных отношений Авогадро выдвинул гипотезу: 1. Атомы одного и
- 13. В 1860 году состоялся I Международный конгресс химиков. Участники конгресса: - четко разграничили понятия атома и
- 14. Основываясь на том, что атомная масса водорода почти в точности равна единице и что атомные массы
- 15. 1829 Иоганн Вольфгант Доберейнер Первая попытка научной классификации химических элементов принадлежит немецкому химику Иоганну Вольфгангу Доберейнеру,
- 16. Систематизация химических элементов
- 17. Систематизация химических элементов
- 18. Систематизация химических элементов
- 19. Систематизация химических элементов В 1871 г. ученый разработал новый вариант периодической системы, который уже мало чем
- 20. Логическим завершением поисков различных вариантов научной систематики химических элементов явилась периодическая система Дмитрия Ивановича Менделеева, составленная
- 21. Периодическая таблица химических элементов, созданная на основе периодического закона, открытого русским ученым ДИ Менделеевым стала научным
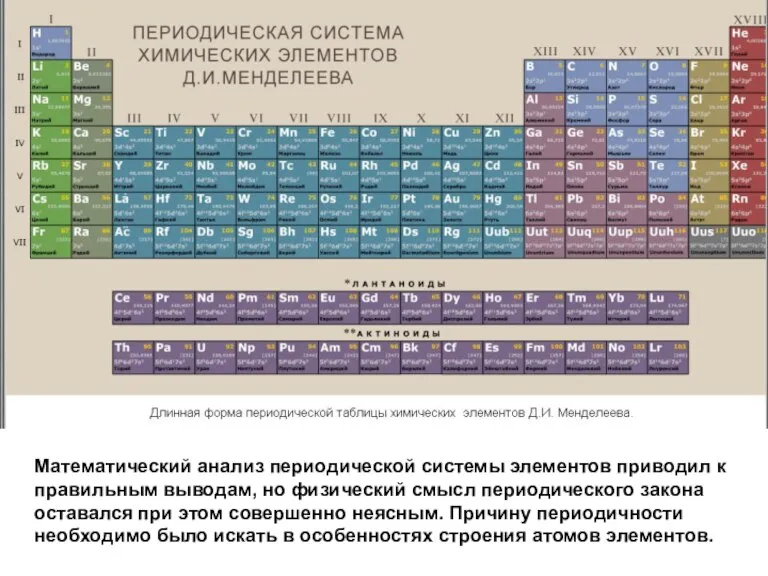
- 22. Математический анализ периодической системы элементов приводил к правильным выводам, но физический смысл периодического закона оставался при
- 23. В 1885 г. шведский исследователь Иоганн Роберт Ридберг подвел математический фундамент под периодический закон: 1) У=
- 24. Ярым противником атомно-молекулярного учения в конце XIX в. выступил известный немецкий естествоиспытатель Вильгельм Оствальд. Он утверждал,
- 26. Скачать презентацию




















 Презентация ожидаемых результатов стажировки в_____________
Презентация ожидаемых результатов стажировки в_____________ Написание наречий
Написание наречий Конструирование шкатулки
Конструирование шкатулки Я - Бизнесмен
Я - Бизнесмен Возможности человеческой памяти
Возможности человеческой памяти Феномен портфолио
Феномен портфолио Предпринимательская деятельность
Предпринимательская деятельность Лекция 3
Лекция 3 Презентация на тему Понимание в семье – ключевой фактор мотивации ребенка к учебе, делу, общению
Презентация на тему Понимание в семье – ключевой фактор мотивации ребенка к учебе, делу, общению  Психологические критерии успешности учителя
Психологические критерии успешности учителя Коммерческие условия Hoff
Коммерческие условия Hoff Великая французская революция 1789-1799 гг
Великая французская революция 1789-1799 гг Comet. Абразивный инструмент на бакелитовой связке
Comet. Абразивный инструмент на бакелитовой связке Лихтенштейн
Лихтенштейн Презентация на тему Народы и древние государства на территории России
Презентация на тему Народы и древние государства на территории России Презентация Беларусь
Презентация Беларусь Законы экологии Коммонера
Законы экологии Коммонера Те́хника
Те́хника Моральный долг (4 класс)
Моральный долг (4 класс) ВПК России
ВПК России Разрезы (вырезы) на аксонометрических изображениях деталей
Разрезы (вырезы) на аксонометрических изображениях деталей Зачем охранять природу?
Зачем охранять природу? Presentation Title
Presentation Title  Влияние индийского искусства на Шри-Ланку
Влияние индийского искусства на Шри-Ланку Процесс автоматизации управления учебно-воспитательной работой
Процесс автоматизации управления учебно-воспитательной работой Изменение имён прилагательных по родам (3 класс)
Изменение имён прилагательных по родам (3 класс) Наука в современном обществе
Наука в современном обществе А у нас сегодня супервизия!
А у нас сегодня супервизия!