Слайд 2Ферменты – это белковые молекулы, которые синтезируются живыми клетками. В каждой клетке

насчитывается более сотни различных ферментов. Роль ферментов в клетке колоссальна. С их помощью химические реакции идут с высокой скоростью, при температуре, подходящей для данного организма.
Слайд 3То есть ферменты – это биологические катализаторы, которые облегчают протекание химической реакции
и за счет этого увеличивают её скорость. Как катализаторы они не изменяют направление реакции и не расходуются в процессе реакции.
Ферменты-биокатализаторы – вещества, увеличивающие скорость химических реакций.
Слайд 4Все ферменты – глобулярные белки с третичной или четвертичной структурой. Ферменты могут
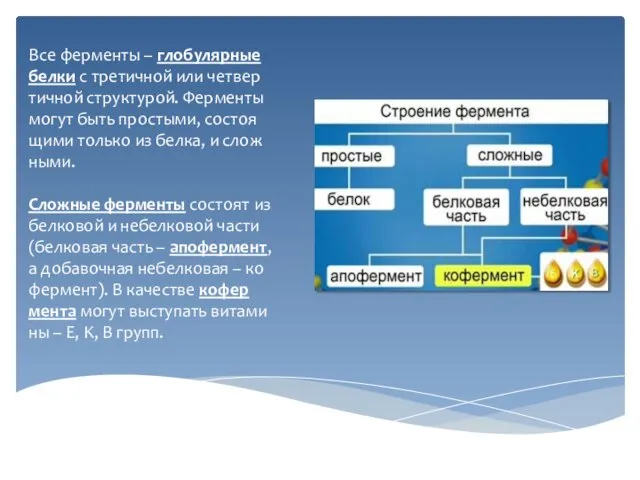
быть простыми, состоящими только из белка, и сложными.
Сложные ферменты состоят из белковой и небелковой части (белковая часть – апофермент, а добавочная небелковая – кофермент). В качестве кофермента могут выступать витамины – E, K, B групп.
Слайд 5Механизм действия ферментов
Фермент взаимодействует с субстратом и образует короткоживущий фермент-субстратный комплекс. По

завершении реакции, фермент-субстратный комплекс распадается на продукты и фермент. Фермент в итоге не изменяется: по окончании реакции он остается таким же, каким был до неё, и может теперь взаимодействовать с новой молекулой субстрата.
Слайд 6На рисунке представлен механизм работы фермента, в частности, образования пептидной связи между
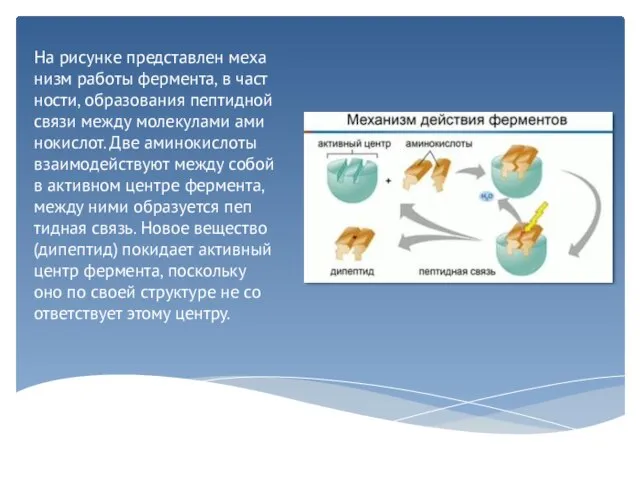
молекулами аминокислот. Две аминокислоты взаимодействуют между собой в активном центре фермента, между ними образуется пептидная связь. Новое вещество (дипептид) покидает активный центр фермента, поскольку оно по своей структуре не соответствует этому центру.
Слайд 7Особенностью ферментов является то, что они обладают высокой специфичностью, т. е. могут

ускорять только одну реакцию или реакции одного типа.
В 1890 году Э. Г. Фишер предположил, что эта специфичность обусловлена особой формой молекулы фермента, которая точно соответствует форме молекулы субстрата. Эта гипотеза получила название «ключа и замка», где ключ сравнивается с субстратом, а замок – с ферментом. Гипотеза гласит: субстрат подходит к ферменту, как ключ подходит к замку. Избирательность действия фермента связана со строением его активного центра.
Слайд 8Активность ферментов
В первую очередь, на активность фермента влияет температура. С повышением температуры

скорость химической реакции возрастает. Увеличивается скорость молекул, у них появляется больше шансов столкнуться друг с другом. Следовательно, увеличивается вероятность того, что реакция между ними произойдет. Температура, обеспечивающая наибольшую активность фермента – оптимальная.
Слайд 9За пределами оптимальной температуры скорость реакции снижается вследствие денатурации белков. Когда температура
снижается, скорость химической реакции тоже падает. В тот момент, когда температура достигает точки замерзания, фермент инактивируется, но при этом не денатурирует.
Слайд 10Кроме этого, активность ферментов зависит ещё от pH среды (кислотности – то

есть показателя концентрации ионов водорода).
В большинстве случаев, ферменты работают при нейтральном pH, т. е. при pH около 7. Но существуют ферменты, которые работают либо в кислой и сильнокислой, либо в щелочной и сильнощелочной среде.
Слайд 11Классификация ферментов
В 1961 году была предложена систематическая классификация ферментов на 6 групп.

Но названия ферментов оказались очень длинными и трудными в произношении, поэтому ферменты принято сейчас именовать с помощью рабочих названий.
Слайд 12Рабочее название состоит из названия субстрата, на который действует фермент, и окончания

«аза». Например, если вещество — лактоза, то есть молочный сахар, то лактаза – это фермент который его преобразует. Если сахароза (обыкновенный сахар), то фермент, который его расщепляет, – сахараза. Соответственно, ферменты, которые расщепляют протеины, носят название протеиназы.
Слайд 13Значение ферментов
Ферменты применяются практически во всех областях человеческой деятельности, и такое широкое
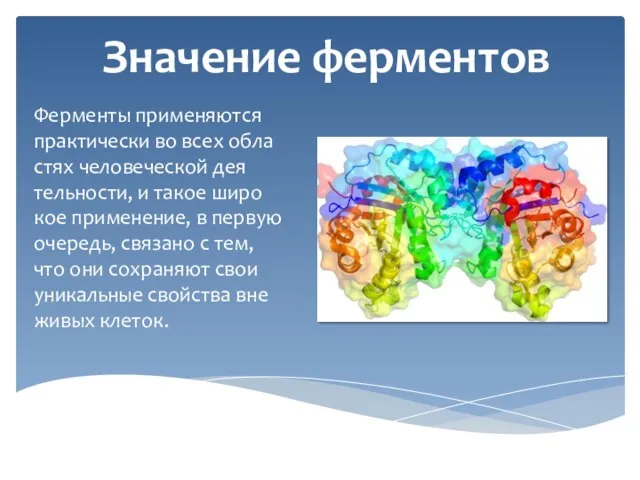
применение, в первую очередь, связано с тем, что они сохраняют свои уникальные свойства вне живых клеток.
Слайд 14Ферменты групп амилаз, протеаз и липаз применяются в медицине. Они расщепляют крахмал,

белки и жиры. Все эти ферменты, как правило, входят в состав комбинированных препаратов, таких как фестал и панзинорм, и используются, в первую очередь, для лечения заболеваний желудочно-кишечного тракта.
Слайд 15Ферменты применяют для растворения тромбов в кровеносных сосудах, при лечении гнойных ран.
Особое

место занимает энзимотерапия при лечении онкологических заболеваний.
Такие ферменты как амилаза расщепляют крахмал и поэтому широко используются в пищевой промышленности. В пищевой промышленности используется протеиназа, расщепляющая белки, и липазы, расщепляющие жиры. Ферменты амилазы используются в хлебопечении, виноделии и пивоварении.














 Породы кошек
Породы кошек Уборка квартир. Стоимость услуг
Уборка квартир. Стоимость услуг Рентгеновские лучи
Рентгеновские лучи Партнерская карта здоровья для розничных клиентов лаборатории KDL
Партнерская карта здоровья для розничных клиентов лаборатории KDL МОДЕЛИРОВАНИЕ ВЗАИМОДЕЙСТВИЯ БЕЛКОВ С МАЛЫМИ МОЛЕКУЛАМИ – РАЗРАБОТКА ЭФФЕКТИВНОГО ИЕТОДА СЛЕПОГО ДОКИНГА Ю.Н. ВОРОБЬЕВ Institute Chemic
МОДЕЛИРОВАНИЕ ВЗАИМОДЕЙСТВИЯ БЕЛКОВ С МАЛЫМИ МОЛЕКУЛАМИ – РАЗРАБОТКА ЭФФЕКТИВНОГО ИЕТОДА СЛЕПОГО ДОКИНГА Ю.Н. ВОРОБЬЕВ Institute Chemic Презентация на тему Алгоритмы сжатия. Алгоритм построения орграфа Хаффмана
Презентация на тему Алгоритмы сжатия. Алгоритм построения орграфа Хаффмана Опиливание деталей. Регулировочная мастерская
Опиливание деталей. Регулировочная мастерская Занятия йогой для детей 3-7 лет
Занятия йогой для детей 3-7 лет Модельная проблемно-ценностная дискуссия старшеклассников «Участие молодежи в жизни города»
Модельная проблемно-ценностная дискуссия старшеклассников «Участие молодежи в жизни города» Презентация на тему История становления французского языка
Презентация на тему История становления французского языка  Риск-менеджмент
Риск-менеджмент Система подготовки интерактивных графических схем«Seamatica-SE»
Система подготовки интерактивных графических схем«Seamatica-SE» Prezentatsia
Prezentatsia Лекция 1 ОХ 2
Лекция 1 ОХ 2 Определение самооценки
Определение самооценки Правила приема абитуриентов в 2021 году
Правила приема абитуриентов в 2021 году Натюрморт из предметов быта в технике Лессировка
Натюрморт из предметов быта в технике Лессировка Урок №13. Превращение пешки
Урок №13. Превращение пешки Строительство Ледового дворцав пригороде Анапы
Строительство Ледового дворцав пригороде Анапы Компания CS: История профессионализма, успеха, высоких технологий и довольных клиентов.
Компания CS: История профессионализма, успеха, высоких технологий и довольных клиентов. Развитие речи. Через уроки литературы к воспитанию и развитию.
Развитие речи. Через уроки литературы к воспитанию и развитию. Геолокационное приложение TravelGO. Проект
Геолокационное приложение TravelGO. Проект «Зоопарк» на голове
«Зоопарк» на голове Особенности дистрибутив Debian
Особенности дистрибутив Debian "Состояние планеты утверждается человеческими деяниями"."Каждая из пустынь была некогда цветущим лугом. Не Природа, но сами люди
"Состояние планеты утверждается человеческими деяниями"."Каждая из пустынь была некогда цветущим лугом. Не Природа, но сами люди  Школа Блогеров
Школа Блогеров Понятие и структура правовой системы
Понятие и структура правовой системы Еврейская культура. Еврейские праздники
Еврейская культура. Еврейские праздники